Clear Sky Science · es
Primera estructura cristalina de un aducto formado tras la reacción de un compuesto de vanadio con la transferrina sérica humana
Por qué importa una proteína sanguínea y un fármaco metálico
Muchos fármacos experimentales contienen átomos metálicos que pueden ayudar a tratar enfermedades que van desde la diabetes hasta el cáncer. Pero una vez que estos medicamentos basados en metales entran en el torrente sanguíneo, deben viajar unidos a las proteínas transportadoras naturales del organismo. Este estudio examina cómo una de esas proteínas, la transferrina sérica humana—el principal portador de hierro en nuestra sangre—interactúa con un prometedor compuesto de vanadio, arrojando luz sobre cómo se transportan los fármacos metálicos por el cuerpo y cómo podrían ajustarse para lograr terapias más seguras y eficaces.
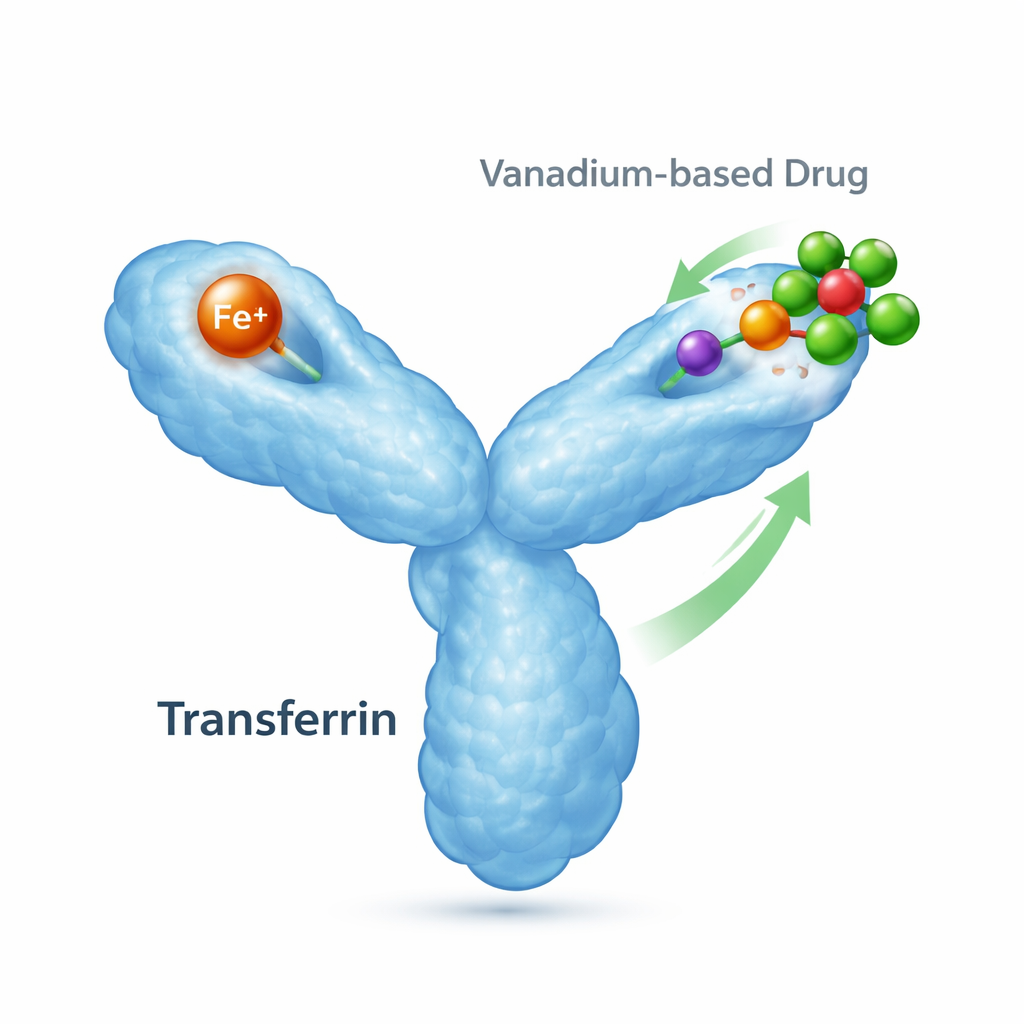
La mensajera del hierro del organismo y sus tareas secundarias
La transferrina es una proteína de 80 kilodaltons cuya función principal es capturar hierro y entregarlo a las células que lo necesitan. Tiene dos “lóbulos”, cada uno capaz de unir un ion de hierro, y cambia de forma según la presencia de hierro. Cuando el hierro se une, un lóbulo se cierra; sin hierro, permanece abierto. Receptores especializados en la superficie celular reconocen estas formas cargadas de hierro y las internalizan, lo que convierte a la transferrina en una pieza central del equilibrio del hierro y de la salud celular. Sin embargo, la transferrina también puede ligar otros metales, incluidos los procedentes de tratamientos médicos, lo que implica que puede influir en adónde viajan y cómo actúan los fármacos basados en metales.
Una instantánea estructural del vanadio en la transferrina
Los investigadores se centraron en un candidato farmacológico de vanadio bien estudiado llamado bis(acetilacetonato)oxovanadio(IV), a menudo escrito como [VIVO(acac)₂]. Trabajos anteriores mostraron que este compuesto, o especies derivadas de él en agua, pueden unirse a la transferrina, pero nadie había visto exactamente cómo. Usando cristalografía de rayos X, el equipo obtuvo estructuras de alta resolución de la transferrina que porta hierro sólo en su lóbulo C‑terminal (la forma “FeC”), tanto antes como después de la exposición al fármaco de vanadio. En los cristales tratados con vanadio observaron no el fármaco original, sino un fragmento transformado de vanadio‑oxígeno unido en el lóbulo N libre de hierro. Esto les dio la primera imagen estructural directa de un fragmento de vanadio ligado a la transferrina humana.
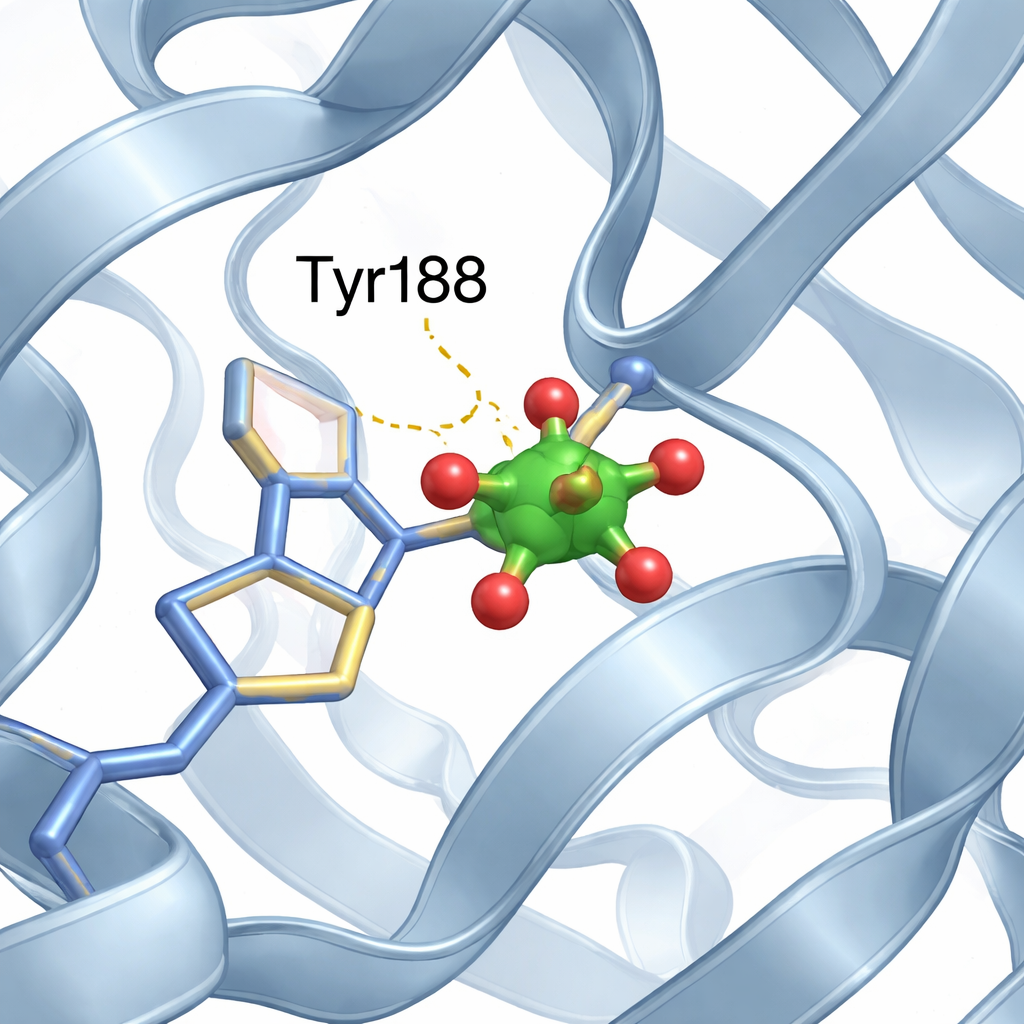
Un pequeño clúster de vanadio encuentra su hueco
En el sitio de hierro del lóbulo N, el equipo identificó un pequeño clúster formado por dos átomos de vanadio y átomos de oxígeno, que se describe mejor como una unidad modificada de “divanadato”. Una de las posiciones de oxígeno del clúster es ocupada por el oxígeno de un aminoácido específico, la tirosina 188 (Tyr188), formando un enlace directo entre la proteína y el clúster metálico. Interacciones adicionales más suaves, como enlaces de hidrógeno procedentes de segmentos proteicos próximos, estabilizan aún más el clúster en su sitio. Es importante señalar que, a pesar de este nuevo huésped metálico ocupando un bolsillo de unión al hierro, la proteína mantiene su disposición habitual de lóbulo N abierto y lóbulo C cerrado, casi idéntica a la estructura sin vanadio.
Cómo la transferrina remodela la química del vanadio
En solución, a la acidez y concentración usadas para la cristalización, la especie de dos vanadios observada en el cristal es normalmente sólo un componente minoritario; tienden a dominar clústeres de vanadio‑oxígeno más grandes. Mediciones espectroscópicas y cálculos teóricos de especiación sugieren que el fármaco de vanadio original se oxida lentamente y se descompone en agua, produciendo iones simples de vanadato que luego se ensamblan en una variedad de clústeres. La estructura cristalina indica que la transferrina estabiliza selectivamente este pequeño fragmento tipo divanadato frente a los clústeres mayores, esencialmente “escogiendo” una forma química de una mezcla compleja en solución al proporcionar un sitio de unión ajustado en Tyr188 y una red de enlaces de hidrógeno de apoyo.
Manteniendo su apretón de manos con el receptor celular
Dado que la transferrina debe unirse a un receptor en la superficie celular para entregar hierro, los investigadores preguntaron si la unión de este clúster de vanadio alteraría ese apretón de manos crucial. Usando electroforesis en gel no desnaturalizante y una técnica sensible llamada interferometría de biocapa, midieron cuán bien la transferrina tratada con vanadio se unía al receptor de la transferrina en comparación con la forma no tratada que llevaba solo hierro. Ambas se comportaron casi idénticamente, con una unión muy fuerte en el rango de los nanomolares bajos. Esto confirma que el clúster de vanadio, pese a estar alojado en el lóbulo N, no altera de forma significativa la región de la transferrina que interactúa con el receptor y, por tanto, no debería impedir que la proteína sea reconocida por las células.
Qué significa esto para los medicamentos basados en metales
Para el público general, la conclusión es que este estudio proporciona una instantánea molecular de cómo un derivado de un fármaco de vanadio se une al principal portador de hierro del organismo sin desbaratar su función normal. La transferrina puede capturar un clúster específico y pequeño de vanadio‑oxígeno en un sitio de hierro, sin que la forma global de la proteína ni su capacidad de unirse al receptor se alteren de modo apreciable. Esto ayuda a explicar cómo los fármacos de vanadio pueden circular unidos a la transferrina y destaca que distintas proteínas pueden favorecer diferentes tamaños de clústeres de vanadio. Tales hallazgos son clave para diseñar terapias metálicas más inteligentes cuya conducta en el torrente sanguíneo—qué formas adoptan, adónde se dirigen y cuánto tiempo duran—pueda predecirse y controlarse.
Cita: Banneville, AS., Lucignano, R., Paolillo, M. et al. First crystal structure of an adduct formed upon reaction of a vanadium compound with human serum transferrin. Commun Chem 9, 89 (2026). https://doi.org/10.1038/s42004-026-01891-1
Palabras clave: fármacos de vanadio, transferrina sérica humana, terapéuticos basados en metales, unión proteína–metal, biología estructural