Clear Sky Science · es
La lactama permite redistribuciones remotas de boronato hacia enlaces C═N
Un nuevo atajo para construir moléculas con aspecto farmacéutico
Los químicos siempre buscan métodos más rápidos y limpios para ensamblar las moléculas complejas presentes en medicamentos y materiales avanzados. Este estudio presenta un ingenioso atajo que permite que una estructura anular común, llamada lactama, guíe temporalmente una reacción y luego se aparte—haciendo posible convertir ingredientes simples y de fácil acceso en bloques de construcción valiosos para la industria farmacéutica sin recurrir a metales caros ni a pasos de preparación elaborados.
Convertir un ayudante silencioso en una guía temporal
Muchos fármacos modernos y materiales funcionales dependen de reacciones de ácidos borónicos, una familia de compuestos que contienen boro valorada por su fiabilidad y comportamiento suave. Tradicionalmente, para inducir que los ácidos borónicos formen nuevos enlaces con dobles enlaces carbono–nitrógeno (C=N), los químicos deben preinstalar “grupos directores” especiales en los reactivos. Estos grupos actúan como asas que orientan la reacción, pero añaden tiempo, coste y pasos—y con frecuencia solo funcionan con parejas muy reactivas. Los autores se dieron cuenta de que las lactamas, parientes anulares del amida común en las proteínas, podían servir como guías temporales integradas. Al coordinarse con el átomo de boro, el oxígeno de la lactama ayuda a formar un centro de boro altamente organizado y tetracoordinado que puede desplazar un fragmento unido hasta una posición distante a lo largo de la molécula, preparando nuevos enlaces carbono–nitrógeno sin necesidad de un grupo director permanente.
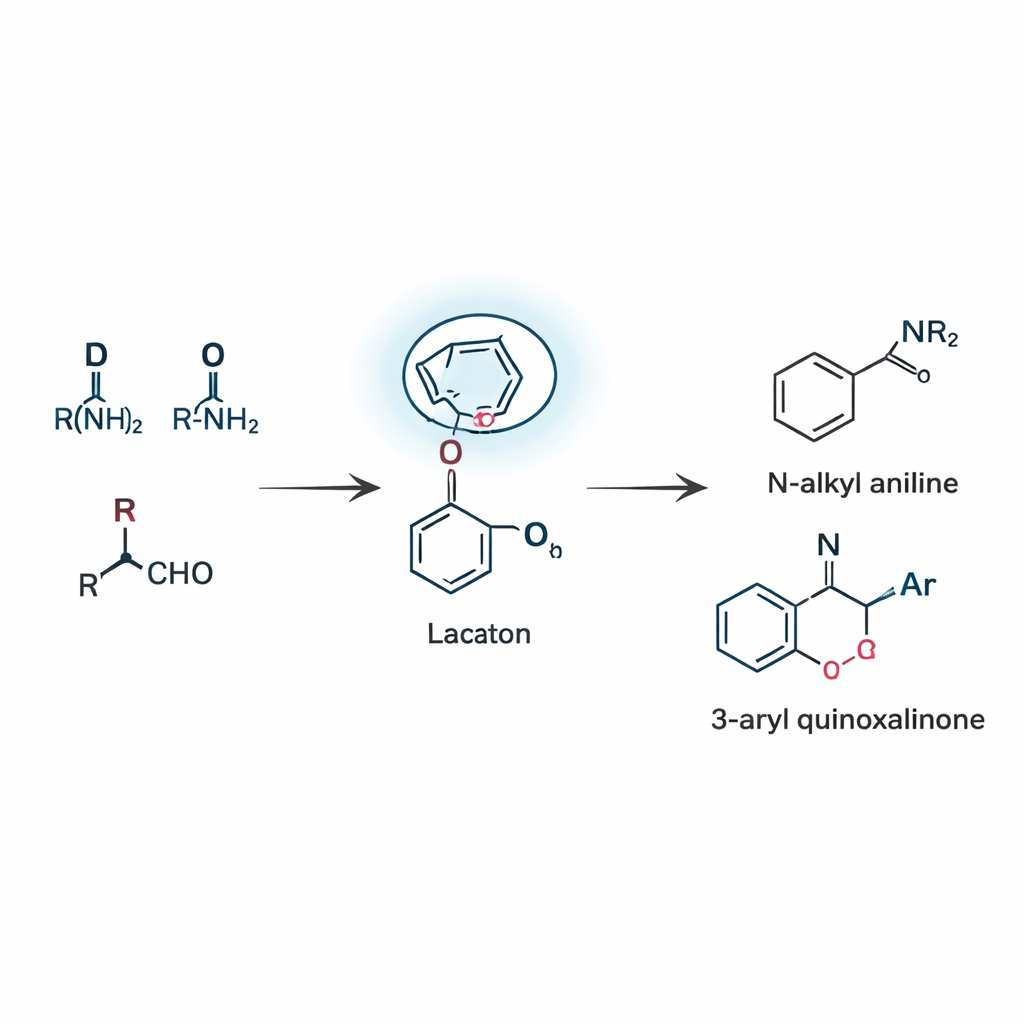
Construir dos familias de productos útiles con una sola estrategia
Aplicando este concepto, el equipo desarrolló dos reacciones relacionadas que se basan en este reordenamiento guiado por lactama, conocido como redistribución remota de boronato. En la primera, tres piezas simples—un aldehído, una amina y un ácido borónico—se combinan para formar anilinas N‑alquiladas, un motivo central que aparece en numerosos candidatos a fármacos y colorantes. La reacción transcurre mediante un raro desplazamiento 1,5, en el que un grupo arilo en el boro salta a través de cinco átomos para alcanzar el enlace C=N. Mediante un ajuste cuidadoso del catalizador, el disolvente y la temperatura, los investigadores obtuvieron rendimientos respetables y mostraron que se toleran muchos sustituyentes distintos, incluidos halógenos, grupos alquilo y heterociclos. En el segundo modo de reacción, la misma idea guía se aplica a las quinoxalinonas, una clase de anillos ricos en nitrógeno comunes en química medicinal. Aquí, la reacción no emplea ningún catalizador metálico añadido y aún así produce 3‑aril quinoxalinonas de manera eficiente, gracias a la capacidad de la lactama para interactuar con el boro y estabilizar el intermedio clave.
Condiciones verdes y edición en etapa tardía de fármacos
Más allá de demostrar un amplio alcance, los autores muestran que esta estrategia es práctica para moléculas del mundo real. Debido a que el reordenamiento 1,4 en quinoxalinonas procede en condiciones libres de metales en un alcohol especializado como disolvente, evita la necesidad de metales de transición caros o tóxicos. El equipo aplicó el método a fragmentos complejos derivados de fármacos comercializados, como el ibuprofeno, y a otros compuestos terapéuticos que contienen el andamiaje de quinoxalinona. En cada caso, la reacción instaló nuevos grupos arilo en una posición específica sin alterar otras características sensibles. Este tipo de “funcionalización en etapa tardía” permite a los químicos decorar rápidamente núcleos farmacéuticos existentes con nuevas cadenas laterales, acelerando la búsqueda de mejoras en potencia, seguridad o propiedades físicas.
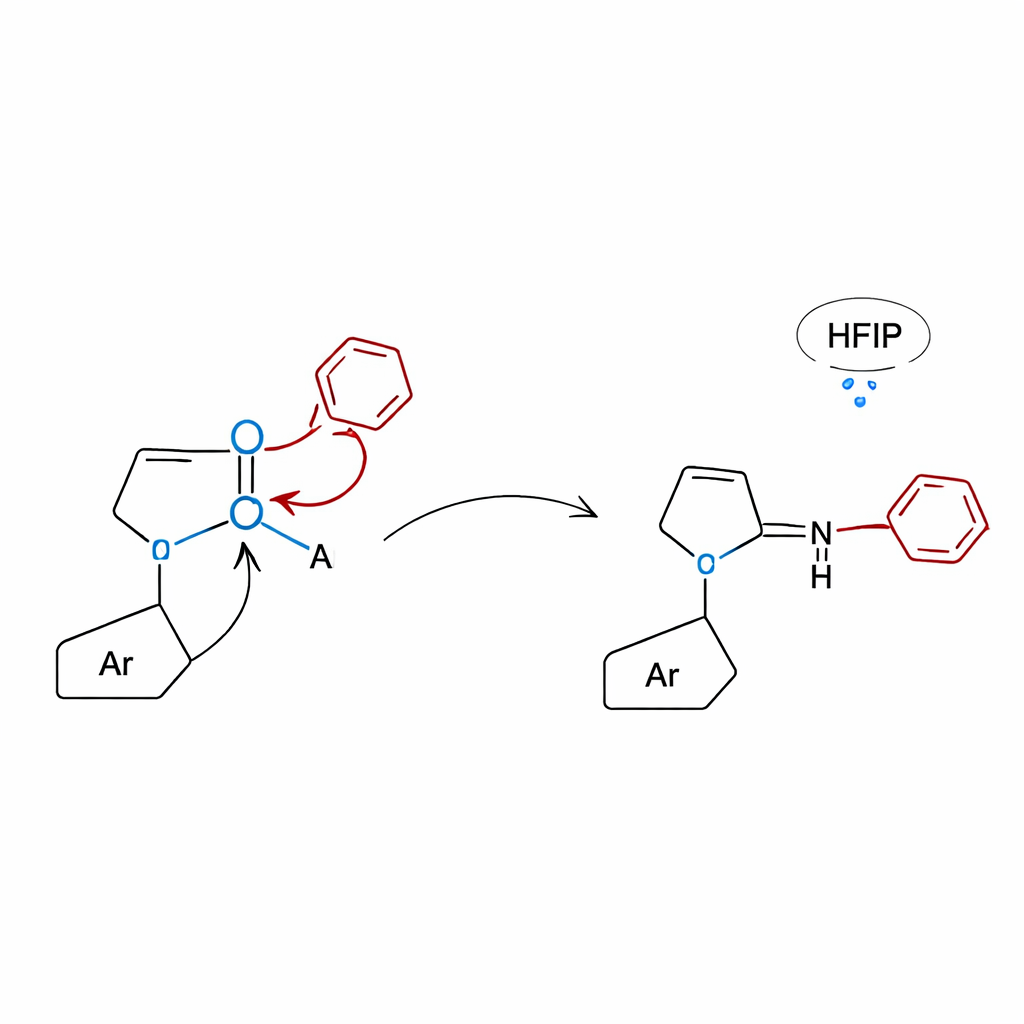
Mirando bajo el capó con teoría y pruebas de control
Para entender por qué el enfoque de la lactama funciona tan bien, los investigadores combinaron experimentos de control cuidadosamente diseñados con simulaciones por ordenador. Cuando se probaron moléculas carentes de la porción de lactama, las reacciones prácticamente se detuvieron, lo que confirma que el anillo de lactama es esencial para activar el ácido borónico y dirigir el reordenamiento. Cálculos cuántico‑químicos revelaron que el oxígeno de la lactama se une al boro para formar una estructura compacta tetracoordinada desde la cual el grupo arilo puede migrar bien sea a través de cinco átomos (desplazamiento 1,5) para dar anilinas N‑alquiladas o a través de cuatro átomos (desplazamiento 1,4) para dar 3‑aril quinoxalinonas. En el caso de las quinoxalinonas, la red de enlaces por puente de hidrógeno proporcionada por el disolvente HFIP reduce además la barrera energética, ayudando a que la reacción avance en condiciones térmicas relativamente suaves sin ningún catalizador añadido.
Por qué esto importa para futuros medicamentos
En conjunto, el trabajo demuestra que un simple anillo de lactama puede actuar como una guía dinámica y reciclable que desbloquea patrones de formación de enlaces previamente inaccesibles en la química de ácidos borónicos. Para los no especialistas, el mensaje clave es que los químicos disponen ahora de una vía más directa y eficiente para convertir bloques de construcción básicos en dos clases importantes de moléculas ricas en nitrógeno que sustentan muchos fármacos. Dado que el método evita metales preciosos, tolera una amplia gama de grupos funcionales y funciona en estructuras avanzadas de tipo farmacéutico, está bien posicionado para ayudar a agilizar el diseño y la optimización de futuros productos farmacéuticos y, potencialmente, de nuevos agroquímicos también.
Cita: Lei, J., Xu, J., Li, X. et al. Lactam enables remote boronate rearrangements to C═N bonds. Commun Chem 9, 88 (2026). https://doi.org/10.1038/s42004-026-01890-2
Palabras clave: ácidos borónicos, química de lactamas, formación de enlaces C–N, quinoxalinonas, química medicinal