Clear Sky Science · es
La mutación del síndrome PACS1 altera el transporte de carga mediado por dineína a través de HDAC6 y BICD2
Por qué esto importa para el desarrollo cerebral
El síndrome PACS1 es una afección genética rara que provoca discapacidad intelectual, convulsiones y rasgos faciales distintivos. Las familias y los clínicos reconocen los síntomas, pero hasta hace poco no estaba claro qué fallaba exactamente dentro de las células de los pacientes. Este estudio desentraña ese misterio, mostrando cómo un cambio de una sola letra en el gen PACS1 desordena el sistema de transporte interno de la célula, sobre todo en las neuronas, y cómo eso conecta el síndrome PACS1 con una familia más amplia de enfermedades neuronales de “tráfico”. 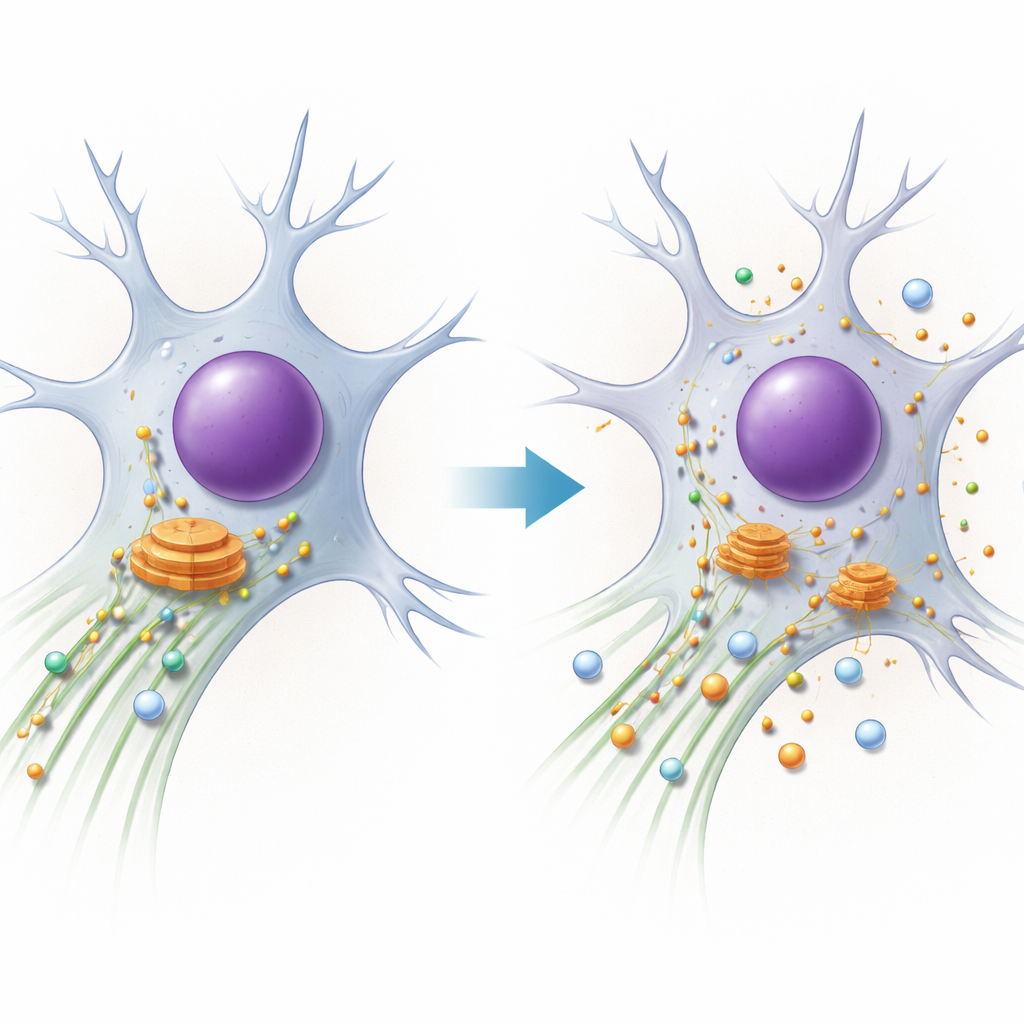
Las autopistas de reparto de la célula
Cada célula depende de autopistas microscópicas formadas por tubos proteicos llamados microtúbulos. Motores moleculares recorren estas vías, transportando cargas como enzimas y compartimentos de membrana hacia donde se necesitan. Un motor, la dineína, es responsable de los “viajes de retorno” de larga distancia, tirando de la carga desde la periferia celular hacia el centro, donde se encuentra una estación de clasificación importante llamada aparato de Golgi. Los autores se centran en PACS1, una proteína que ayuda a seleccionar qué carga usa la dineína y que además ajusta el estado de las vías mediante otra proteína, HDAC6, que controla una etiqueta química (acetilación) en los microtúbulos. Las neuronas, con sus extensiones muy largas, son especialmente sensibles incluso a pequeñas fallas en este sistema.
Un coordinador mutante que se agarra con demasiada fuerza
El síndrome PACS1 se debe a la mutación recurrente R203W en PACS1. El equipo halló que tanto PACS1 normal como el mutante se unen físicamente a la cadena pesada de la dineína, pero la forma mutante se aferra con mayor fuerza. Usando células dérmicas de pacientes y líneas celulares modificadas, demostraron que este exceso de interacción produce el mismo resultado que una pérdida parcial de la función de la dineína: el Golgi se desintegra en mini‑pilas dispersas y una enzima importante llamada furina, que normalmente se localiza en el lado trans del Golgi, se desvía hacia otros compartimentos. Al diseccionar la estructura de PACS1, localizaron un breve parche en forma de tira beta que contacta específicamente con la dineína. Cuando alteraron ese parche sin perturbar otras funciones de PACS1, la furina volvió a perder su localización correcta, confirmando que el apretón entre dineína y PACS1 es crucial para colocar la carga en su sitio. 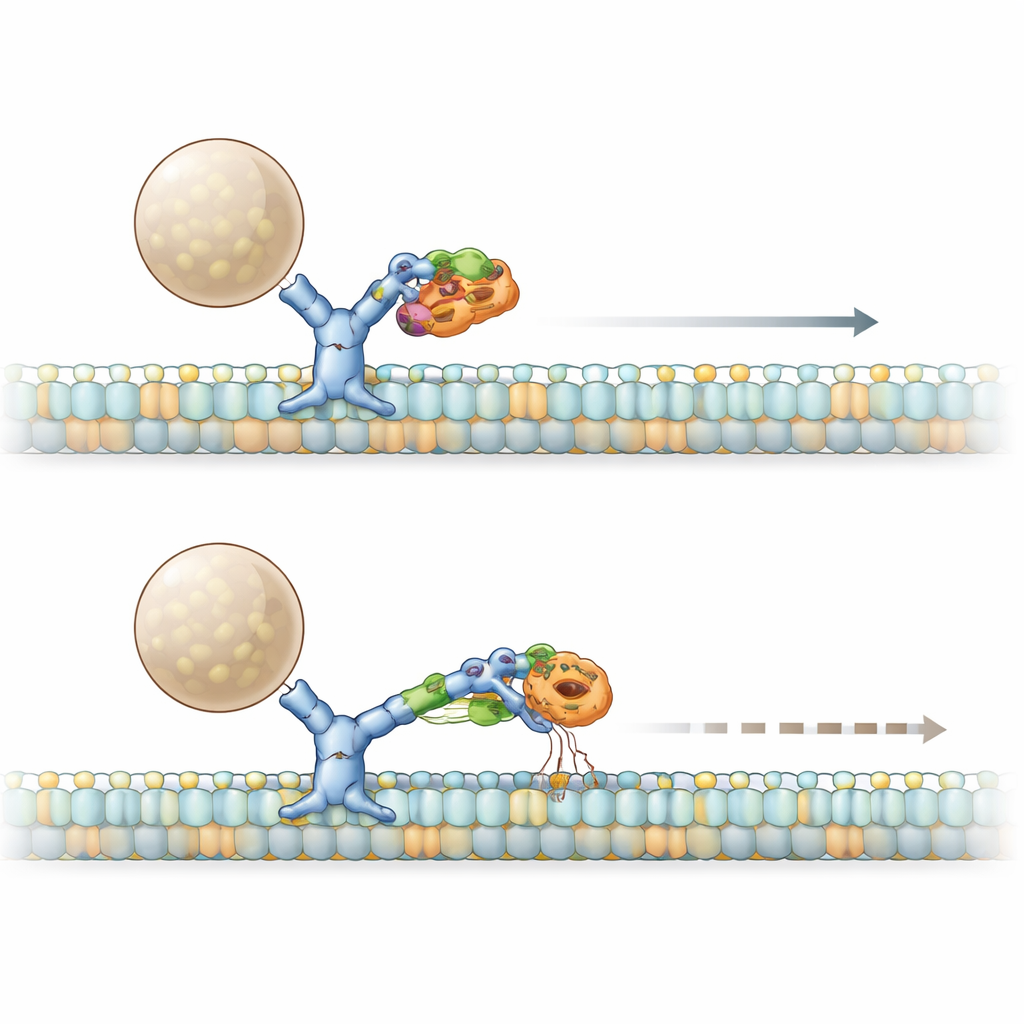
Cómo una alianza de tres proteínas atasca el motor
La historia se complica con dos actores adicionales: HDAC6 y un adaptador llamado BICD2, que ayuda a ensamblar complejos activos de dineína. PACS1 mutante no solo aumenta la actividad de HDAC6, reduciendo la acetilación en los microtúbulos, sino que también forma un complejo ampliado con HDAC6 y BICD2. Pruebas bioquímicas revelaron que, juntos, PACS1 mutante y HDAC6 separan a BICD2 de la dineína mientras mantienen su asociación con un motor que avanza (kinesina). En células vivas, una carga artificial que normalmente avanza rápidamente impulsada por la dineína se ralentizó y menos cargas se movieron cuando estaba presente PACS1 mutante. Bloquear la actividad de HDAC6 restauró tanto la velocidad como el número de partículas en movimiento, mostrando que el ensamblaje PACS1 mutante–HDAC6–BICD2 actúa como un freno sobre la capacidad de la dineína para iniciar y mantener el transporte.
Rescatando el tráfico con un ayudante natural de la dineína
Los investigadores probaron si la dineína podía “re‑activarse” a pesar del complejo mutante. Recurrieron a Lis1, un conocido ayudante de la dineína que estabiliza los ensamblajes motores activos. En las células de pacientes, los niveles de Lis1 estaban algo reducidos. Cuando el equipo añadió Lis1 en exceso, mejoraron dos aspectos: el Golgi volvió a reagruparse cerca del centro celular y los lisosomas, otra clase de orgánulos que se habían desplazado hacia afuera, regresaron a su lugar. En el mismo ensayo de motilidad, Lis1 aumentó tanto la frecuencia como la velocidad del movimiento de cargas impulsadas por dineína en presencia de PACS1 mutante. Estos resultados muestran que el problema no es la ausencia de dineína, sino que queda atrapada en un estado poco activo, un estado que puede corregirse parcialmente ya sea atenuando HDAC6 o reforzando la activación de la dineína.
Conectando un síndrome raro con un conjunto más amplio de trastornos
Combinando análisis estructural, biología celular e imágenes en vivo, los autores proponen un modelo claro: PACS1 normalmente enlaza cargas seleccionadas a la dineína y ajusta el rendimiento del motor a través de HDAC6 y la acetilación de microtúbulos. La mutación R203W abre la superficie de interacción de PACS1, reclutando en exceso a HDAC6 y BICD2 en un complejo que socava la capacidad de la dineína para enganchar microtúbulos y moverse eficientemente. El resultado es una distribución errónea generalizada del Golgi, los lisosomas y otras cargas, particularmente en las neuronas donde el transporte a larga distancia es vital. Este mecanismo ayuda a explicar por qué reducir PACS1 o HDAC6 con terapias antisense corrige defectos cerebrales en modelos murinos y está siendo explorado ahora en pacientes. Más ampliamente, sitúa al síndrome PACS1 dentro del espectro creciente de trastornos del tráfico en microtúbulos, junto a afecciones causadas por mutaciones en dineína, BICD2 y factores de transporte relacionados.
Cita: Yang, Y., Thomas, L., Chen, K. et al. PACS1 syndrome mutation disrupts dynein-mediated cargo transport via HDAC6 and BICD2. Commun Biol 9, 450 (2026). https://doi.org/10.1038/s42003-026-09924-0
Palabras clave: Síndrome PACS1, transporte por dineína, tráfico en microtúbulos, organización del aparato de Golgi, desarrollo neuronal