Clear Sky Science · es
La proteína secretada CLCF1 mejora la enfermedad hepática colestásica al inhibir la síntesis hepática de ácidos biliares y promover su excreción
Por qué esta investigación importa para la salud del hígado
Las enfermedades hepáticas colestásicas son condiciones en las que la bilis, un fluido digestivo producido por el hígado, deja de fluir correctamente y se acumula, intoxicando gradualmente el hígado desde dentro. Los medicamentos actuales solo ayudan a una fracción de los pacientes y muchos acaban necesitando un trasplante de hígado. Este estudio descubre una proteína producida de forma natural, llamada CLCF1, que el organismo parece activar como un sistema de defensa durante la colestasis hepática. Comprender cómo funciona esta proteína podría señalar el camino hacia nuevos tratamientos que protejan el hígado tanto reduciendo la producción de componentes biliares perjudiciales como ayudando al cuerpo a eliminarlos con mayor eficacia.
Un ayudante oculto en hígados enfermos
Los investigadores empezaron examinando tejido hepático de pacientes con colangitis biliar primaria y colangitis esclerosante primaria, dos formas principales de enfermedad hepática colestásica crónica. Compararon personas con enfermedad en estadios tempranos con otras en colestasis más avanzada y también analizaron conjuntos de datos genéticos públicos existentes. A través de estas fuentes humanas independientes, una proteína secretada destacó: CLCF1 estuvo de forma consistente entre los genes más aumentados en hígados colestásicos. Niveles más altos de CLCF1 se asociaron con peores marcadores sanguíneos de gravedad de la enfermedad, lo que sugiere que el hígado incrementa esta proteína a medida que empeoran el estrés y la acumulación de bilis. En pacientes en estadio temprano tratados con el fármaco estándar ácido ursodesoxicólico, quienes respondieron bien tendían a tener más CLCF1 en sus hígados, lo que insinúa que esta proteína podría señalar un hígado más adaptable y sensible al tratamiento.
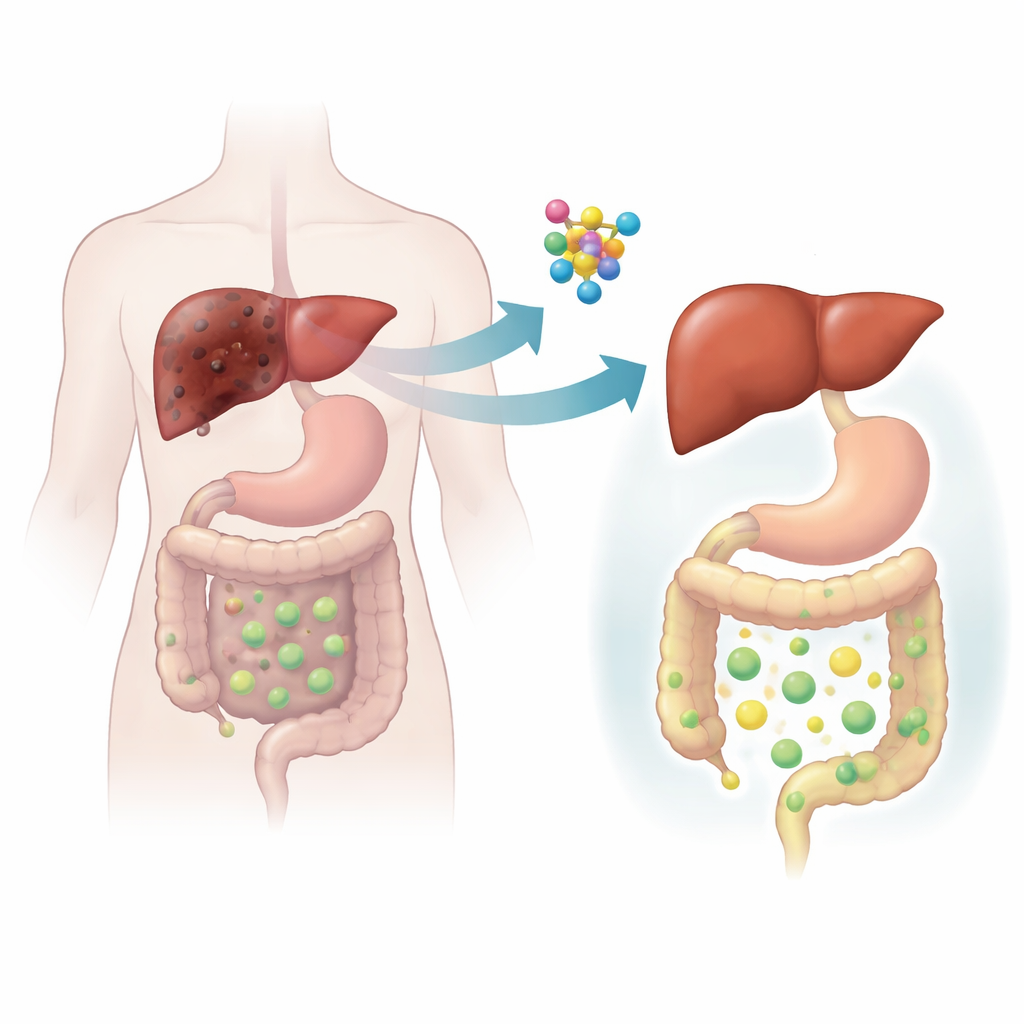
Probando CLCF1 en modelos animales
Para ir más allá de las correlaciones humanas, el equipo recurrió a ratones y usó trucos genéticos y dietéticos para imitar la enfermedad hepática colestásica. En dos modelos distintos de ratón, la colestasis aumentó fuertemente la producción hepática de Clcf1, reflejando los hallazgos en humanos. Cuando los científicos eliminaron específicamente el receptor de CLCF1 en las células hepáticas, la lesión colestásica empeoró mucho: los conductos biliares crecieron en exceso, el tejido hepático sufrió necrosis, aumentó la inflamación, se acumuló tejido cicatricial y se acumularon ácidos biliares tóxicos. El experimento inverso contó una historia más esperanzadora. Cuando el equipo usó un virus inofensivo para aumentar los niveles de Clcf1 únicamente en el hígado, los ratones quedaron protegidos. Sus hígados se mostraron más saludables, las analíticas sanguíneas mejoraron, se redujo la fibrosis y la cantidad de ácidos biliares retenidos en el hígado disminuyó notablemente.
Reducir el grifo y abrir el desagüe
¿Cómo reduce CLCF1 la sobrecarga de ácidos biliares con tanta eficacia? Los investigadores hallaron dos acciones complementarias. Primero, CLCF1 calmó directamente la propia maquinaria hepática de producción de bilis. En varios modelos de ratón y en cultivos de células hepáticas, la CLCF1 adicional apagó de forma consistente enzimas clave que convierten el colesterol en ácidos biliares, cerrando efectivamente el grifo a la producción nueva de bilis. Esto ocurrió sin activar el regulador nuclear habitual del hígado para el control de la bilis, un receptor llamado FXR, lo que sugiere que CLCF1 utiliza una vía alternativa dentro de las células hepáticas para frenar la síntesis de bilis. Segundo, CLCF1 influyó en cómo se manejaba la bilis más adelante en el organismo. Remodeló la comunidad microbiana intestinal hacia bacterias particularmente eficaces en procesar ácidos biliares e incrementó la cantidad de ácidos biliares que salen del cuerpo en las heces, actuando como un desagüe más eficaz.
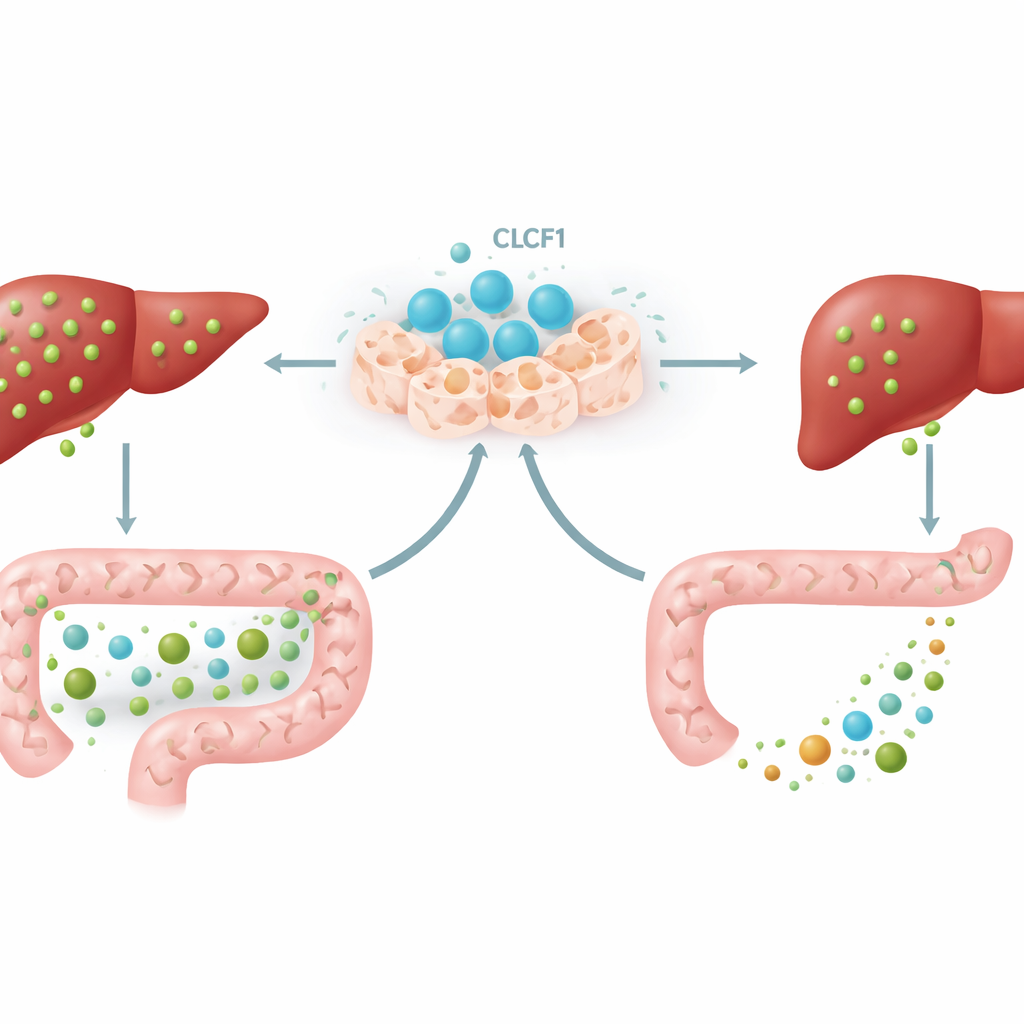
La conversación intestino–hígado
Una pieza clave del rompecabezas implicó un circuito de señalización entre el intestino y el hígado. Ciertos ácidos biliares en el intestino activan un sensor llamado FXR en las células intestinales, que luego liberan una hormona mensajera conocida como FGF15 en ratones. Esta hormona viaja por la sangre hasta el hígado y le indica que reduzca la producción de ácidos biliares. Con CLCF1 adicional, los ratones acumularon tipos específicos de ácidos biliares en sus intestinos—particularmente formas conocidas por ser potentes activadores de FXR. Como resultado, el FXR intestinal se activó, los niveles de FGF15 aumentaron tanto en intestino como en hígado, y el hígado redujo aún más su producción de ácidos biliares. Cuando los científicos bloquearon el FXR intestinal con un fármaco de acción limitada al intestino, gran parte del efecto protector de CLCF1 se desvaneció, demostrando que esta conversación intestino–hígado es una parte esencial de la acción de la proteína.
Qué podría significar esto para tratamientos futuros
En conjunto, estos hallazgos describen a CLCF1 como una válvula de seguridad incorporada para la enfermedad hepática colestásica. La proteína reduce los niveles de ácidos biliares desde ambos extremos: ralentiza su creación dentro del hígado y fomenta su eliminación a través del intestino, ayudada por microbios intestinales beneficiosos y una señal hormonal de retroalimentación. A diferencia de los fármacos existentes que activan FXR en todo el cuerpo y pueden causar efectos secundarios como prurito y alteraciones de los lípidos sanguíneos, CLCF1 parece dirigir el control de la bilis de manera más suave y selectiva, especialmente a través del intestino. Aunque este trabajo aún está en ratones y muestras de laboratorio, sugiere que aumentar CLCF1 o imitar sus vías podría constituir la base de nuevas terapias—y que medir esta proteína, o los ácidos biliares que enriquece en el intestino, podría ayudar a identificar a los pacientes que más se beneficiarían.
Cita: Liu, M., Su, Y., Hu, Y. et al. The secretory protein, CLCF1, improves cholestatic liver disease by inhibiting hepatic bile acid synthesis and promoting bile acid excretion. Commun Biol 9, 370 (2026). https://doi.org/10.1038/s42003-026-09847-w
Palabras clave: enfermedad hepática colestásica, ácidos biliares, eje intestino–hígado, CLCF1, microbiota intestinal