Clear Sky Science · es
El sistema de secreción tipo VI de Acinetobacter: mecanismos, biología y potencial terapéutico
Armas ocultas en los gérmenes hospitalarios
Muchas personas saben que algunos gérmenes hospitalarios pueden resistir los antibióticos, pero son menos las que se dan cuenta de que estos microbios también libran batallas encarnizadas entre sí. Esta revisión examina una “lanza cargada por resorte” microscópica dentro de Acinetobacter, un grupo de bacterias que incluye al notorio patógeno hospitalario Acinetobacter baumannii. Comprender cómo funciona esta arma incorporada, cuándo se activa y cómo ayuda a establecer infecciones podría abrir nuevas vías para diagnosticar y desarmar infecciones resistentes a los fármacos y potencialmente mortales.
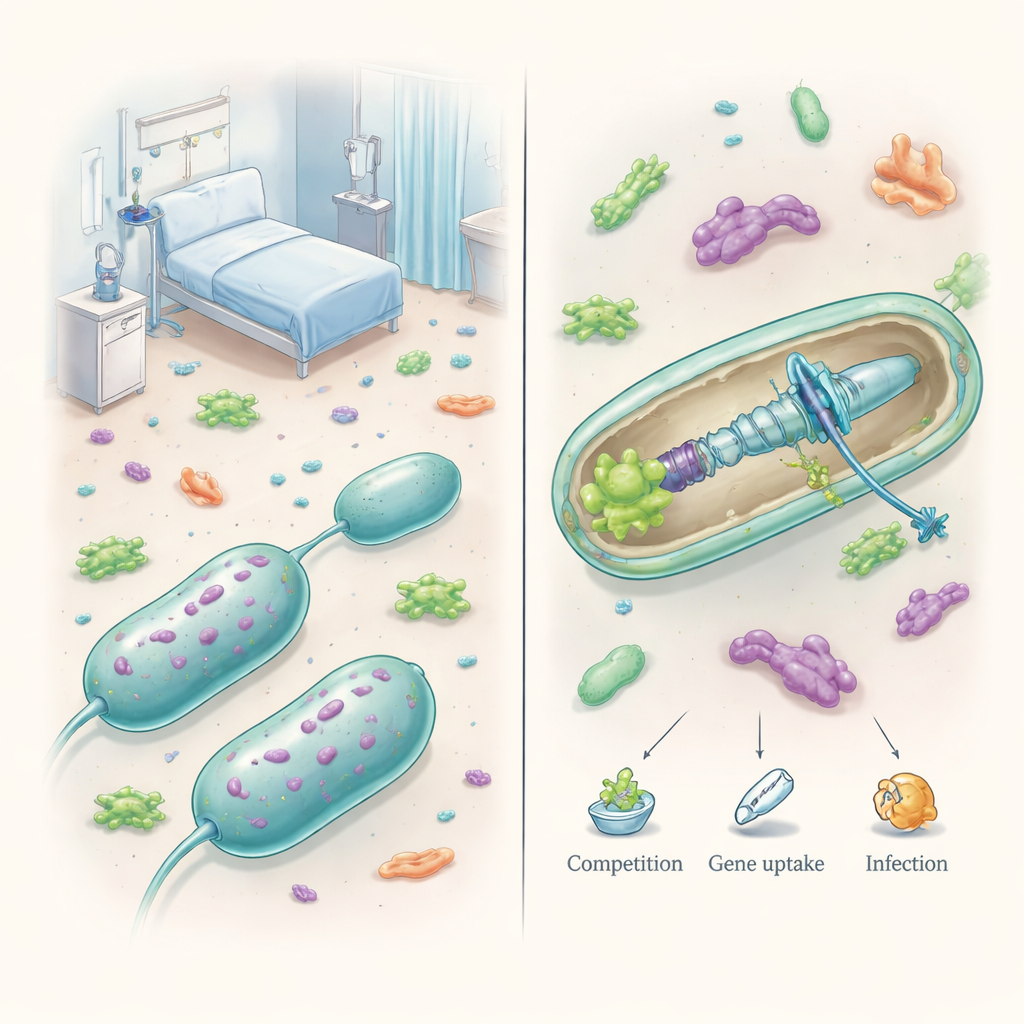
Una máquina de supervivencia, no solo un dardo venenoso
Las especies de Acinetobacter viven en el suelo, en el agua y en nuestra piel, pero algunas se han convertido en patógenos hospitalarios muy exitosos. Una herramienta clave de su arsenal es el sistema de secreción tipo VI, o T6SS, una diminuta máquina contráctil anclada en la envoltura celular. Cuando se dispara, lanza una punta similar a una aguja cargada con proteínas tóxicas hacia las células vecinas, a menudo matando a las bacterias competidoras por contacto. A diferencia de otros gérmenes que llevan varias versiones de este sistema, los Acinetobacter patógenos suelen tener un solo T6SS, sin embargo han reconvertido esta única plataforma para servir a múltiples propósitos, desde repeler rivales hasta moldear las infecciones.
Hardware reconstruido: una plataforma de lanzamiento inusual
La mayoría de las bacterias construyen su T6SS alrededor de un conjunto estándar de piezas, pero Acinetobacter ha remodelado varias piezas clave. Carece de un anclaje común en la membrana externa llamado TssJ y, en su lugar, depende de un trío de ayudantes especializados: TsmK forma una base en la membrana interna, TslA estabiliza una larga proteína “túnel” (TssM) mientras atraviesa la pared celular, y TagX corta localmente la pared para dejar paso al arma. Además, una proteína de la espiga en particular, VgrG1, debe tener una forma casi perfecta para que el sistema pueda disparar: cambios de un solo aminoácido pueden desactivarla. En conjunto, estos ajustes muestran cómo la evolución puede reemplazar piezas ausentes con nuevas soluciones mientras preserva el principio básico de disparo.
Controles inteligentes: cuándo tiene sentido el modo ataque
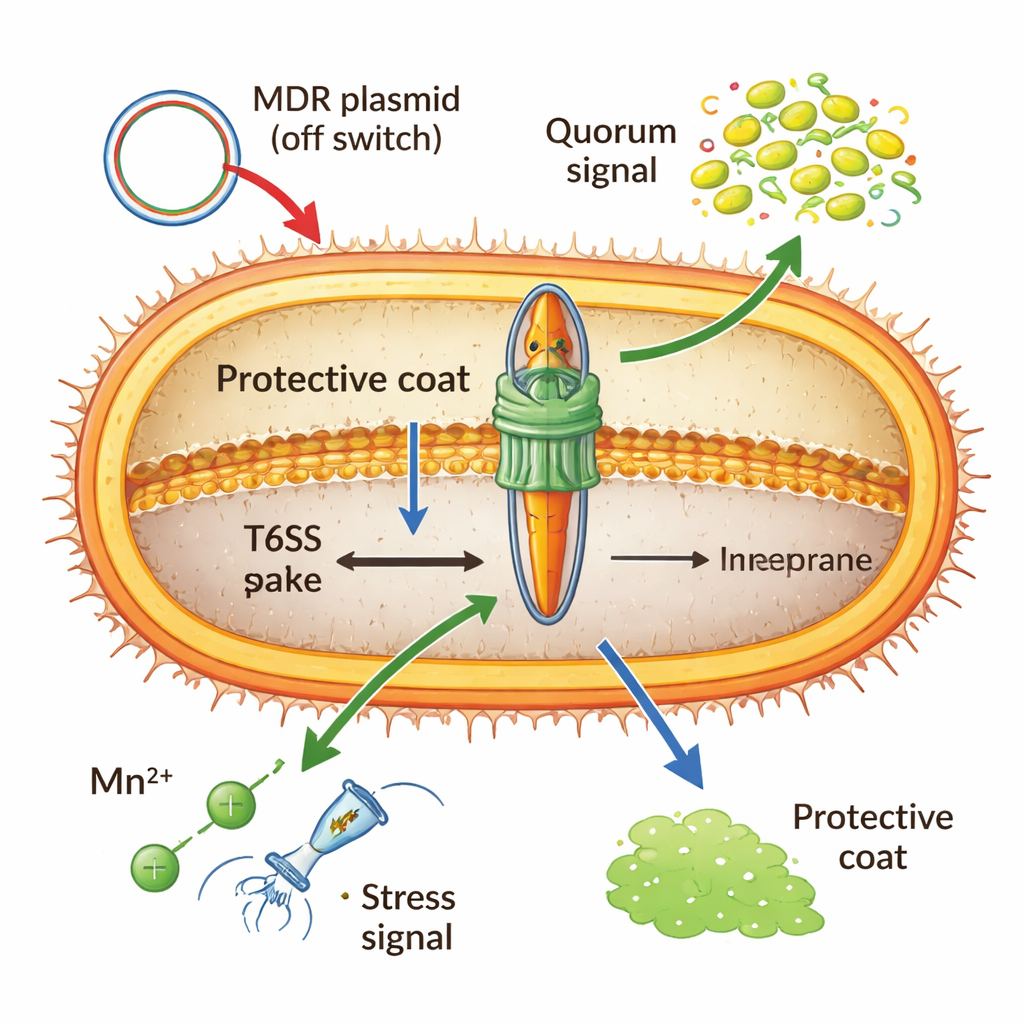
Construir y disparar esta nanomáquina es costoso, por lo que Acinetobacter la mantiene bajo estricto control. Una proteína global que se une al ADN (H‑NS) y represores especiales llevados en plásmidos multirresistentes pueden bloquear el sistema en la posición de “apagado”, especialmente cuando se comparten genes de resistencia entre células. A gran densidad celular, señales químicas de “quórum” pueden activarlo, preparando a las bacterias para la competencia a corta distancia. Los iones metálicos también intervienen: bajo estrés oxidativo, el manganeso importado activa un pequeño ARN que provoca la destrucción de mensajes clave del T6SS, reduciendo el arma para favorecer la supervivencia dentro del huésped. Incluso la cápsula —una cubierta externa azucarada— actúa a la vez como escudo y freno, bloqueando ataques entrantes pero también amortiguando físicamente el propio disparo de Acinetobacter.
Un kit diverso de golpes microscópicos
Cuando Acinetobacter aprieta el gatillo, puede entregar una amplia gama de toxinas. Algunas enzimas degradan la resistente pared celular de los rivales; otras erosionan silenciosamente las membranas celulares, y otras cortan el ADN dentro de las células objetivo. Cada toxina va emparejada con una proteína de “inmunidad” que protege al atacante del fuego amigo. Una toxina que corta ADN, ahora llamada TafE, puede incluso matar hongos, lo que sugiere escaramuzas entre diferentes reinos en lugares como el intestino o los pulmones. Los estudios genómicos indican que Acinetobacter codifica muchas más toxinas aún no caracterizadas, a menudo agrupadas en grandes proteínas Rhs que actúan como portadores modulares. En lugar de depender de un solo golpe, estas bacterias parecen usar ataques en capas que dañan varias estructuras esenciales a la vez.
Modelando infecciones, genes y tratamientos futuros
La evidencia de aislamientos de pacientes y modelos animales sugiere que un T6SS activo a menudo va de la mano con una enfermedad más grave, una inflamación más intensa y una mejor supervivencia de las bacterias dentro de los huéspedes. Al matar microbios vecinos, el sistema también libera ADN que las células de Acinetobacter naturalmente competentes pueden absorber, acelerando la difusión de rasgos como la resistencia a antibióticos. Sin embargo, mantener el arma constantemente activa es costoso, por lo que muchas cepas hospitalarias exitosas llevan plásmidos o mutaciones que la silencian una vez que la resistencia está asegurada. En conjunto, los autores sostienen que este sistema de secreción no debe verse como un simple factor de virulencia, sino como un “módulo de aptitud” flexible que Acinetobacter ajusta al alza o a la baja para equilibrar agresividad, persistencia y gasto energético. Esta nueva perspectiva apunta a aplicaciones prácticas, desde vacunas que apunten a partes conservadas del T6SS hasta fármacos que bloqueen selectivamente el mecanismo de disparo, ayudando a los médicos a burlar a un enemigo hospitalario peligroso y adaptable.
Cita: Jie, J., Gu, S., Li, D. et al. The type VI secretion system of Acinetobacter: mechanisms, biology and therapeutic potential. Commun Biol 9, 327 (2026). https://doi.org/10.1038/s42003-026-09782-w
Palabras clave: Acinetobacter, sistema de secreción tipo VI, resistencia a los antibióticos, competencia bacteriana, infecciones hospitalarias