Clear Sky Science · es
Optimización de la precisión del CRISPR en embriones de ratón mediante un enfoque dominado por la unión por microhomología
Por qué importa obtener ratones editados genéticamente con mayor precisión
Herramientas de edición genética como CRISPR han hecho notablemente sencillo crear ratones que modelan enfermedades humanas, pero existe un problema oculto: los cambios genéticos en la primera generación de animales suelen ser desordenados y heterogéneos. Eso ralentiza los experimentos, reduce su fiabilidad y requiere más animales. Este estudio presenta una forma de orientar los cortes de CRISPR en embriones de ratón hacia resultados altamente predecibles, de modo que la mayoría de los animales fundadores nazcan con la misma mutación bien definida, aportando biología más limpia y una ética mejorada a la investigación con edición genética.
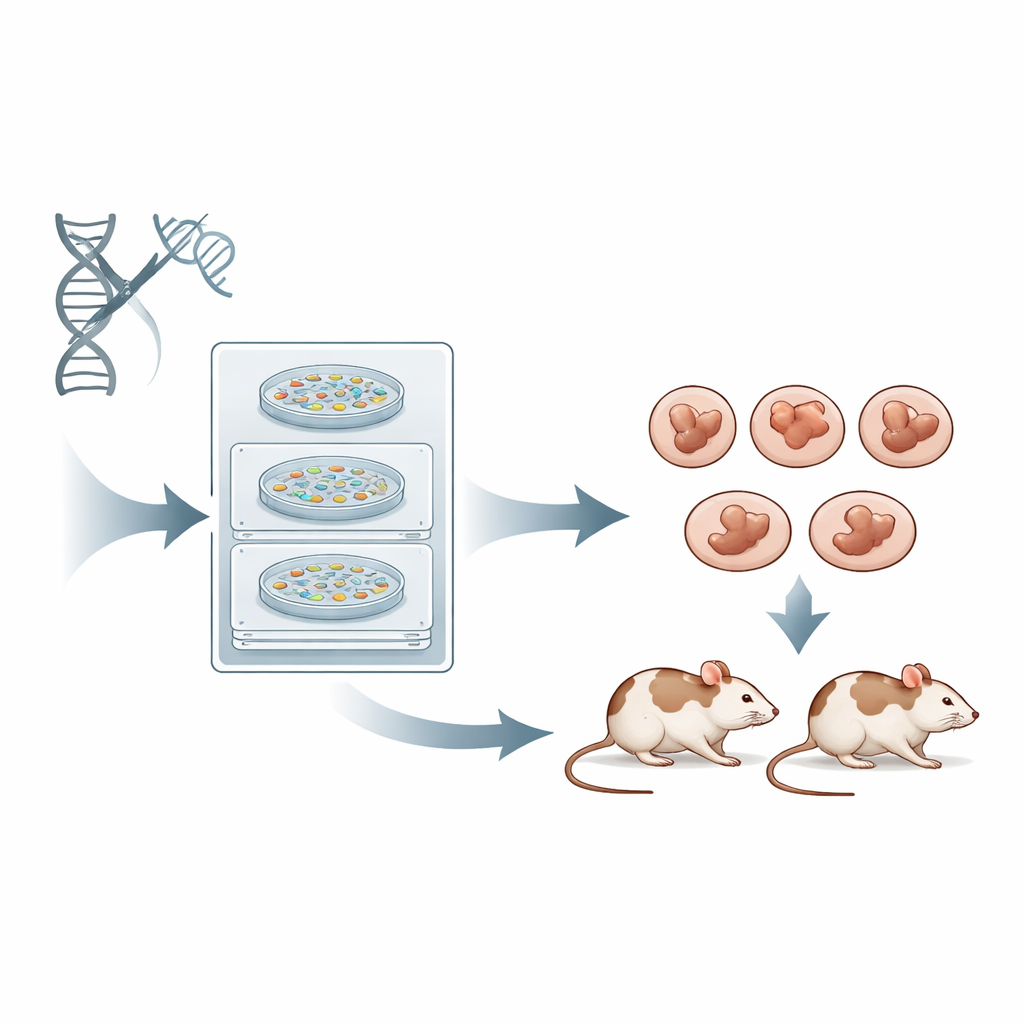
El desafío de las reparaciones de ADN desordenadas
Cuando CRISPR corta el ADN, la célula debe reparar la rotura usando sus propios sistemas de reparación. La vía más común, llamada unión no homóloga (NHEJ), es rápida pero imprecisa, produciendo una mezcolanza de pequeñas inserciones y deleciones en el sitio de corte. Otra vía, la unión por microhomología (MMEJ), tiende a eliminar fragmentos de ADN de forma estereotipada usando secuencias cortas coincidentes como guías. Ambas son mucho más eficientes que la ruta precisa pero lenta dirigida por homología (HDR). En experimentos estándar con CRISPR, los científicos se centran principalmente en cuán eficaz puede cortar un ARN guía y en minimizar los sitios fuera de objetivo, prestando mucha menos atención a qué vía de reparación se favorecerá o a cuál mutación exacta resultará. El resultado es que muchos ratones fundadores portan un mosaico de mutaciones diferentes en distintas células, obligando a los investigadores a cruzarlos hasta la siguiente generación antes de poder trabajar con un genotipo limpio y uniforme.
Una manera más inteligente de elegir guías CRISPR
Los autores se propusieron cambiar este guion diseñando guías no solo por eficacia y seguridad, sino también por predictibilidad. Comenzaron con inDelphi, una herramienta de aprendizaje automático entrenada con grandes conjuntos de datos de mutaciones inducidas por CRISPR en células en cultivo. inDelphi no solo indica con qué frecuencia se editará un sitio; predice el conjunto completo de posibles inserciones y deleciones y la frecuencia de cada una, con atención especial a los eventos impulsados por microhomología. El equipo examinó el gen de la tirosinasa (Tyr) en ratón, donde la pérdida de función vuelve albinos a los animales, y seleccionó ARN guía predichos para favorecer deleciones por microhomología fuertes y repetibles, manteniendo bajos los riesgos fuera de objetivo. Luego editaron embriones de ratón y midieron las mutaciones resultantes mediante secuenciación profunda. En general, el genotipo preferido por inDelphi para cada guía apareció en los embriones con frecuencias similares a las predichas, y las guías con características de microhomología más fuertes efectivamente produjeron patrones de mutación más uniformes.
Usar células madre como escenario de ensayo
Sin embargo, la predicción por sí sola no fue suficiente. Cuando el equipo comparó los pronósticos de inDelphi con los patrones reales de edición, encontró solo un acuerdo moderado. Para salvar esta brecha, introdujeron un paso intermedio práctico: probar cada guía en células madre embrionarias de ratón que comparten muchas características con los embriones muy tempranos. Tras transfectar estas células con los componentes de CRISPR, clasificaron las células editadas y secuenciaron los sitios objetivo. Los patrones de mutación en las células madre coincidieron con los de los embriones mucho más estrechamente que el modelo informático. Las guías que produjeron una deleción dominante en células madre típicamente hicieron lo mismo en blastocistos y embriones en etapas posteriores. Al combinar la clasificación de inDelphi con este “ensayo general” en células madre, los investigadores pudieron elegir de forma fiable guías que impulsan la reparación por microhomología y minimizan la diversidad de alelos mutantes.
Del color de ojos a miembros ausentes
Los autores pusieron a prueba su flujo de trabajo en animales vivos. Para el gen Tyr, eligieron tres guías representando precisión alta, media y baja según la predicción, e implantaron embriones editados en madres nodrizas. En el día 11.5 de desarrollo examinaron la pigmentación ocular y secuenciaron cada embrión de forma individual. La guía con fuerte preferencia por microhomología produjo embriones mayoritariamente albinos que llevaban una deleción pequeña dominante, a menudo en ambas copias del gen, con muy poca variación. Una guía menos optimizada produjo una mezcla de pérdida de pigmento y pigmentación parcial ligada a un conjunto más complejo de mutaciones. Aplicaron luego el mismo enfoque al gen Fgf10, cuya pérdida de función da lugar a embriones sin extremidades. Seleccionando una guía predicha —y confirmada en células madre— para generar una deleción específica de cuatro bases con alta probabilidad de interrumpir el gen, obtuvieron embriones al día 15.5 uniformemente sin extremidades y portadores de un conjunto fuertemente enriquecido de las deleciones esperadas. En ambos genes, los mismos pocos tipos de mutación dominaron en las predicciones de inDelphi, en las células madre, en embriones tempranos y en embriones en etapas posteriores.
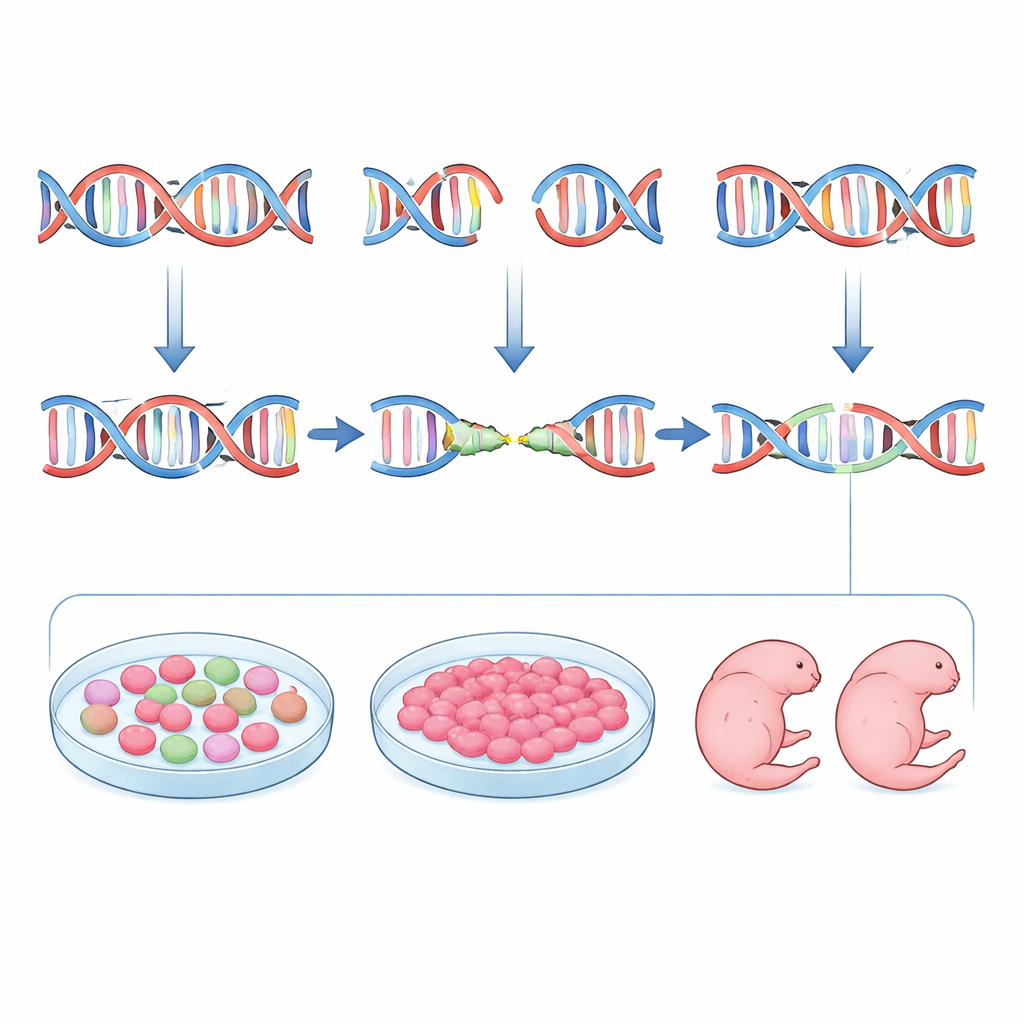
Genética más limpia con menos animales
En términos prácticos, el estudio ofrece una nueva plantilla para diseñar experimentos CRISPR en ratones. En lugar de pasar apresuradamente de una guía diseñada por ordenador a la edición de embriones, los autores recomiendan una canalización integrada: usar inDelphi y herramientas de predicción de fuera de objetivo para elegir guías que probablemente favorezcan deleciones por microhomología y cambios de marco, probar esas guías en células madre embrionarias para confirmar tanto la eficiencia como la uniformidad de las mutaciones, y avanzar a embriones solo con las guías mejores. Esta estrategia produce ratones fundadores cuyas células comparten abrumadoramente la misma mutación bien caracterizada, haciéndolos inmediatamente útiles para modelar enfermedades humanas —especialmente las causadas por deleciones recurrentes— mientras reduce el número de animales que deben criarse y seleccionarse. El resultado es una genética más precisa y reproducible y una vía más ética hacia modelos de enfermedad potentes.
Cita: Lkhagvadorj, K., Okamura, E., Taki, T. et al. Optimizing CRISPR precision in mouse embryos via microhomology-mediated end joining-dominant targeting. Commun Biol 9, 371 (2026). https://doi.org/10.1038/s42003-026-09771-z
Palabras clave: CRISPR, modelos de ratón, edición del genoma, reparación del ADN, modelado de enfermedades