Clear Sky Science · es
La glicosilación como regulador dinámico de las vías de señalización innata RLR y cGAS-STING
Cómo las etiquetas de azúcar ayudan a las células a detectar virus
Nuestras células están en constante vigilancia frente a virus invasores, y gran parte de esta defensa depende de pequeñas etiquetas de azúcar unidas a las proteínas. Esta revisión explica cómo estas etiquetas azucaradas, conocidas como glicosilación, funcionan más como reguladores de intensidad que como simples interruptores de encendido/apagado para vías antivirales clave. Comprender este ajuste fino basado en azúcares podría abrir nuevas vías para mejorar vacunas, tratar infecciones virales e incluso aprovechar el sistema inmunitario contra el cáncer.
La alarma temprana de la célula
Cuando los virus entran en una célula, dejan tras de sí hebra(s) discernible(s) de ARN o ADN. Sistemas especializados de “alarma” patrullan el interior celular en busca de estos restos genéticos. Un sistema, llamado vía de receptores tipo RIG-I (RLR), detecta ARN viral. Otro, conocido como vía cGAS–STING, reconoce ADN que aparece en un lugar inapropiado dentro de la célula. Una vez activadas, ambas vías encienden cascadas químicas que culminan en la liberación de interferones de tipo I y moléculas inflamatorias: señales potentes que avisan a las células vecinas y movilizan las defensas inmunitarias. Dado que una respuesta excesiva o insuficiente puede ser peligrosa, la célula debe afinar cuidadosamente estas alarmas, y la glicosilación es una de las formas clave de hacerlo. 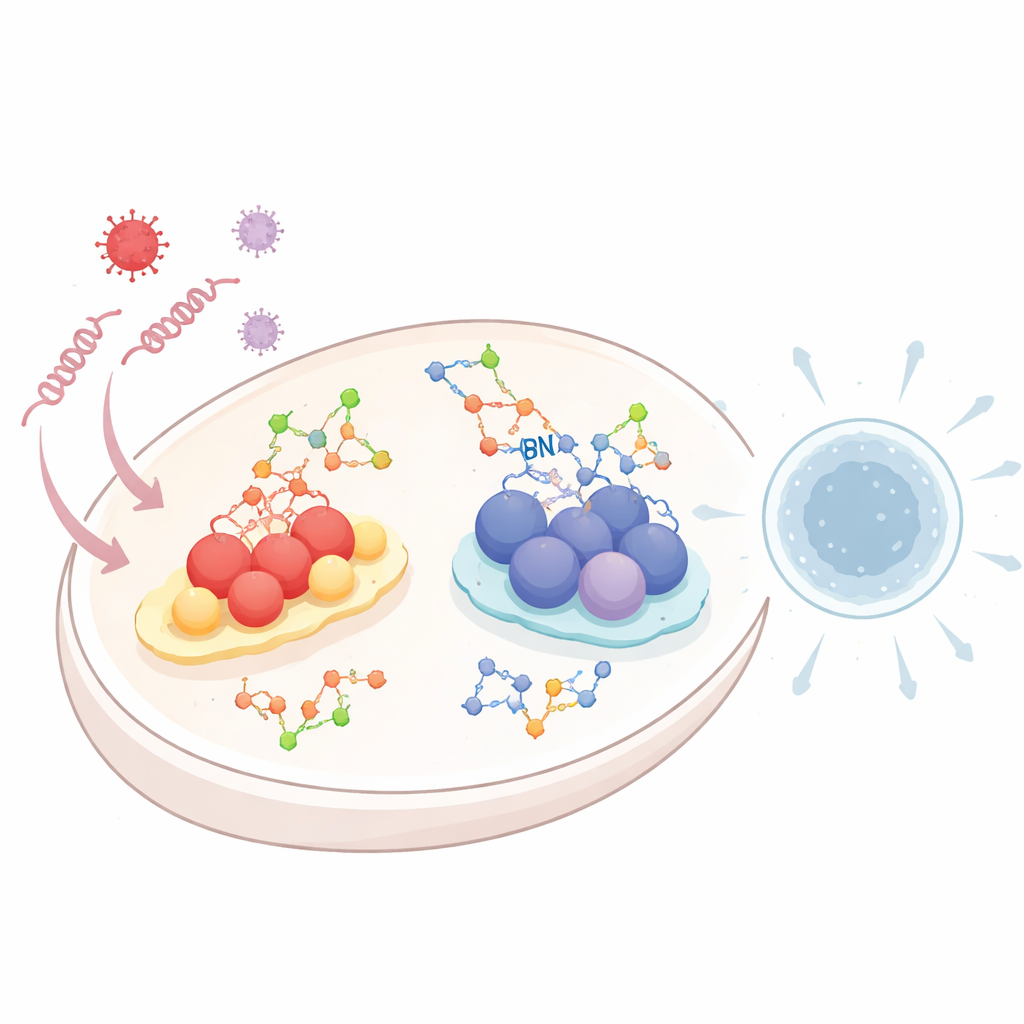
Las cubiertas de azúcar como controles de precisión
La glicosilación añade pequeñas unidades de azúcar a las proteínas en distintos compartimentos celulares. En la red de envío interna de la célula, el retículo endoplásmico y el aparato de Golgi, cadenas N-ligadas voluminosas ayudan a que las proteínas se plieguen correctamente, se mantengan estables y lleguen a la membrana adecuada. En contraste, una forma más ligera llamada O-GlcNAcilación coloca un único azúcar en proteínas del citoplasma y el núcleo. Esta etiqueta minimalista es altamente dinámica, renovándose rápidamente a medida que dos enzimas la añaden o la retiran en respuesta a los niveles de nutrientes y al estrés. La revisión describe cómo estos distintos tipos de azúcar no se limitan a encender o apagar los sensores inmunitarios; en su lugar, ajustan la facilidad con la que los sensores se aglutinan, su vida útil y la intensidad de su señalización. De este modo, la glicosilación vincula directamente el estado metabólico de la célula con su disposición para combatir infecciones.
Afinando la vía sensora de ARN
Dentro del sistema sensor de ARN RLR, una proteína de relevo central llamada MAVS se localiza en las mitocondrias y actúa como un núcleo clave. La revisión muestra que la O-GlcNAcilación en MAVS puede tanto acelerar como frenar la señalización antiviral, dependiendo de dónde se adhiera el azúcar. Las etiquetas azucaradas en determinados sitios favorecen otras modificaciones proteicas, como un tipo específico de cadena de ubiquitina, que ayudan a que MAVS forme grandes cúmulos de señalización y promueva una fuerte producción de interferón frente a virus de ARN. Otros sitios de glicosilación mantienen a MAVS disperso e inactivo en condiciones normales, evitando inflamación innecesaria. La infección viral y los cambios en la vía metabólica productora de azúcares de la célula pueden desplazar el equilibrio entre estas marcas activadoras e inhibidoras. Modificaciones relacionadas en otro factor, IRF5, pueden empujar al sistema inmune hacia tormentas de citocinas dañinas, lo que subraya que más azúcar no siempre es mejor. En paralelo, los virus pueden explotar azúcares N-ligados en proteínas de la superficie celular, como el receptor del factor de crecimiento EGFR, para marcar sensores aguas arriba como RIG-I para su degradación, debilitando así las defensas antivirales.
Afinando la vía sensora de ADN
La vía sensora de ADN cGAS–STING también está fuertemente modulada por la glicosilación. STING, una proteína de membrana en el retículo endoplásmico, necesita cadenas de azúcar N-ligadas para plegarse correctamente, mantenerse estable y ensamblarse en cúmulos de señalización una vez activada por mensajeros derivados del ADN. Sin estos azúcares, STING no logra formar las estructuras de orden superior ni traficar a través de los compartimentos celulares requeridos para una liberación robusta de interferón. Al mismo tiempo, la O-GlcNAcilación de STING en un sitio particular potencia un conjunto distinto de marcas químicas que favorecen su aglutinamiento y movimiento, amplificando las señales antivirales frente a virus de ADN. Cadenas azucaradas llamadas glicosaminoglicanos sulfatosas, construidas en el Golgi, ayudan además facilitando que STING activado se polymerice en estructuras largas que reclutan enzimas aguas abajo. Los virus contraatacan alterando sus propias glicoproteínas o desencadenando vías de degradación que tienen como blanco a STING, a menudo en los mismos espacios celulares donde estas decoraciones de azúcar se añaden o procesan. 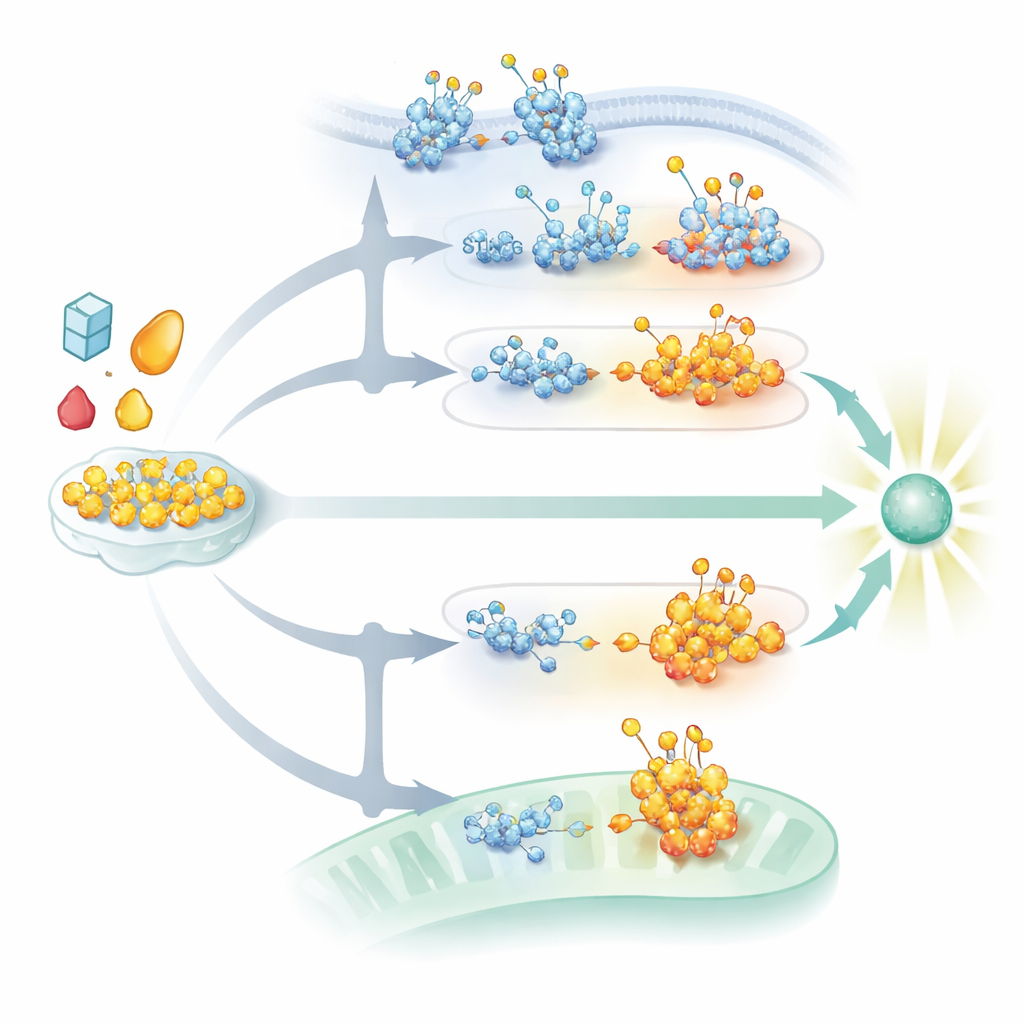
Metabolismo, enfermedad y terapias futuras
Dado que el donante principal de azúcar para la O-GlcNAcilación se produce por una vía metabólica conocida como la ruta biosintética de hexosaminas, los cambios en el uso de nutrientes afectan directamente a la señalización antiviral. Muchos virus activan esta vía para su beneficio, mientras que el aumento o bloqueo experimental del flujo de hexosaminas puede fortalecer o debilitar las respuestas antivirales en modelos animales. La revisión conecta estos mecanismos con la enfermedad humana: los tumores con frecuencia reorganizan la glicosilación para atenuar la señalización de interferón y escapar del ataque inmune, mientras que el estrés metabólico crónico o defectos heredados en el procesado de glicanos pueden inclinar la balanza hacia una autoinmunidad dañina. Los autores sostienen que las enzimas que controlan la glicosilación —especialmente las que añaden o eliminan O-GlcNAc o construyen estructuras N-ligadas clave— son dianas farmacológicas prometedoras pero complejas. Las terapias futuras probablemente deberán actuar de forma específica por sitio y consciente del contexto, orientando el “glicocódigo” hacia una mejor protección contra infecciones, cáncer y trastornos inflamatorios sin desencadenar nuevas formas de desequilibrio inmunitario.
La perspectiva general para la salud cotidiana
En términos cotidianos, este artículo revela que las alarmas antivirales de primera línea del organismo no actúan aisladamente: están conectadas al uso de energía y la química del azúcar de la célula. Pequeñas etiquetas de azúcar en un puñado de proteínas críticas deciden si un genoma viral errante provoca una advertencia mesurada, una defensa total o una reacción exagerada y peligrosa. Al descifrar y, eventualmente, aprender a ajustar este sistema de control basado en azúcares, los investigadores esperan diseñar tratamientos que mejoren la eficacia de las vacunas, ayuden a eliminar infecciones persistentes, desenmascaren tumores ante el sistema inmune y calmen la inflamación descontrolada en enfermedades autoinmunes.
Cita: Tong, J., Zhang, W., Xue, M. et al. Glycosylation as a dynamic regulator of RLR and cGAS-STING innate immune signalling pathways. Commun Biol 9, 422 (2026). https://doi.org/10.1038/s42003-026-09767-9
Palabras clave: inmunidad innata, glicosilación, vía RLR, cGAS-STING, O-GlcNAcilación