Clear Sky Science · es
Información estructural sobre la maquinaria de pili tipo IV de Thermus thermophilus que ensambla dos tipos distintos de pili
Pequeños pelos bacterianos con grandes funciones
Las bacterias pueden ser microscópicas, pero muchas disponen de notables “pelos” en su superficie que les permiten desplazarse, adherirse a sustratos e incluso captar ADN suelto del entorno. En este estudio, los investigadores analizan cómo una bacteria termófila, Thermus thermophilus, construye y pone en marcha una avanzada nano-máquina que empuja estos pelos —llamados pili— a través de su envoltura celular. Comprender esta maquinaria no solo revela cómo los microbios se adaptan y evolucionan, sino que también ofrece inspiración para la nanotecnología futura y nuevas formas de desactivar bacterias dañinas.
Dos pelos diferentes desde una misma máquina
Thermus thermophilus produce dos tipos distintos de pili: un filamento más ancho y grueso y otro más estrecho y delgado. Trabajos previos mostraron que estos filamentos están compuestos por bloques constructores distintos y probablemente cumplen funciones diferentes, como el movimiento sobre superficies o la captación de ADN. No obstante, ambos son ensamblados por la misma máquina multiparte que abarca desde la cara interna hasta la externa de la célula. La cuestión central de este estudio es cómo un solo sistema puede montar dos filamentos diferentes y empujarlos a través de las capas protectoras de la célula hacia el exterior.
Cartografiar el hardware oculto
Para descubrir cómo se compone la máquina, los investigadores emplearon tomografía crioelectrónica, una técnica que congela rápidamente las células y las imagen en 3D a muy bajas temperaturas. Combinaron estas instantáneas con modificaciones genéticas dirigidas que eliminaron o alteraron partes específicas de la máquina. Al comparar células normales con mutantes que carecían de ciertos componentes, pudieron identificar qué formas borrosas en sus mapas tridimensionales correspondían a qué proteínas. Luego usaron herramientas avanzadas de predicción estructural como planos moleculares, ayudando a encajar estos modelos proteicos en las densidades observadas y a ensamblar un modelo hipotético de la maquinaria en su longitud completa.
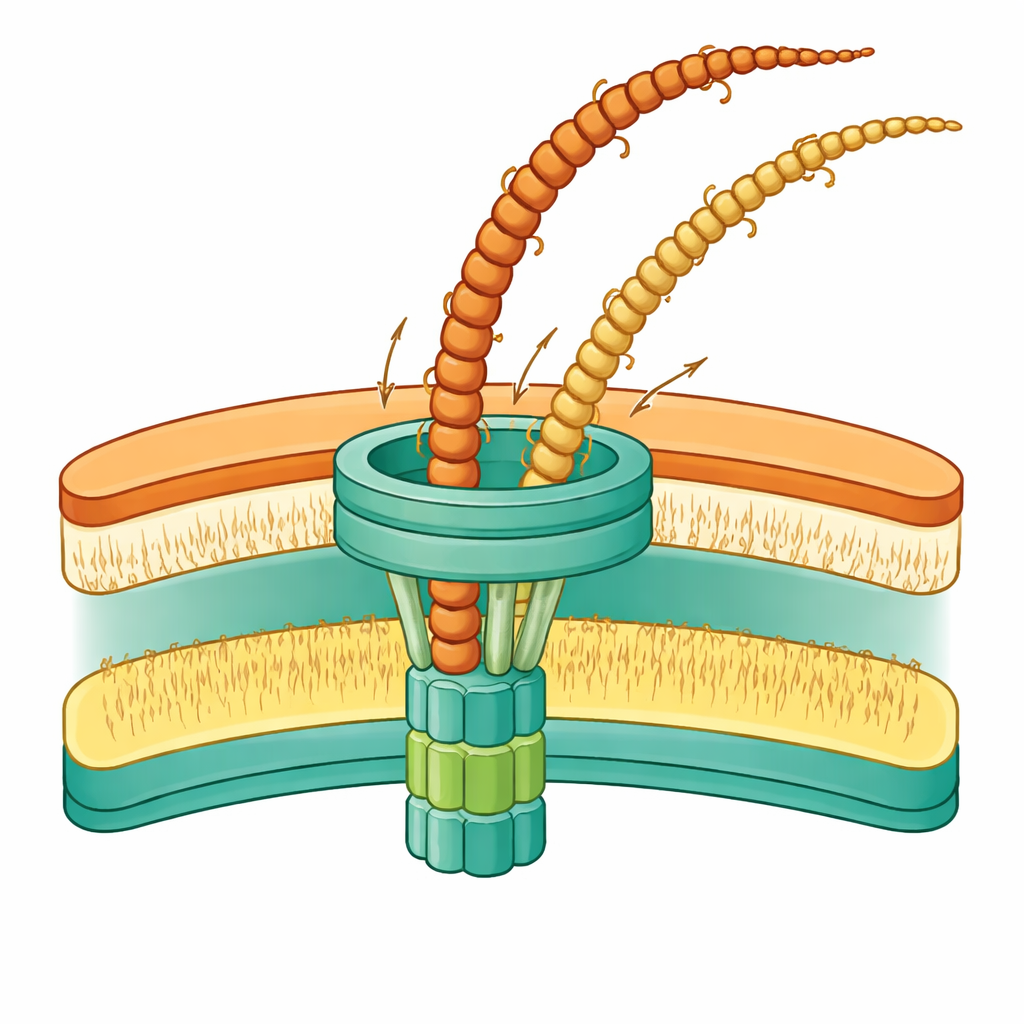
Un enlace flexible que mantiene todo unido
Un resultado destacado concierne a una proteína llamada PilW. Este componente se sitúa entre una compuerta de la membrana externa y una plataforma interna anclada en la membrana citoplasmática. Cuando PilW falta por completo, los pili no alcanzan el exterior y se amontonan en el espacio entre membranas. Cuando solo se recorta parte de PilW, la máquina aún funciona, pero sus componentes internos cambian de posición y las membranas circundantes se doblan hacia dentro. Estas observaciones sugieren que PilW actúa como una cuerda flexible que enlaza la compuerta externa con la plataforma interna, ajustando su longitud y forma a medida que la máquina alterna entre estados inactivos y activos. Los modelos del equipo indican que esta flexibilidad permite al sistema afrontar la brecha inusualmente amplia entre las dos membranas en Thermus, manteniendo al mismo tiempo el alineamiento suficiente de las piezas para ensamblar y expulsar los pili.
Observando los filamentos y sus recubrimientos azucarados
Paralelamente a la imagen intracelular, los investigadores aislaron también los dos tipos de pilis y los examinaron con mayor detalle mediante crio-microscopía electrónica de partícula única. Este enfoque de mayor resolución reveló la disposición precisa de los bloques constructores y, crucialmente, permitió al equipo modelar las moléculas de azúcar que decoran la superficie de los filamentos. El pilus más ancho porta tres sitios de unión de azúcares por cada subunidad, generando un halo denso de carbohidratos. El pilus más estrecho tiene sólo un sitio de este tipo, pero su cadena azucarada sobresale más, haciendo que el filamento en conjunto parezca mayor de lo que indicaría su núcleo proteico. Las simulaciones por ordenador exploraron después cómo estas azúcares se doblan y se mueven mientras el filamento atraviesa la compuerta de la membrana externa.
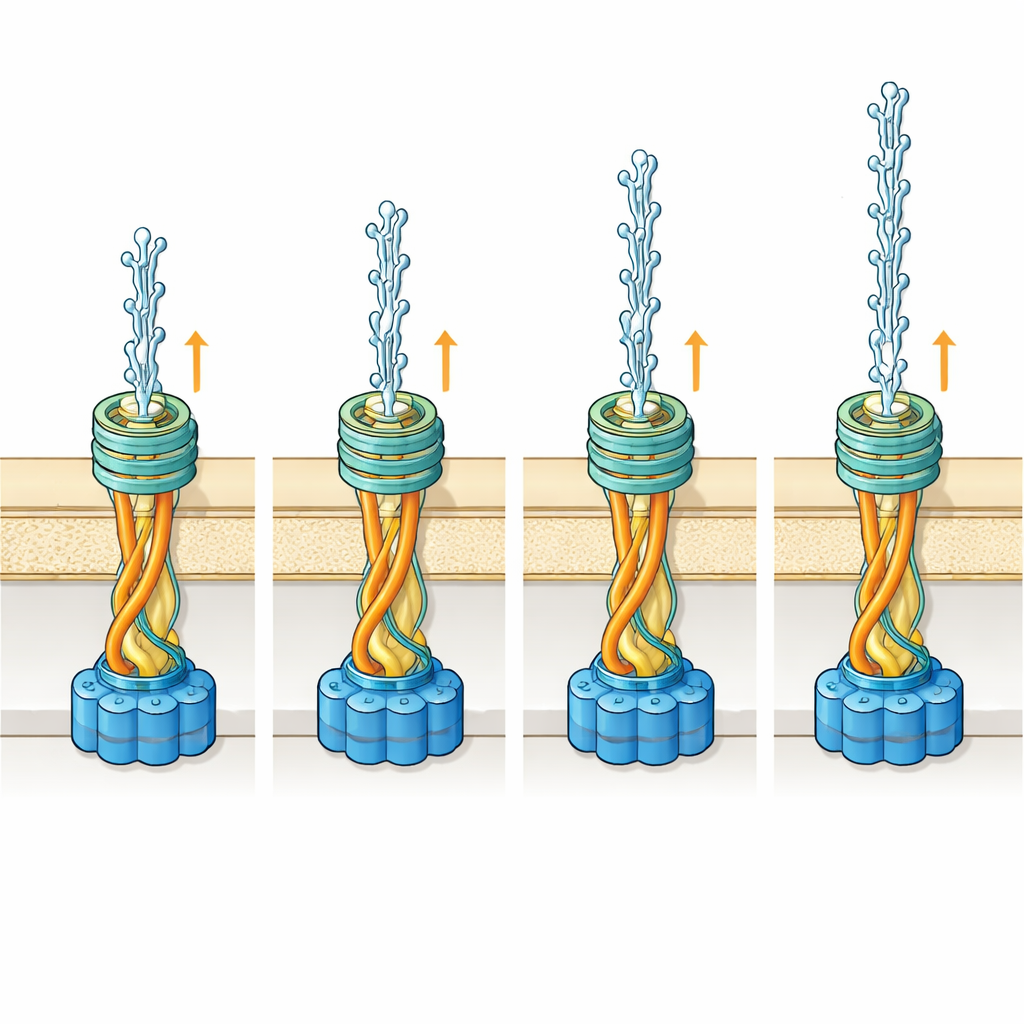
Una compuerta compartida para dos cables muy diferentes
Al acoplar sus estructuras detalladas de los pili en un modelo de la compuerta de la membrana externa, llamada PilQ, el equipo encontró que, en principio, ambos tipos de filamento pueden deslizarse por la misma apertura. Para el filamento más ancho, sus múltiples azúcares tienen suficiente espacio para adoptar muchas conformaciones mientras atraviesan la compuerta. Para el filamento más estrecho, en un punto del canal el espacio se vuelve limitado, por lo que algunas conformaciones azucaradas chocarían con las paredes. Las simulaciones sugieren que en este caso la cadena de azúcar probablemente se ajusta más al filamento mientras está dentro de la compuerta y sólo se despliega una vez fuera de la célula. En lugar de evolucionar una compuerta más grande y costosa para acomodar cómodamente ambos filamentos, la bacteria parece confiar en la flexibilidad natural de estas cadenas azucaradas para que el sistema funcione de manera eficiente.
Qué significa esto para la vida microbiana
En conjunto, el estudio dibuja un panorama coherente de cómo una sola máquina adaptable monta y exporta dos pili muy distintos en una bacteria de fuentes termales. Una proteína enlazadora flexible parece mantener alineadas las partes internas y externas mientras el motor cicla y la estructura se acorta ligeramente durante el crecimiento activo del filamento. Al mismo tiempo, los recubrimientos azucarados de los pili les proporcionan protección y alcance, siendo suficientemente flexibles para comprimirse a través de un conducto de salida relativamente estrecho. Para los no especialistas, el mensaje clave es que incluso microbios aparentemente simples dependen de ensamblajes móviles y altamente coordinados para sobrevivir y evolucionar: dispositivos moleculares cuya elegancia y eficiencia compiten e incluso superan, en ocasiones, a las máquinas humanas a escala nanométrica.
Cita: Neuhaus, A., McLaren, M., Isupov, M.N. et al. Structural insights into the Thermus thermophilus type IV pilus machinery assembling two distinct pili. Commun Biol 9, 474 (2026). https://doi.org/10.1038/s42003-026-09762-0
Palabras clave: pili tipo IV, nanomáquinas bacterianas, crio-microscopía electrónica, glicosilación de proteínas, Thermus thermophilus