Clear Sky Science · es
Modelado impulsado por la tasa de crecimiento sugiere que la adaptación fenotípica impulsa la resistencia a fármacos en melanomas con la mutación BRAFV600E
Células cancerosas que aprenden a convivir con los fármacos
Los fármacos dirigidos han transformado el tratamiento de muchas personas con melanoma, un cáncer de piel grave. Sin embargo, estos medicamentos casi siempre dejan de funcionar: tumores que antes se encogían vuelven a crecer. Este estudio plantea una pregunta simple pero potente: en lugar de apoyarse únicamente en mutaciones genéticas, ¿pueden las células de melanoma “aprender” a sobrevivir al tratamiento cambiando su comportamiento, y podría este aprendizaje explicar por qué algunas formas de administrar fármacos funcionan mejor que otras?
De células sensibles a sobrevivientes
Los investigadores se centraron en células de melanoma que portan una alteración común en un gen llamado BRAF, lo que las hace especialmente sensibles a un tipo de fármaco conocido como inhibidor de BRAF. En experimentos de laboratorio previos, estas células se expusieron al fármaco encorafenib a distintas dosis y durante distintos periodos. Midiendo con precisión la velocidad con la que las células crecían o morían en cada condición, los autores dividieron las células en dos categorías amplias: células no tratadas que nunca habían visto el fármaco, y células adaptadas al fármaco que habían vivido en su presencia al menos una semana. Las células no tratadas crecían bien sin tratamiento pero se ralentizaban mucho o morían con el fármaco. Las células adaptadas, en cambio, crecían mejor en presencia del fármaco pero perdían esa ventaja cuando se retiraba el fármaco, lo que sugiere que su supervivencia estaba ligada a un cambio de estado flexible y reversible más que a un daño genético permanente.
Un mapa de comportamientos celulares ocultos
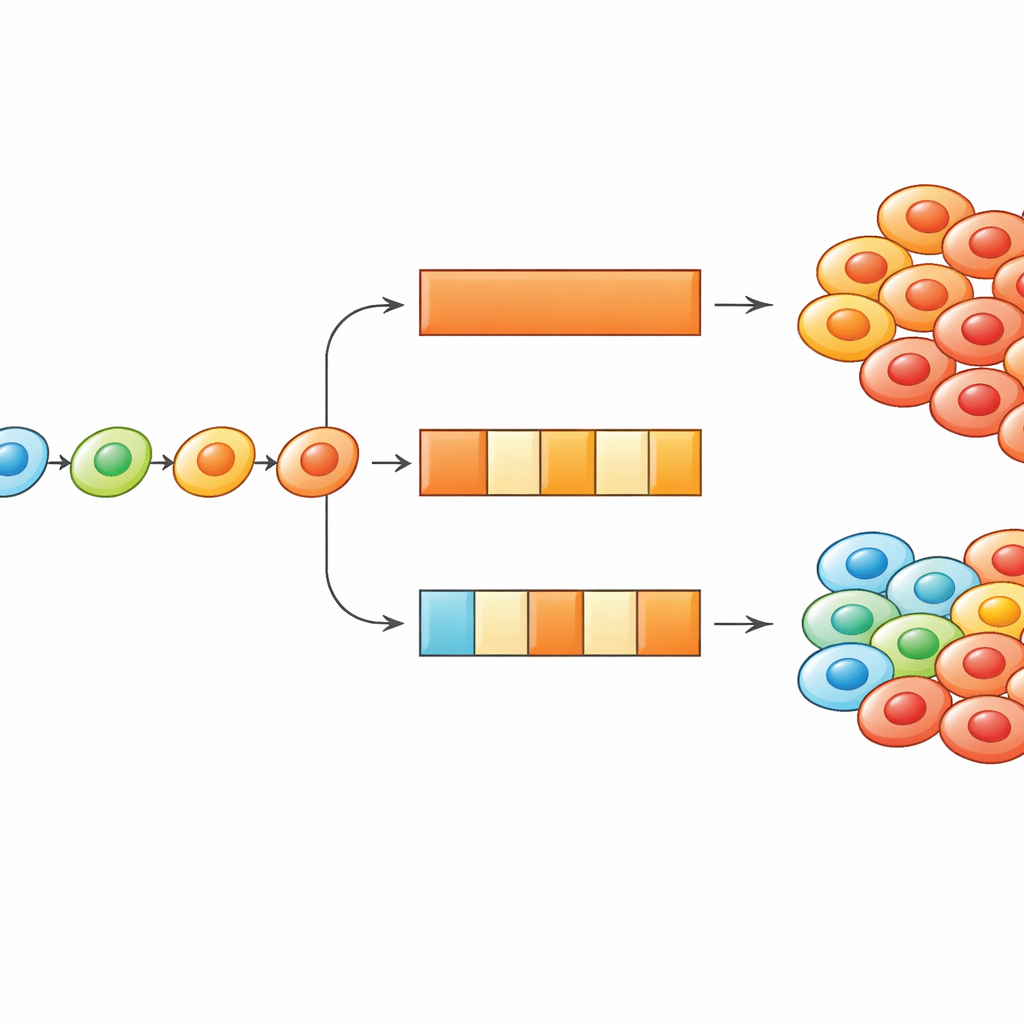
Para entender estos cambios, el equipo construyó un modelo matemático en el que a cada célula cancerosa se le asigna un “estado fenotípico”: una posición abstracta en una escala desde muy sensible al fármaco hasta muy resistente. En lugar de asumir solo dos tipos de células, permitieron muchos estados intermedios, reflejando cambios graduales en marcadores biológicos de resistencia. Para cada combinación de estado y dosis de fármaco estimaron una tasa neta de crecimiento, que podía ser positiva (más divisiones que muertes) o negativa (más muertes que divisiones). Todas estas tasas se organizaron en una cuadrícula, o “matriz de aptitud”, que actúa como un paisaje: algunos estados a ciertas dosis son buenos lugares para prosperar, otros son letales. En el modelo, las células pueden moverse paso a paso a través de ese paisaje conforme el tratamiento se enciende o se apaga.
¿Las células derivan o escalan hacia la ventaja?
La incógnita clave era cómo se mueven las células por ese paisaje. Los autores probaron cuatro estrategias posibles. En una, las células no cambian nunca de estado, de modo que cualquier célula resistente debe estar presente desde el inicio. En otra, las células deambulan aleatoriamente entre estados vecinos, como una marcha errática, sin importar si su situación mejora. En las dos estrategias restantes, las células tienden a moverse hacia estados donde su tasa de crecimiento es mayor—ya sea de forma ruidosa, con algunos traspiés, o de forma fuerte, siempre escalando hacia una mejor supervivencia. Cuando el equipo ejecutó simulaciones por ordenador y las comparó con datos de laboratorio reales, especialmente experimentos en los que el fármaco se administró de forma continua o en un patrón intermitente (una semana con fármaco, una semana sin), solo las estrategias en las que las células escalan hacia una mayor aptitud pudieron reproducir lo observado: el tratamiento intermitente a alta dosis suprimió mejor el número de células que el tratamiento continuo con el mismo tiempo total y una cantidad global mayor de fármaco.
Usar dosis on–off para convertir la adaptación en contra del cáncer
Profundizando, los investigadores usaron tanto simulaciones como ecuaciones más simples para explorar con qué frecuencia se permite a las células cambiar de estado y cuánto duran los periodos con y sin fármaco. Encontraron que cuando las células se adaptan de forma dirigida, los horarios de tratamiento se pueden ajustar para frenar o explotar esta adaptación. Acortar la frecuencia con la que las células pueden actualizar su estado—conceptualmente, ralentizar los mecanismos biológicos que permiten el cambio fenotípico—tiende a hacer que los tratamientos intermitentes sean más potentes, porque las células no pueden escalar tan rápido hacia estados altamente resistentes. Por el contrario, si las células comienzan en un estado fuertemente resistente, las pausas en el fármaco pueden darles tiempo para volver hacia estados más sensibles, de modo que reintroducir el fármaco provoque una oleada de muerte celular. El estudio muestra cómo el ritmo de dosificación y la velocidad de adaptación celular conjuntamente determinan qué pauta funciona mejor.
Qué significa esto para la atención del cáncer en el futuro
Para un público general, el mensaje central es que las células cancerosas no son enemigos inmutables; son cambiantes. En este sistema de melanoma, las células parecen moverse activamente hacia comportamientos que les permiten crecer bajo las condiciones que enfrentan. El modelo de los autores sugiere que esta adaptación dirigida por sí sola—sin invocar distintos linajes clonales permanentes—puede explicar por qué los esquemas on–off a veces superan a la dosificación constante, incluso cuando usan menos fármaco en conjunto. Aunque estos resultados provienen de células cultivadas en laboratorio y requieren más trabajo antes de guiar la atención en pacientes, el enfoque ofrece un marco práctico: midiendo qué tan rápido y en qué dirección se adaptan las células cancerosas, los médicos podrían diseñar eventualmente programas de tratamiento que no solo ataquen a los tumores sino que también encaminen su “aprendizaje” fenotípico hacia callejones sin salida en lugar de rutas de escape.
Cita: Hamis, S., Browning, A.P., Jenner, A.L. et al. Growth rate-driven modelling suggests that phenotypic adaptation drives drug resistance in BRAFV600E-mutant melanoma. Commun Biol 9, 385 (2026). https://doi.org/10.1038/s42003-026-09760-2
Palabras clave: melanoma, resistencia a fármacos, plasticidad celular, terapia intermitente, modelado matemático