Clear Sky Science · es
Base estructural de la activación por dimerización de la quinol-dependiente reductasa de óxido nítrico de Neisseria meningitidis
Cómo las bacterias burlan nuestra defensa inmunitaria
Cuando bacterias nocivas invaden el organismo, nuestras células inmunitarias liberan moléculas tóxicas como el óxido nítrico para eliminarlas. Sin embargo, algunos patógenos han desarrollado trucos moleculares para neutralizar este ataque y sobrevivir. Este estudio revela, con detalle atómico, cómo una enzima bacteriana clave se reconfigura en pares para volverse mucho mejor en la desintoxicación del óxido nítrico, y por qué entender este comportamiento de cambio de forma podría abrir nuevas vías para el diseño de antibióticos.
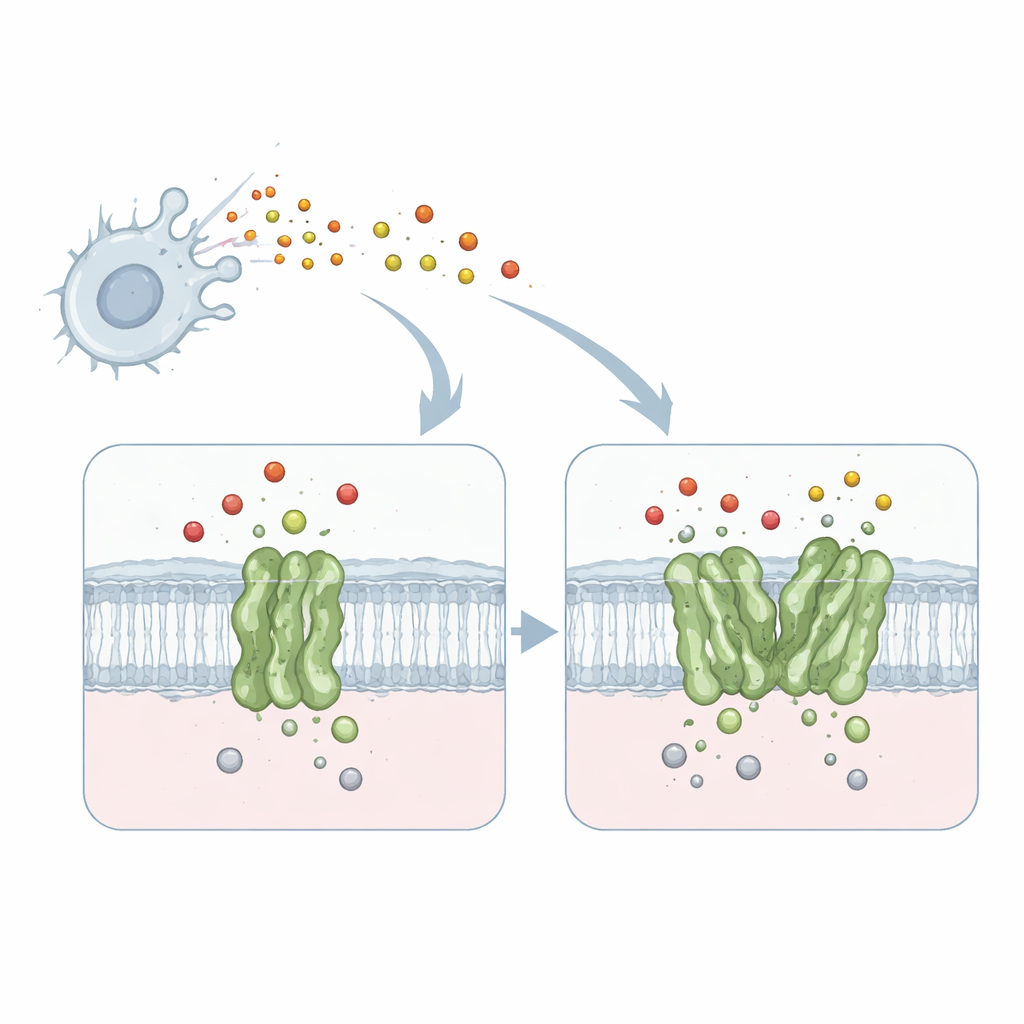
Una máquina diminuta que desarma un gas tóxico
El trabajo se centra en una proteína de membrana denominada reductasa de óxido nítrico dependiente de quinol, o qNOR, de la bacteria causante de la meningitis Neisseria meningitidis. qNOR se ubica en la membrana celular bacteriana y convierte el óxido nítrico —un gas tóxico producido por nuestro sistema inmune— en productos menos dañinos. Esta desintoxicación permite al microbio seguir respirando y creciendo incluso dentro de ambientes hostiles como los macrófagos humanos. Dado que la respiración y la eliminación de óxido nítrico son vitales para la supervivencia del patógeno, qNOR constituye una diana atractiva para nuevos fármacos antimicrobianos.
Cuando uno está bien pero dos son mejores
Estudios bioquímicos previos mostraron que qNOR puede existir ya sea como una unidad única (monómero) o como un par (dímero), y que el dímero actúa de dos a cuatro veces más rápido en neutralizar el óxido nítrico. Hasta ahora no estaba claro por qué el simple emparejamiento de dos copias de la misma enzima tenía un impacto tan drástico en su rendimiento. Para responder a esto, los investigadores usaron crio-microscopía electrónica de partículas individuales a alta resolución para capturar estructuras tridimensionales detalladas tanto del qNOR monomérico como del dimérico de la misma cepa bacteriana. Obtuvieron vistas casi a resolución atómica —1,89 angstroms para el dímero y 2,25 angstroms para el monómero— lo bastante nítidas como para localizar cadenas laterales de aminoácidos individuales, iones metálicos y muchas moléculas de agua.
Una hélice flexible que se convierte en un puntal estabilizador
Sorprendentemente, el corazón catalítico de la enzima —el centro metálico donde se convierte el óxido nítrico— se veía casi idéntico en ambas formas. En cambio, las diferencias clave aparecían a cierta distancia, en una hélice transmembrana llamada TM10 y en cómo esta contacta con otra hélice (TM2) cuando dos moléculas de qNOR se emparejan. En el monómero, TM10 está débilmente anclada y puede oscilar y doblarse de manera considerable, como reveló el análisis computacional de los datos de crio-EM. En el dímero, TM10 de cada pareja se bloquea contra su vecina para formar un paquete de cuatro hélices, restringiendo mucho su movimiento. Esta estabilización reposiciona sutilmente un aminoácido crucial, un glutamato llamado Glu563, acercándolo a otro glutamato (Glu494) próximo al sitio activo y configurando una vía más enfocada para los protones entrantes necesarios para la reacción.
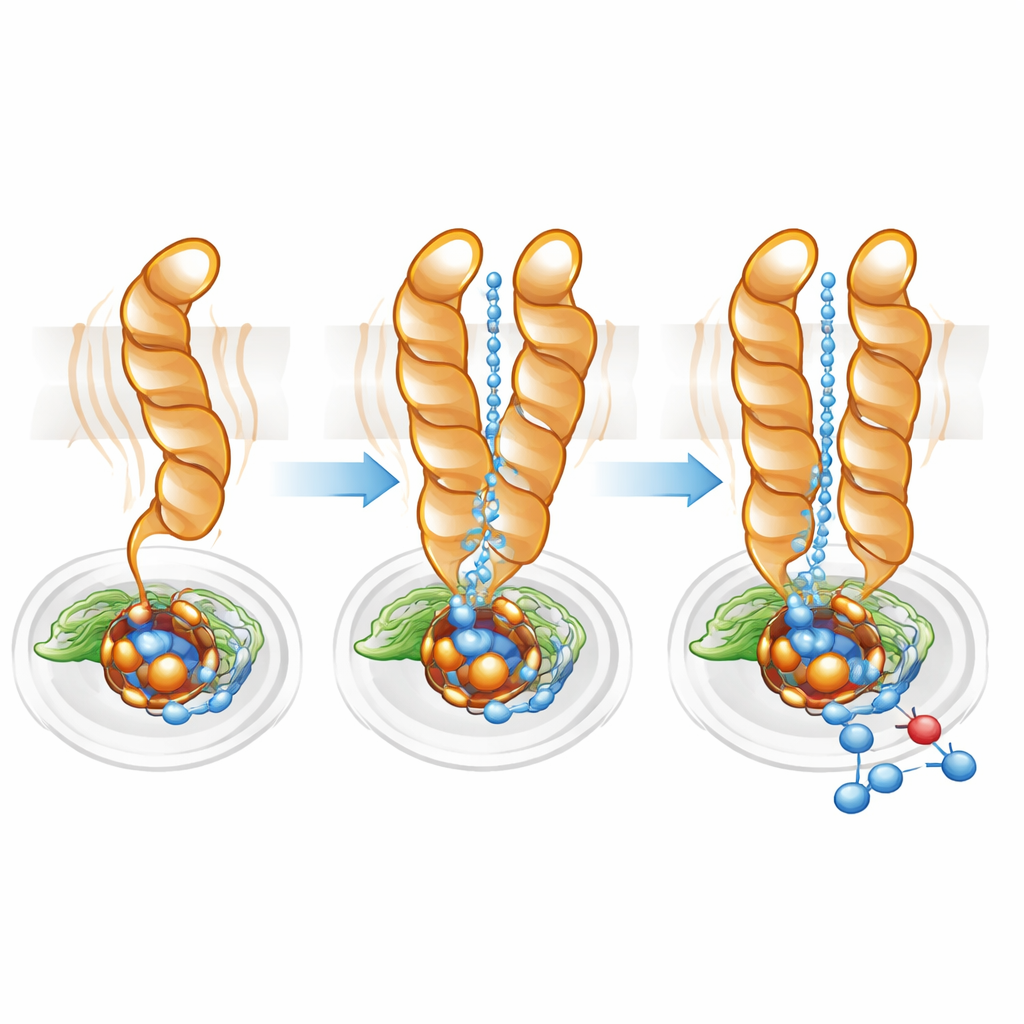
Afinando la autopista de protones
Los protones —iones de hidrógeno con carga positiva— deben ser entregados eficientemente desde el interior celular hasta el sitio activo enterrado para que la reducción del óxido nítrico pueda proceder. Utilizando software de mapeo de rutas, el equipo encontró una cavidad hidrofílica que conecta el citoplasma con el sitio activo tanto en monómero como en dímero. Sin embargo, en el monómero este canal era más ancho y difuso, coherente con la mayor movilidad de TM10. En el dímero, la posición bloqueada de TM10 y la orientación favorable de Glu563 ayudaron a definir una vía más directa y mejor organizada. La mutación de Glu563 por aminoácidos que no pueden formar las mismas interacciones redujo la actividad de la enzima a menos del 10% de la normal y también desestabilizó el dímero, mientras que mutaciones en posiciones relacionadas disminuyeron la cantidad de hierro no hemo esencial en el sitio activo. En conjunto, estos resultados muestran que la formación del dímero y la precisa colocación de Glu563 y Glu494 están fuertemente vinculadas tanto a la integridad estructural como a la eficiencia catalítica.
Convertir los conocimientos estructurales en nuevos tratamientos
Los hallazgos revelan una línea clara desde el emparejamiento de proteínas en la superficie de la membrana hasta ajustes finos en lo profundo del sitio activo que controlan con qué eficacia qNOR elimina el óxido nítrico. En términos sencillos, cuando dos copias de la enzima se abrazan, enderezan y rigidizan un segmento flexible que ayuda a encauzar protones hacia el centro de reacción, aumentando la productividad de la enzima. Para el desarrollo de fármacos, esto sugiere una estrategia no convencional: en lugar de bloquear directamente el sitio activo, se podrían diseñar moléculas que separen el dímero o que interrumpan la interacción Glu563–Glu494, forzando a la enzima a su lento estado monomérico. Dado que qNOR y enzimas relacionadas son cruciales para la supervivencia de varios patógenos peligrosos y resistentes a fármacos, tales enfoques guiados por la estructura podrían contribuir a la próxima generación de antimicrobianos dirigidos.
Cita: Gopalasingam, C.C., Egami, H., Shigematsu, H. et al. Structural basis of Neisseria meningitidis quinol dependent nitric oxide reductase activation by dimerization. Commun Biol 9, 433 (2026). https://doi.org/10.1038/s42003-026-09754-0
Palabras clave: desintoxicación de óxido nítrico, respiración bacteriana, enzimas de membrana, crio-microscopía electrónica, dianas para fármacos antimicrobianos