Clear Sky Science · es
La multiómica espacial revela características inmunometabólicas inducidas por electroporación irreversible en el margen inflamatorio del cáncer de hígado
Por qué hace falta examinar más de cerca un nuevo tratamiento para el cáncer de hígado
La electroporación irreversible (IRE) es una técnica relativamente nueva para destruir tumores hepáticos que utiliza pulsos eléctricos breves y de alto voltaje en lugar de calor. Dado que puede preservar los vasos sanguíneos y los conductos biliares cercanos, resulta especialmente útil para tumores en localizaciones delicadas. Sin embargo, hasta un tercio de los pacientes sigue presentando recidiva tumoral justo al lado del área tratada. Este estudio pregunta qué ocurre en esa estrecha región limítrofe después de la IRE y si cambios ocultos en las células inmunitarias y el metabolismo celular en ese lugar podrían preparar en silencio el terreno para la reaparición del cáncer.
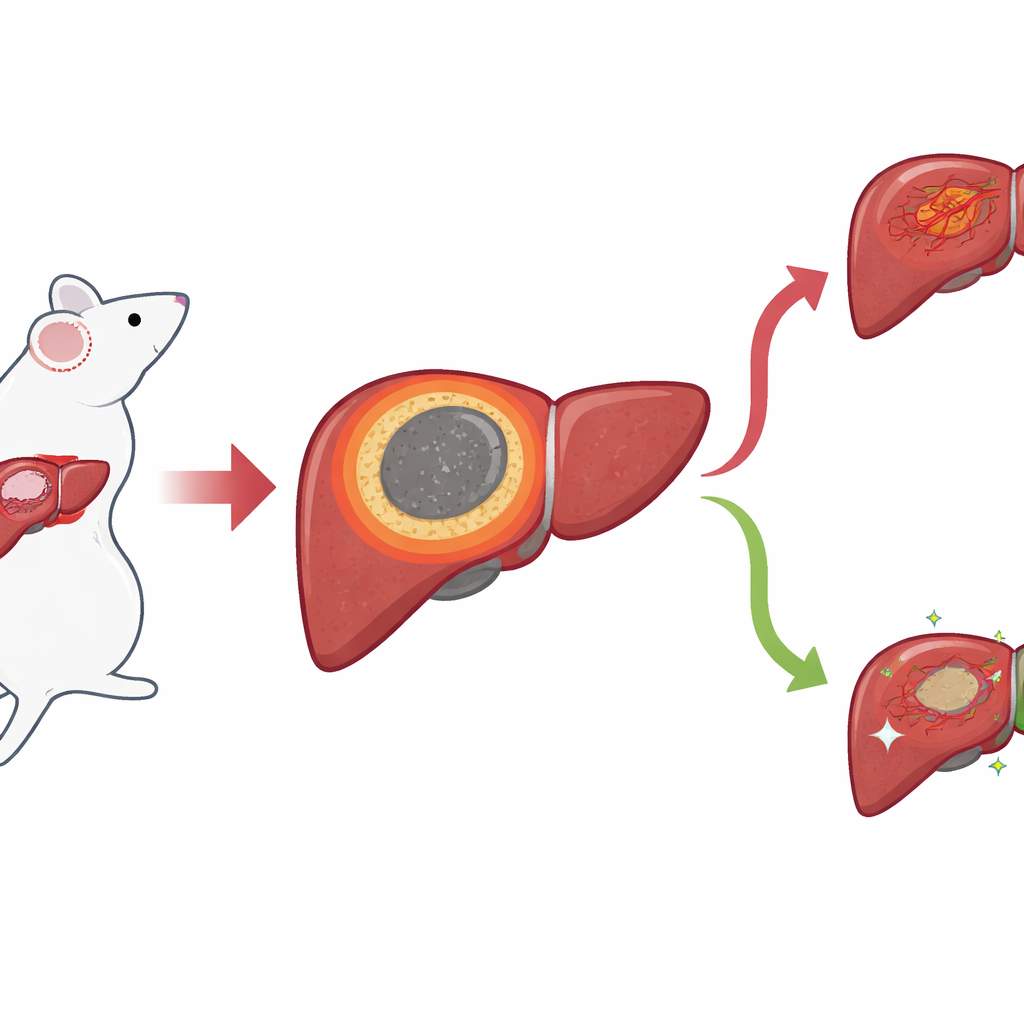
Un borde estrecho con grandes consecuencias
Utilizando un modelo murino de cáncer de hígado, los investigadores se centraron en el delgado anillo de tejido que se forma entre el núcleo necrótico ablacionado y el hígado sano circundante tras la IRE. Lo denominan margen inflamatorio, o IM. Las imágenes microscópicas estándar mostraron que esta zona coincide exactamente con los lugares donde suelen aparecer las recidivas locales, pero sus límites eran difíciles de definir a simple vista. Para obtener una imagen más nítida, el equipo aplicó métodos “espaciales” que detectan qué genes y pequeñas moléculas están presentes preservando su ubicación en el tejido. Con transcriptómica espacial, mapearon la actividad génica punto por punto y descubrieron un grupo distintivo de puntos que se alineaban precisamente con el IM, separando el centro necrótico del hígado y las zonas tumorales normales.
Las células inmunitarias se concentran, pero muchas frenan el ataque
Los científicos emplearon luego secuenciación de ARN unicelular y de un solo núcleo, junto con un potente método de perfilado llamado CyTOF, para catalogar los tipos celulares individuales a lo largo del hígado. Encontraron que el IM está dominado por un tipo de célula inmunitaria llamadas macrófagos. En particular, un subconjunto parecido a los “macrófagos asociados a lípidos” (LAMs) inundó el IM en cuestión de días tras la IRE. Estas células presentan marcadores de superficie y firmas génicas vinculadas a la supresión inmunitaria, incluidos niveles elevados de PD-L1, una molécula conocida por disminuir las respuestas de las células T. Los análisis de expresión génica sugirieron que estos macrófagos son hábiles en fagocitar material, responder a señales químicas atrayentes y emitir señales que pueden frenar a las propias células T necesarias para eliminar las células tumorales. La visualización confirmó que los macrófagos PD-L1 positivos eran mucho más abundantes en el IM que en el tejido normal cercano.
Un punto caliente de química lipídica alterada
A continuación, el equipo superpuso este paisaje inmunitario con metabolómica espacial, un enfoque de imagen por espectrometría de masas que mapea la distribución de cientos de pequeñas moléculas. Mostraron que el IM posee una huella metabólica distinta, diferente tanto del núcleo necrótico como del hígado circundante. En esta banda estrecha, muchas rutas lipídicas estaban fuertemente aumentadas, incluida la producción de ácidos grasos insaturados, derivados del ácido araquidónico y esfingolípidos. Lípidos señalizadores clave, como prostaglandinas y leucotrienos derivados del ácido araquidónico, se enriquecieron en el IM, mientras que otras vías enzimáticas para procesar la misma molécula estaban relativamente atenuadas. Otra familia lipídica, los esfingolípidos —incluidos ceramidas y esfingomielinas— también se acumularon, respaldada por una mayor expresión de las enzimas que los sintetizan y remodelan.
Un cambio gradual de daño a un nicho rico en combustible
Al subdividir el margen inflamatorio en tres capas delgadas desde el núcleo necrótico hacia afuera, los investigadores observaron un desplazamiento gradual en la química. Más cerca de la zona necrótica, los lípidos complejos y las moléculas relacionadas con el colesterol eran más abundantes, mientras que más hacia el exterior aumentaban pequeñas moléculas energéticas como la glucosa y ciertos aminoácidos. Este patrón sugiere que, en una corta distancia, el tejido transita de un entorno cargado de lípidos y rico en señales a otro orientado a alimentar la supervivencia y el crecimiento celular. Los autores proponen que esta reprogramación escalonada ayuda a sostener a los macrófagos inmunosupresores ávidos de lípidos que dominan el IM y que podrían preparar en silencio el terreno para que las células tumorales se reestablezcan.
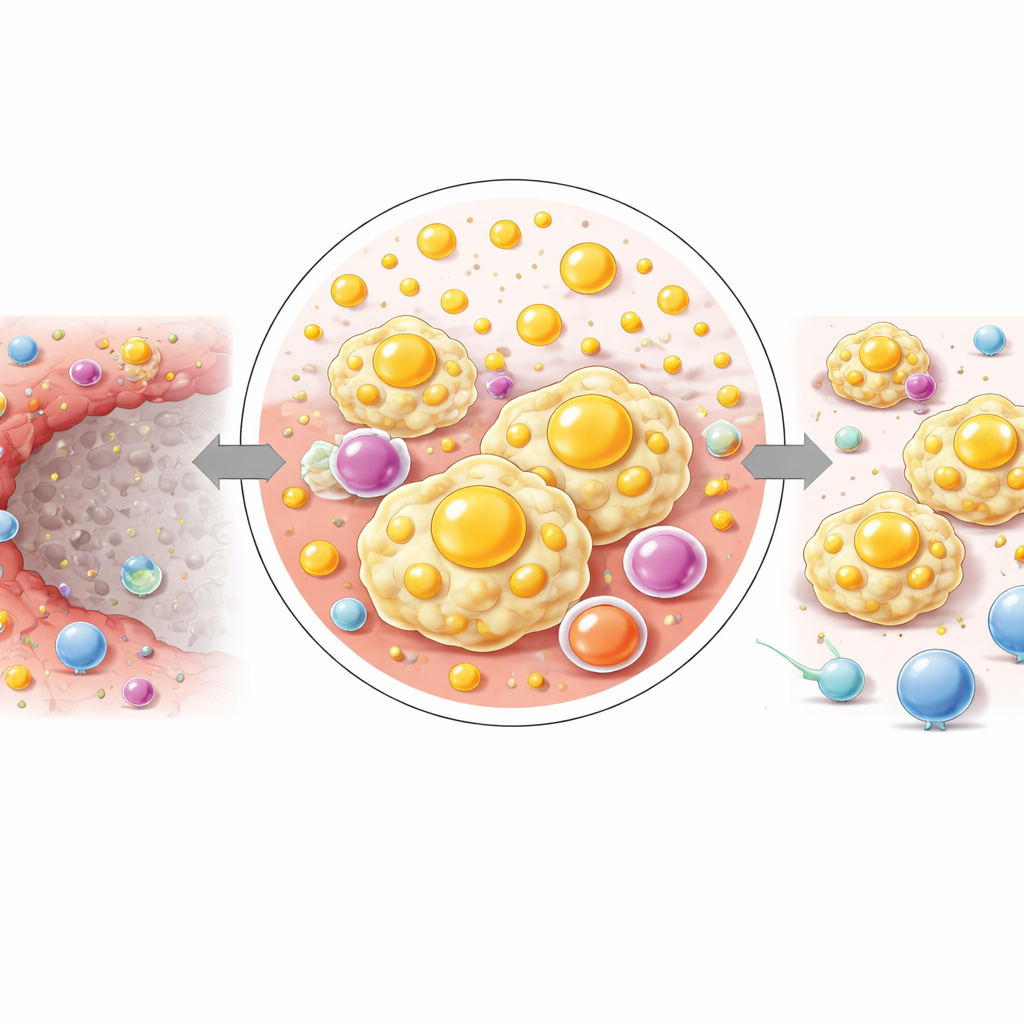
Qué significa esto para la atención futura del cáncer de hígado
En términos sencillos, este trabajo muestra que la IRE hace más que matar células tumorales: también crea un anillo estrecho de tejido donde las células inmunitarias y la química lipídica construyen juntos un vecindario protegido y favorable al tumor. Los macrófagos en esta zona son abundantes, están cargados de lípidos y orientados a desactivar las células T en lugar de ayudarles. Dado que estos cambios están estrechamente ligados a vías metabólicas específicas, sugieren nuevas estrategias terapéuticas. Combinar la IRE con fármacos que apunten al metabolismo de lípidos o que bloqueen PD-L1 en este margen podría, en principio, transformar un borde propenso a recaídas en una zona que realmente complete la eliminación del cáncer de hígado.
Cita: Liu, J., Guan, S., Sun, Z. et al. Spatial multiomics reveals irreversible electroporation-induced immuno-metabolic characteristics of the inflammatory margin in liver cancer. Commun Biol 9, 458 (2026). https://doi.org/10.1038/s42003-026-09742-4
Palabras clave: cáncer de hígado, ablación tumoral, microambiente inmunitario, macrófagos, metabolismo de lípidos