Clear Sky Science · es
La decoración superficial de bacterias genera terapias vivas robustas para mejorar el tratamiento de la colitis ulcerosa
Convertir microbios amistosos en pequeños guardianes
La colitis ulcerosa es una enfermedad intestinal dolorosa en la que el propio intestino del cuerpo se vuelve crónicamente inflamado, causando diarrea urgente, sangrado y una calidad de vida muy reducida. Médicos y pacientes muestran interés en pastillas de “bacterias beneficiosas” que podrían calmar esta inflamación desde dentro, pero la mayoría de estos microbios mueren en el duro recorrido por el estómago y el intestino delgado antes de llegar al colon, donde se necesitan. Este estudio describe una nueva forma de vestir a las bacterias probióticas con una armadura protectora para que puedan atravesar el tracto digestivo con seguridad, asentarse en el colon y ayudar a reparar el intestino dañado.
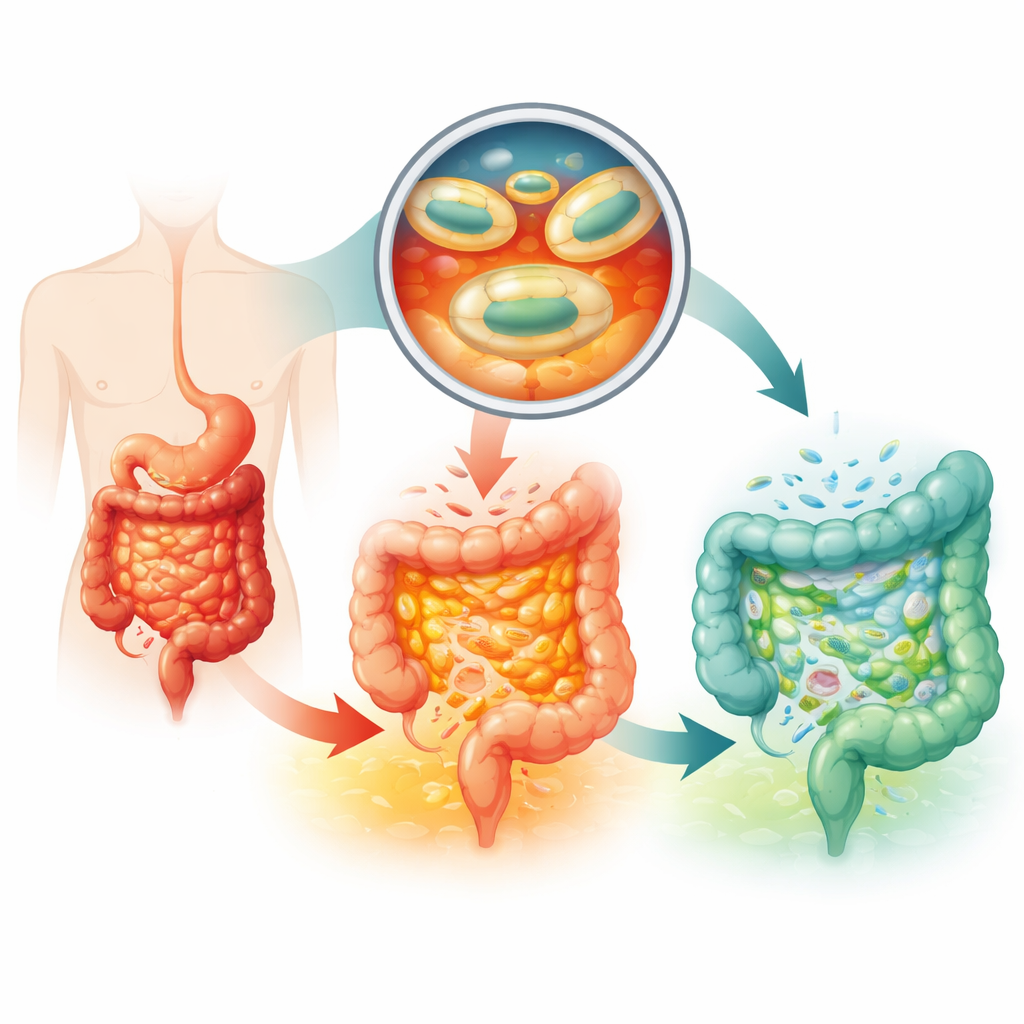
Por qué las pastillas probióticas actuales a menudo no son suficientes
Los tratamientos estándar para la colitis ulcerosa se basan en fármacos antiinflamatorios e inmunosupresores que pueden tener efectos secundarios graves y no funcionan para todos. Los probióticos ofrecen un enfoque más suave al ayudar a reequilibrar la comunidad microbiana intestinal. Una cepa especial de Escherichia coli llamada Nissle 1917 ya está aprobada como medicamento para esta enfermedad, pero los pacientes deben ingerir dosis extremadamente altas cada día y aun así los beneficios son modestos. El problema clave es la supervivencia y la entrega: el ácido del estómago, las enzimas digestivas y el tránsito rápido por los intestinos superiores matan o arrastran la mayoría de las bacterias antes de que puedan adherirse y crecer en el colon, donde normalmente reside más del 99 % de los microbios intestinales.
Construir una cáscara protectora alrededor de bacterias útiles
Para resolver esto, los investigadores crearon un recubrimiento fino e inteligente alrededor de cada célula probiótica utilizando un material derivado de plantas llamado lignina. Modificaron químicamente la lignina para hacerla más soluble y sensible a los cambios de acidez, obteniendo una sustancia que permanece estable en ácidos fuertes pero se descompone en el ambiente más neutro del colon. Mediante un proceso suave capa a capa, primero añadieron iones de calcio a la superficie probiótica y luego la envolvieron con la lignina modificada, formando una “armadura” lisa de aproximadamente una diezmilésima de milímetro de espesor. La microscopía y las mediciones de tamaño de partículas mostraron que este blindaje protegía a las bacterias sin matarlas, y el mismo método funcionó en varias especies bacterianas muy distintas, lo que sugiere que podría servir como una plataforma general para muchas terapias probióticas.
Dirigirse al colon y ayudar a su reparación
Cuando se probaron en fluidos digestivos simulados, las bacterias sin protección fueron destruidas rápidamente por el ácido gástrico, mientras que las bacterias blindadas permanecieron vivas durante horas y solo liberaron su contenido de manera eficiente a niveles de pH similares a los del colon. En ratones con colitis ulcerosa inducida químicamente, las bacterias recubiertas se acumularon fuertemente en el colon, mientras que las bacterias sin recubrimiento o las mezclas simples con el material de recubrimiento en gran medida no lo hicieron. El equipo usó imágenes fluorescentes, pruebas genéticas y modelado matemático para mostrar que las bacterias protegidas no solo llegaron al colon íntegras, sino que también se multiplicaron allí, alcanzando aproximadamente una de cada mil de todos los microbios intestinales. Los ratones tratados perdieron menos peso, mantuvieron el colon más largo y presentaron un tejido intestinal mucho más sano al microscopio, con uniones celulares más estrechas y una capa de mucosidad restaurada que en conjunto forman una barrera crucial entre el cuerpo y el contenido intestinal.
Calmar el sistema inmunitario y reequilibrar el microbioma
Más allá de la reparación física, los probióticos blindados remodelaron el panorama inmunitario y microbiano en el intestino enfermo. En la sangre y el colon de ratones enfermos, los niveles de moléculas inflamatorias eran altos y los de una señal antiinflamatoria clave eran bajos; el nuevo tratamiento revirtió estas tendencias, desplazando el sistema inmunitario hacia un estado más calmado. Los análisis celulares detallados mostraron cambios en la mezcla de células inmunitarias tanto en el colon como en el bazo. Al mismo tiempo, la secuenciación del ADN de los microbios intestinales reveló que la terapia aumentó la diversidad microbiana general y potenció la presencia de varios grupos de bacterias vinculadas a la salud intestinal, incluidos Akkermansia y Muribaculum. El perfilado de metabolitos mostró además cambios generales en pequeñas moléculas relacionadas con el metabolismo de vitaminas, ácidos grasos y aminoácidos, lo que sugiere que el microbioma reequilibrado estaba produciendo un entorno químico más compatible con la curación.
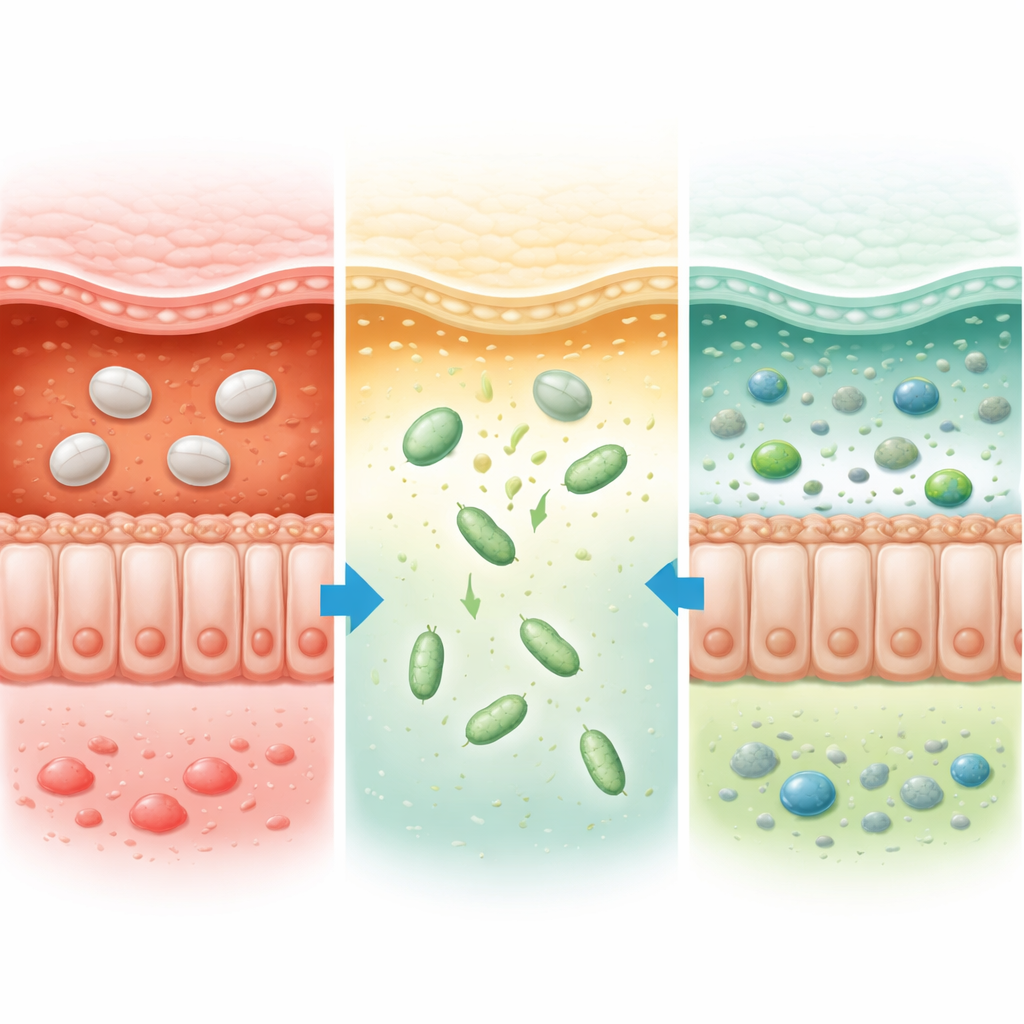
Del estudio en ratones a futuras medicinas vivas
En conjunto, el trabajo demuestra que dotar a los probióticos de una armadura sensible al pH puede transportarlos de forma fiable a través del difícil trayecto digestivo y depositarlos donde la colitis ulcerosa causa más daño. En ratones, esta estrategia permitió que dosis mucho más bajas de bacterias colonizaran el colon, repararan la barrera intestinal, redujeran la inflamación dañina y restauraran una comunidad microbiana y un perfil metabólico más saludables. Dado que el recubrimiento de origen vegetal en sí en gran medida atraviesa el cuerpo sin cambios y el método puede aplicarse a muchos tipos bacterianos, los autores sostienen que su enfoque ofrece un plan de amplio alcance para diseñar medicinas “vivas” de próxima generación para la colitis ulcerosa y otras enfermedades del colon.
Cita: Liu, J., Fang, Z., Li, X. et al. Surface decoration of bacteria generates robust living therapeutics for improved ulcerative colitis therapy. Commun Biol 9, 428 (2026). https://doi.org/10.1038/s42003-026-09732-6
Palabras clave: colitis ulcerosa, probióticos, microbioma intestinal, administración de fármacos, barrera intestinal