Clear Sky Science · es
Los activadores de NRF2 y el inhibidor de exportación nuclear, selinexor, restringen los coronavirus al dirigirse a una red que involucra ACE2, TMPRSS2 y XPO1 mediante un mecanismo independiente de NRF2
Fármacos que ayudan a las células a decir “no” a los coronavirus
La mayoría de los tratamientos contra coronavirus actuales atacan directamente al propio virus. Pero los virus son maestros del cambio, y las nuevas variantes pueden anular rápidamente esos fármacos. Este estudio explora una estrategia distinta: ayudar a que nuestras propias células sean menos hospitalarias frente a coronavirus peligrosos como el SARS-CoV-2 y ante cepas estacionales más benignas. Al ajustar cómo las células manejan unas pocas proteínas clave de control, los investigadores muestran que pequeñas moléculas ya conocidas pueden reducir notablemente la infección en modelos de laboratorio, y lo hacen de una forma que no depende de la vía antiviral por la que se hicieron célebres.
Un nuevo enfoque para la defensa contra coronavirus
El equipo se centró en compuestos conocidos por activar un programa de protección celular controlado por una proteína llamada NRF2. Estos compuestos —4-octil itaconato (4OI), bardoxolona (BARD) y sulforafano (SFN)— se probaron junto con selinexor (SEL), un fármaco que bloquea una proteína de transporte llamada XPO1, que facilita la salida de otras proteínas del núcleo celular. En modelos de células pulmonares y renales, los cuatro fármacos redujeron los niveles de SARS-CoV-2 sin dañar las células. También fueron eficaces frente a varias variantes de preocupación. Sorprendentemente, cuando NRF2 se eliminó genéticamente, los virus se replicaron mejor, lo que prueba que NRF2 es protector de forma natural —pero los fármacos siguieron funcionando bien, lo que indica que su poder antiviral procede por una vía distinta. 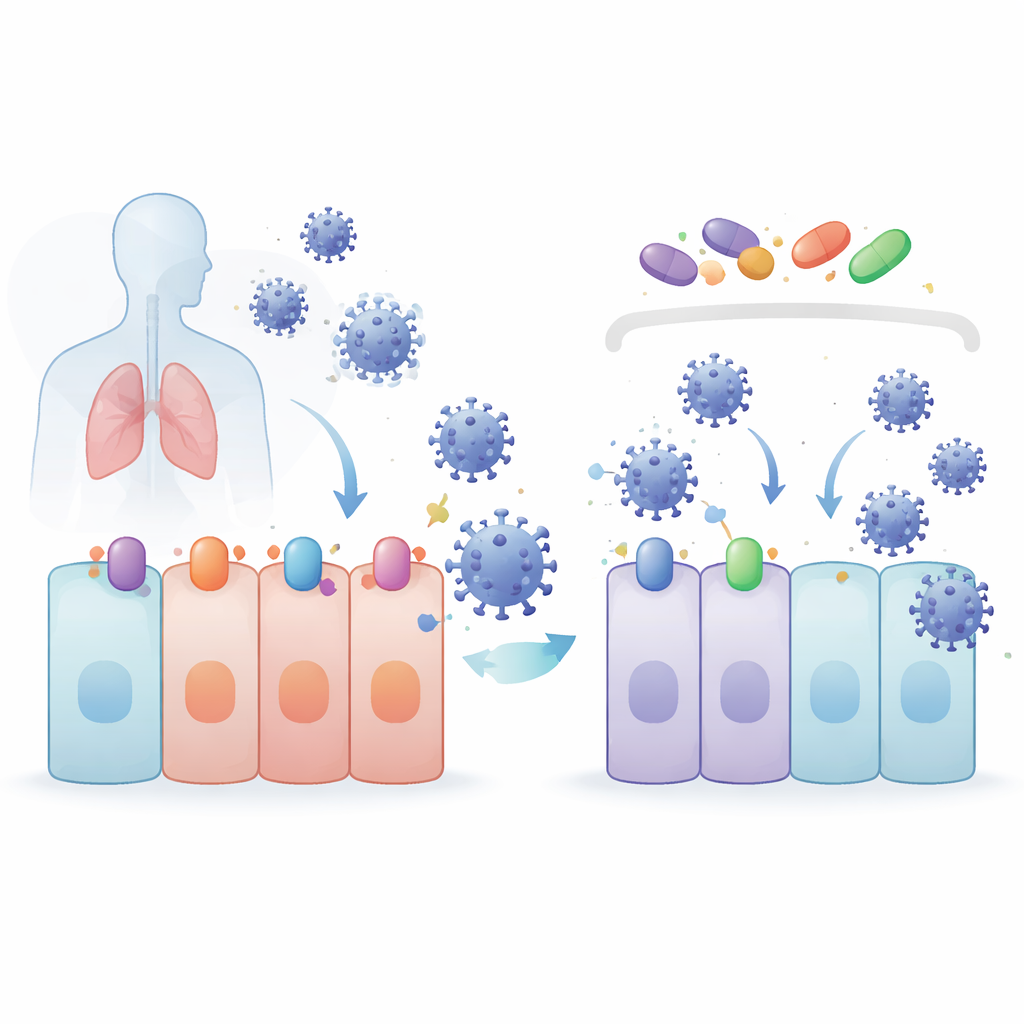
Cerrando la puerta de entrada viral
Los coronavirus inician la infección acoplándose a proteínas receptoras en la superficie celular. Para SARS-CoV-2 y sus parientes cercanos, la puerta principal es ACE2, con la ayuda de una enzima cortadora llamada TMPRSS2. La proteína de exportación XPO1 también parece favorecer la infección. Los investigadores hallaron que 4OI, BARD, SFN y SEL redujeron las cantidades de ACE2, TMPRSS2 y XPO1 en células humanas pulmonares. 4OI y SEL fueron especialmente potentes cuando estaban presentes antes de la infección, y bloquearon la entrada de partículas similares a virus cubiertas con las proteínas spike de coronavirus. En otras palabras, estos fármacos no solo ralentizan al virus después de que entra: ayudan a eliminar las cerraduras y los tiradores que el virus necesita para abrir la puerta en primer lugar.
Cómo las células desmantelan ayudas virales clave
Ahondando más, el equipo mostró que 4OI acelera la degradación de la proteína ACE2. En condiciones normales, ACE2 perdura durante muchas horas; con 4OI, desapareció de la superficie celular en una fracción de ese tiempo. Esta destrucción requirió dos etiquetadores celulares, NEDD4L y MDM2, que colocan banderas moleculares de “desecharme” en las proteínas. Bloquear a estos etiquetadores debilitó la capacidad de 4OI para eliminar ACE2. Sorprendentemente, la maquinaria habitual de degradación de proteínas, el proteasoma, no fue la vía principal. En cambio, ACE2 fue canalizada hacia el sistema de reciclaje y eliminación celular, el lisosoma. Los fármacos también redujeron la actividad génica de ACE2 y XPO1, en parte al disminuir la activación de STAT3, una proteína que normalmente potencia la transcripción del gen ACE2. 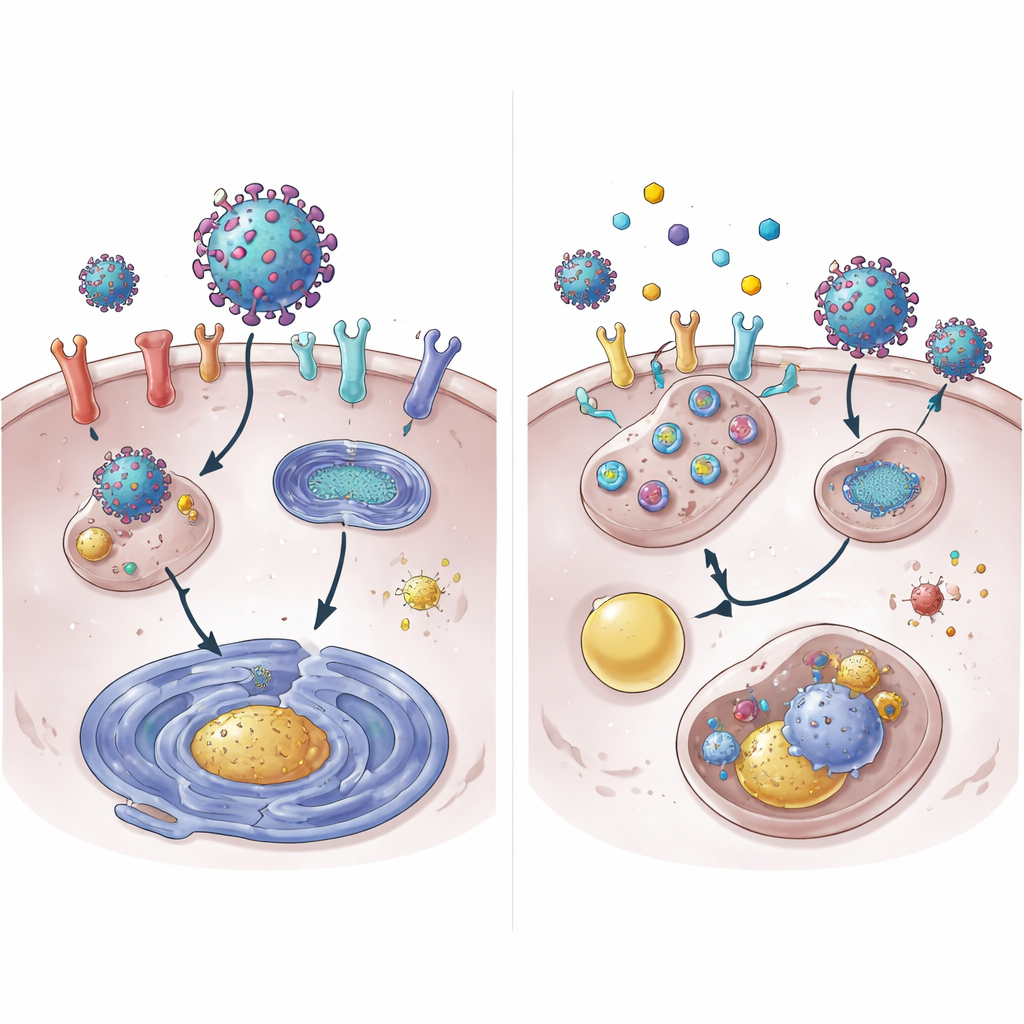
Coronavirus estacionales y la conexión con XPO1
Los científicos se centraron después en hCoV-229E, un coronavirus estacional que suele causar resfriados leves pero puede ser peligroso en personas con sistemas inmunitarios debilitados. Usando virus diseñados para brillar cuando se replican, mostraron que los cuatro compuestos suprimían con fuerza al 229E en células pulmonares y de vasos sanguíneos, incluso cuando NRF2 estaba ausente. A diferencia de SARS-CoV-2, este virus usa un receptor distinto, ANPEP, que los fármacos no modificaron. En cambio, su impacto se relacionó estrechamente con la intensidad con que redujeron XPO1. Reducir la expresión de XPO1 por sí sola bajó drásticamente la replicación de 229E, y el efecto de selinexor casi desapareció en células con bajos niveles de XPO1. Esta clasificación —SEL la más dependiente de XPO1, BARD la menos— sugiere que cada compuesto tiene una mezcla ligeramente distinta de objetivos, con XPO1 como un nodo central para gran parte de su acción antiviral.
Qué podría significar esto para tratamientos futuros
Para el público general, el mensaje clave es que es posible combatir los coronavirus no solo atacando al virus, sino reconfigurando suavemente nuestras propias células para que sean más difíciles de infectar. En células humanas cultivadas en laboratorio, los compuestos estudiados eliminaron sitios de anclaje y vías auxiliares cruciales de los que dependen SARS-CoV-2 y un coronavirus del resfriado común, y lo hicieron en gran medida sin la misma vía NRF2 que inicialmente los hizo atractivos. Aunque estos hallazgos siguen siendo preclínicos y todavía no se traducen directamente en medicamentos, señalan una vía prometedora: fármacos que reducen simultáneamente la entrada viral, atenúan la inflamación dañina y protegen tejidos al dirigirse a una red compartida de proteínas del hospedador como ACE2, TMPRSS2 y XPO1.
Cita: Waqas, F.H., Silva da Costa, L., Zapatero-Belinchón, F.J. et al. NRF2 activators and the inhibitor of nuclear export, selinexor, restrict coronaviruses by targeting a network involving ACE2, TMPRSS2, and XPO1 through an NRF2-independent mechanism. Commun Biol 9, 384 (2026). https://doi.org/10.1038/s42003-026-09724-6
Palabras clave: antivirales dirigidos al hospedador, entrada del coronavirus, ACE2 y TMPRSS2, activadores de NRF2, inhibición de XPO1