Clear Sky Science · es
Cuantificación ultrarrápida y específica de miRNA mediante cinética de oscurecimiento de fluorescencia a nivel de molécula única
Por qué importan las pruebas rápidas de enfermedad
El diagnóstico de enfermedades como el cáncer o las infecciones virales a menudo depende de detectar trazas minúsculas de material genético en la sangre u otros fluidos corporales. Las pruebas estándar de referencia actuales pueden ser muy precisas, pero a veces son lentas, costosas o tienen dificultades para detectar señales muy raras. Este estudio presenta un nuevo método basado en microscopía, llamado Q‑FISH, que puede leer estas pistas genéticas en menos de un segundo. Si se tradujera a herramientas clínicas, tal velocidad y precisión podrían facilitar la detección temprana de enfermedades, seguir la respuesta a tratamientos y personalizar la atención para cada paciente.
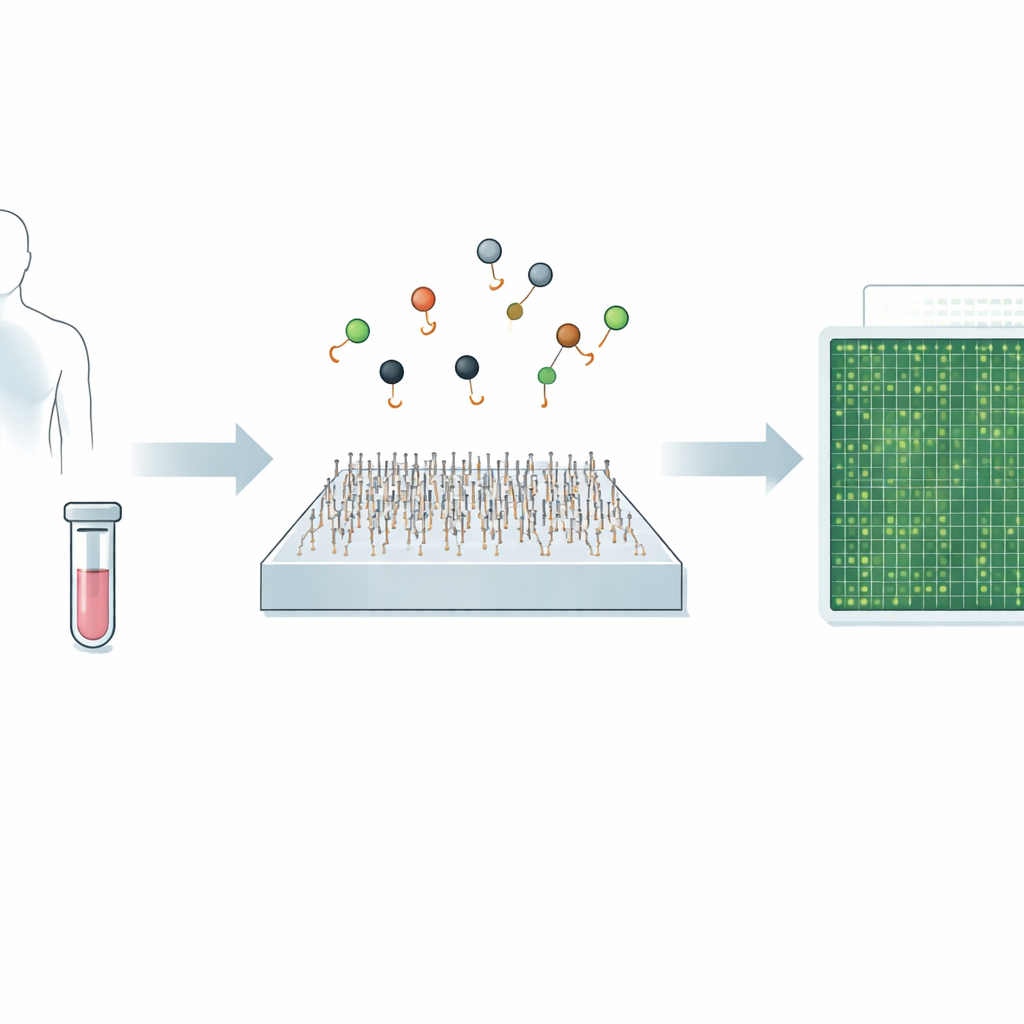
Una nueva forma de ver mensajes genéticos minúsculos
El trabajo se centra en los microARN—fragmentos cortos de ARN que regulan el uso de nuestros genes y que están estrechamente vinculados a muchos cánceres, enfermedades cardíacas, infecciones y trastornos cerebrales. Debido a que los microARN son tan pequeños y a menudo difieren por solo uno o dos nucleótidos, los métodos estándar como la PCR y la secuenciación de nueva generación pueden tener problemas para distinguir tipos estrechamente relacionados, especialmente cuando están presentes a niveles muy bajos. Enfoques recientes de imagen de moléculas individuales mejoraron esta especificidad al seguir cómo sondas individuales se unen y se desprenden, pero seguían siendo relativamente lentos, requiriendo cerca de diez minutos para analizar un solo objetivo.
Observar el parpadeo de la luz para encontrar el objetivo correcto
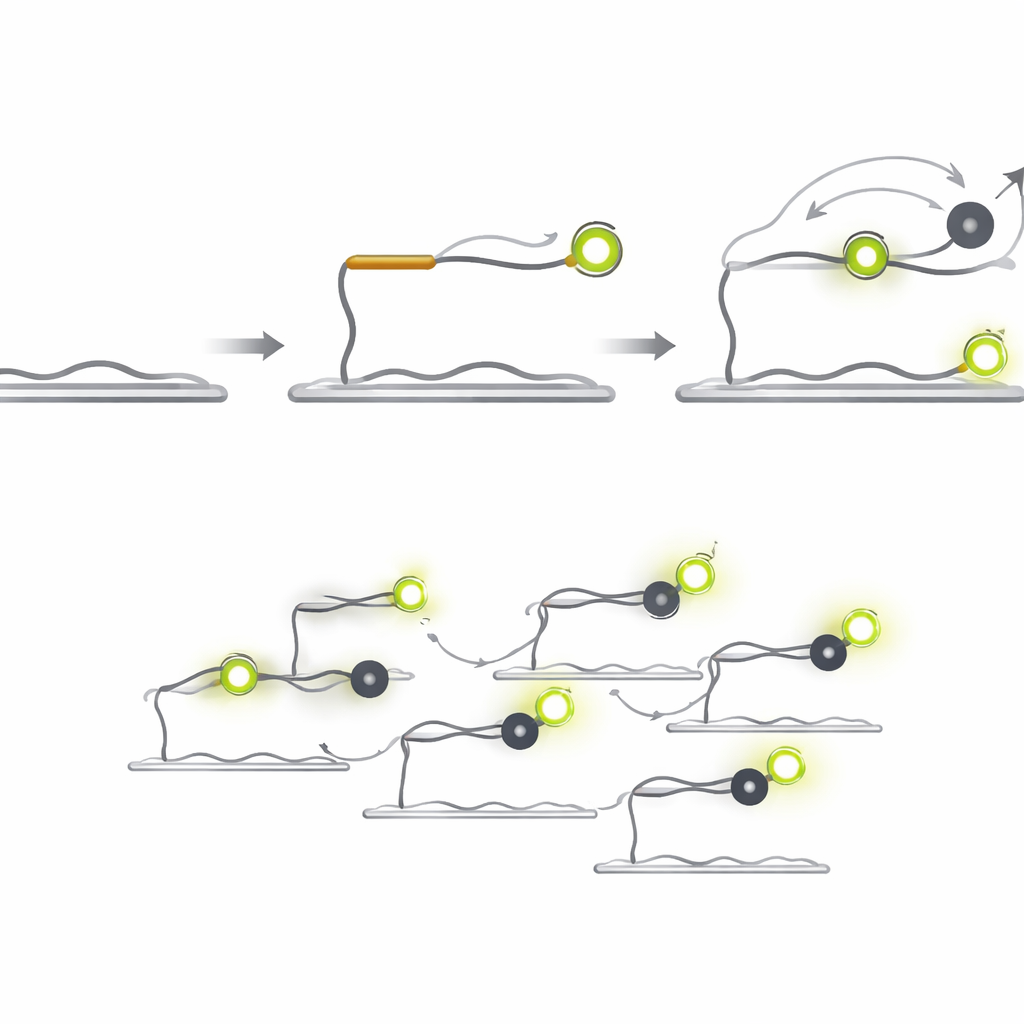
Q‑FISH invierte el problema aprovechando los breves destellos de luz de moléculas individuales. El método utiliza dos sondas de ADN cortas que reconocen posiciones contiguas en un microARN objetivo. Una sonda lleva un tinte fluorescente que brilla bajo un láser, mientras que la otra lleva un “apagador” (quencher) que absorbe la luz cuando se acerca. La sonda fluorescente se une al objetivo y permanece el tiempo suficiente para ser vista, mientras que la sonda con quencher está diseñada para unirse y soltarse muy rápidamente. Cada vez que el quencher aterriza junto al tinte, la luz cae de forma súbita; cuando se va, la luz vuelve a subir. Al registrar estos rápidos destellos de encendido‑apagado de moléculas individuales y analizar cuánto duran los periodos brillantes y tenues, el sistema puede decidir si hay un objetivo real presente.
De minutos a milisegundos
Puesto que la sonda quencher no emite luz propia, puede usarse a concentraciones mucho mayores que las sondas fluorescentes sin generar un resplandor de fondo. Acortar la sonda quencher aumenta la rapidez con la que se desprende, y elevar su concentración aumenta la frecuencia con que se une. Juntas, estas decisiones de diseño conducen a un salto dramático en la velocidad. En pruebas con un microARN relacionado con el cáncer denominado let‑7a, Q‑FISH alcanzó más del 70% de su eficiencia máxima de detección en solo un segundo de observación. Métodos comparables de molécula única necesitaron decenas a cientos de segundos para lograr un rendimiento similar, lo que hace que Q‑FISH sea en la práctica más de 600 veces más rápido.
Separar señales casi idénticas y medir muestras reales
Los investigadores también demostraron que Q‑FISH puede distinguir entre varios miembros de la familia de microARN let‑7, que comparten secuencias casi idénticas pero tienen roles distintos en el control de genes vinculados al cáncer. Emplearon dos estrategias de multiplexado. En una, se introdujeron diferentes sondas quencher una tras otra, cada una afinada para un microARN ligeramente distinto; en la otra, las sondas se marcaron con colores diferentes y se visualizaron al mismo tiempo. En ambos casos, leer los patrones de parpadeo permitió al equipo identificar correctamente qué microARN era cuál en alrededor de un segundo. Finalmente, aplicaron el método al ARN total extraído de tejidos humanos de hígado y pulmón. Añadiendo cantidades conocidas de microARN sintéticos y contando los puntos resultantes, construyeron curvas de calibración y luego determinaron los niveles naturales presentes en los tejidos, revelando diferencias claras entre órganos.
Qué podría significar esto para futuras pruebas
En conjunto, el estudio muestra que Q‑FISH puede seleccionar microARN específicos con muy alta precisión, incluso cuando son casi idénticos entre sí, y hacerlo a velocidades que superan con creces a los métodos previos de molécula única. Aunque los experimentos se realizaron en muestras preparadas usando un microscopio especializado, la idea subyacente—usar eventos rápidos de oscurecimiento de la luz en lugar de depender únicamente de uniones lentas—podría adaptarse a muchos tipos de marcadores genéticos, incluidos fragmentos de ADN tumoral en sangre. Con un mayor desarrollo y una preparación de muestras más ágil, este enfoque podría ayudar a acercar diagnósticos moleculares rápidos, altamente multiplexados y extremadamente sensibles al uso clínico cotidiano.
Cita: Kim, J., Hohng, S. Ultrafast and specific miRNA quantification via single-molecule fluorescence quenching kinetics. Commun Biol 9, 432 (2026). https://doi.org/10.1038/s42003-026-09714-8
Palabras clave: detección de microRNA, imágenes de moléculas individuales, diagnóstico molecular, oscurecimiento de fluorescencia, biópsia líquida