Clear Sky Science · es
Una estrategia en dos pasos mediada por actina permite a Campylobacter jejuni promover la agregación mitocondrial y la homeostasis del hierro, para la supervivencia y persistencia intracelular
Por qué importa esta pequeña batalla dentro de las células
La intoxicación alimentaria por pollo poco cocinado suele atribuirse a una bacteria llamada Campylobacter jejuni. La mayoría de las personas se recupera, pero este microbio es sorprendentemente bueno sobreviviendo en muchos entornos, lo que facilita su propagación de la granja a la mesa. Este estudio analiza lo que ocurre cuando la bacteria se oculta dentro de una ameba de vida libre —un microbio de agua dulce común— y revela un truco de supervivencia sorprendentemente sofisticado que gira en torno a remodelar el esqueleto interno de la célula, agrupar los “paquetes de energía” llamados mitocondrias y controlar el hierro y la química oxidativa dañina. Comprender esta fase oculta de su ciclo vital podría señalar nuevas formas de frenar la contaminación antes de que la bacteria llegue a las personas.
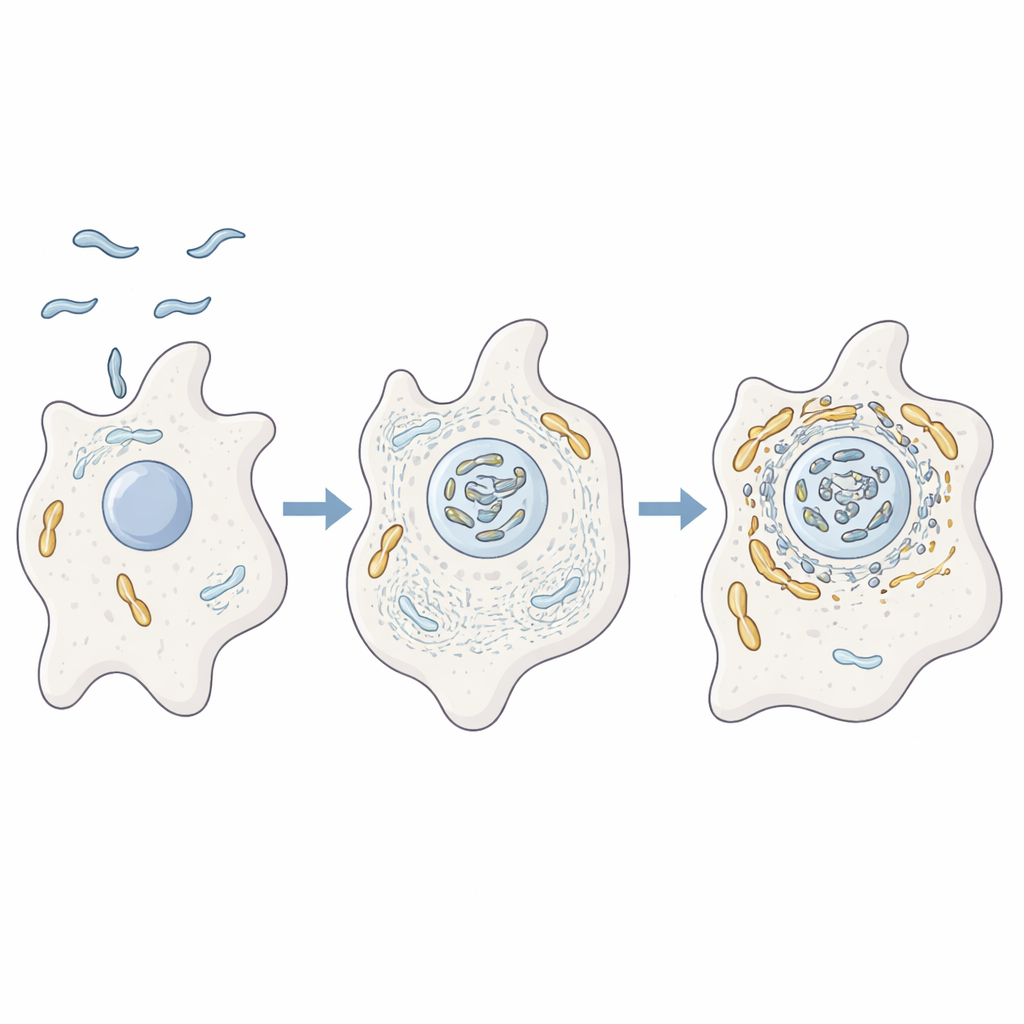
Un microbio que se entrena dentro de las amebas
Los autores estudiaron cómo se comporta C. jejuni dentro de la ameba Acanthamoeba castellanii, un organismo unicelular que vive en el suelo y en el agua. Estas amebas actúan como campos de entrenamiento para muchas bacterias patógenas, ofreciendo protección frente a condiciones adversas y a desinfectantes. Mediante análisis avanzados de proteínas, microscopía y mutantes genéticos, los investigadores mostraron que cuando C. jejuni infecta amebas termina estrechamente asociado con las mitocondrias del hospedador. Al mismo tiempo, el andamiaje interno de actina de la ameba, junto con proteínas que regulan su forma y movimiento, se encuentra fuertemente enriquecido cerca de estas mitocondrias, lo que sugiere que la bacteria está reorganizando activamente la arquitectura interna de la célula.
Doblar el esqueleto celular para mover los paquetes de energía
Para comprobar si la actina realmente impulsa esta interacción, el equipo bloqueó la formación de filamentos de actina y su ramificación en redes. En estas condiciones, las mitocondrias dejaron de agruparse cerca de las bacterias y permanecieron dispersas como puntos, y la supervivencia bacteriana disminuyó. Luego se centraron en dos proteínas bacterianas colaboradoras, CiaD y CiaI, que se inyectan en las células del hospedador a través del flagelo de la bacteria, una cola parecida a un látigo. CiaD resultó potenciar el crecimiento de actina y promover proyecciones puntiagudas en la superficie de la ameba, ayudando a la célula a capturar las bacterias. Una vez dentro, se observó que las mitocondrias se agrupaban alrededor del compartimento bacteriano de forma dependiente de la actina, ubicando a la bacteria en una zona privilegiada rica en maquinaria energética del hospedador.
Un interruptor molecular que remodela las mitocondrias
Mientras que CiaD es clave para la entrada, CiaI controla lo que ocurre después. Cuando los investigadores eliminaron el gen de CiaI, C. jejuni dejó de desencadenar una fuerte agregación mitocondrial y sobrevivió mal dentro de las amebas. Añadir CiaI purificada acoplada a pequeñas cuentas, sin bacterias vivas, fue suficiente para provocar la fusión y agrupación de mitocondrias cercanas y para eliminar localmente actina. Pruebas bioquímicas mostraron que CiaI se une a moléculas transportadoras de energía de manera cooperativa, comportándose como un interruptor molecular que puede activar o desactivar su actividad según las condiciones dentro del hospedador. Los autores proponen que, tras el crecimiento de actina impulsado por CiaD que acerca las mitocondrias, CiaI induce la degradación local de actina y remodela la red mitocondrial en agregados densos que rodean el compartimento que contiene a la bacteria.
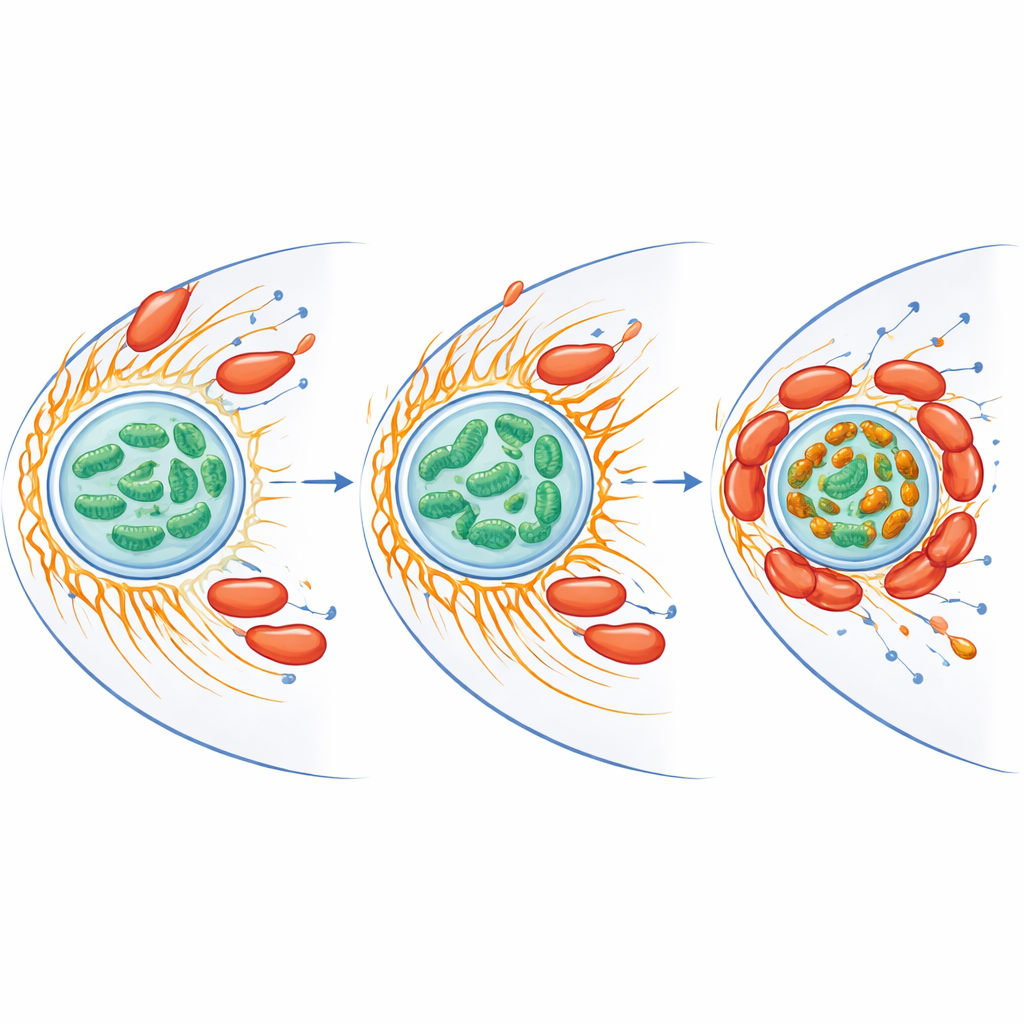
Reconfigurar el hierro y el estrés dentro de la célula hospedadora
Las mitocondrias hacen más que producir energía: también gestionan el hierro y generan especies reactivas de oxígeno, formas químicamente agresivas de oxígeno que pueden matar microbios. Los investigadores encontraron que la infección redujo el hierro libre total dentro de las mitocondrias pero, al mismo tiempo, creó brillantes racimos ricos en hierro donde las mitocondrias se agregaban alrededor de las bacterias. Las proteínas implicadas en el manejo del hierro y en la defensa frente al estrés oxidativo aumentaron tanto en el hospedador como en la bacteria. Cuando el equipo eliminó el hierro libre usando un quelante, el estallido de especies reactivas de oxígeno de la ameba disminuyó y la supervivencia de C. jejuni aumentó de forma notable. Las mitocondrias en células infectadas también mostraron un mayor potencial de membrana, signo de actividad elevada, lo que sugiere que la bacteria empuja a los “paquetes de energía” del hospedador hacia un estado que favorece su propia persistencia mientras limita la química oxidativa dañina.
Qué significa esto para la seguridad alimentaria y la infección
En conjunto, los resultados respaldan una estrategia en dos pasos: primero, CiaD estimula el crecimiento de actina para ayudar a la bacteria a entrar en las amebas y atraer mitocondrias hacia el sitio de entrada; segundo, CiaI desmantela localmente la actina y remodela las mitocondrias en racimos ricos en hierro envolviendo el compartimento bacteriano, al tiempo que atenúa las defensas oxidativas del hospedador. Este control finamente ajustado de la forma celular, el uso de energía y el equilibrio metálico ayuda a C. jejuni a sobrevivir dentro de las amebas y probablemente contribuye a su capacidad para persistir en el ambiente y posteriormente infectar a humanos. Al revelar los actores clave en este tira y afloja microscópico, el estudio apunta a nuevos objetivos —como las proteínas Cia, los contactos actina-mitocondria o las vías de manejo del hierro— que podrían ser interferidos para reducir la contaminación y la enfermedad.
Cita: Nasher, F., Wren, B.W. A two-step actin-mediated strategy enables Campylobacter jejuni to promote mitochondrial aggregation and iron homeostasis, for intracellular survival and persistence. Commun Biol 9, 431 (2026). https://doi.org/10.1038/s42003-026-09713-9
Palabras clave: Campylobacter, amebas, mitocondrias, citoesqueleto de actina, homeostasis del hierro