Clear Sky Science · es
La regulación en múltiples capas de los receptores kainato GluK3 está mediada por subunidades Neto y por zinc
Por qué importan los pequeños interruptores del cerebro
Cada pensamiento, recuerdo y estado de ánimo del cerebro depende de interruptores microscópicos que permiten el flujo de partículas cargadas dentro y fuera de las células nerviosas. Este estudio se centra en uno de esos interruptores, un receptor poco conocido llamado GluK3. Al descubrir cómo proteínas asociadas y iones de zinc afinan el comportamiento de GluK3, el trabajo ofrece pistas sobre cómo los circuitos cerebrales mantienen el equilibrio—y cómo ese equilibrio puede inclinarse en trastornos como la epilepsia, la depresión y la esquizofrenia.
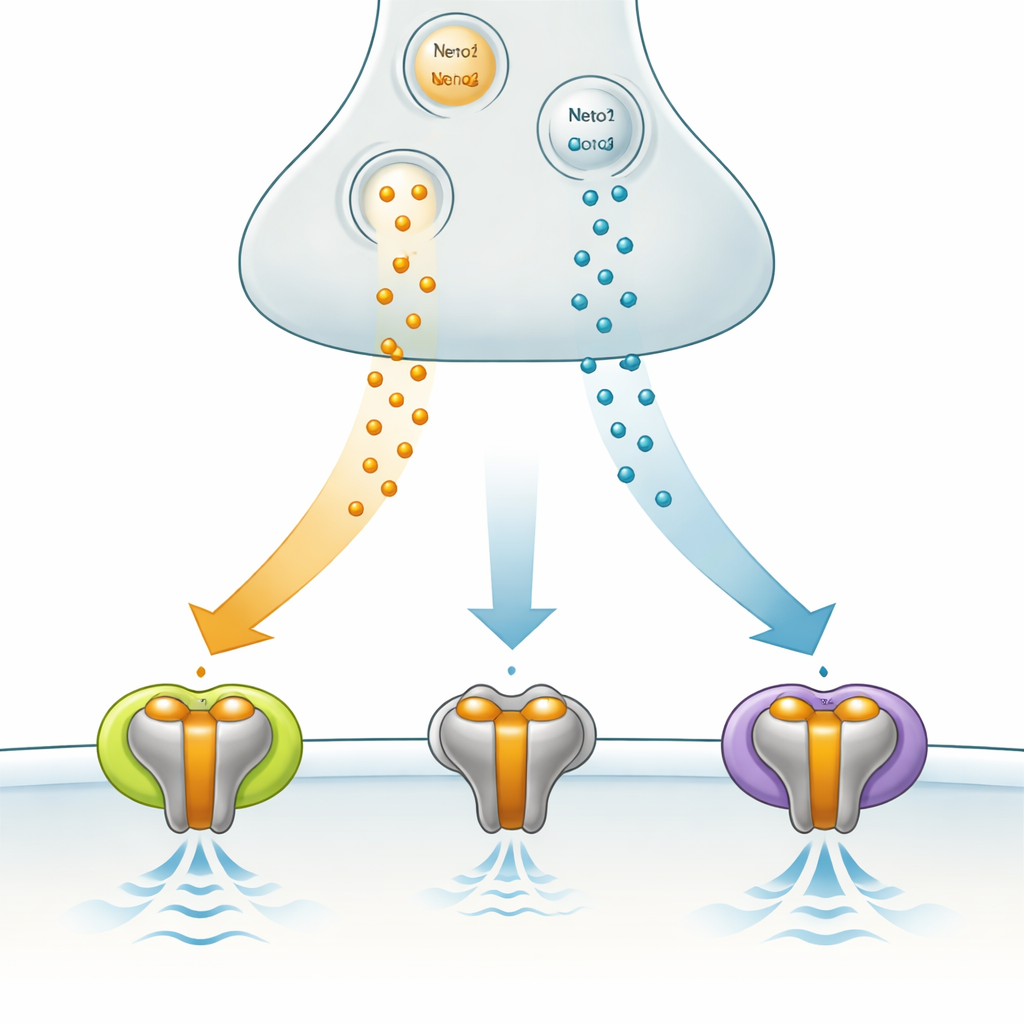
Una compuerta de señal especializada en el cerebro
GluK3 pertenece a la familia de los receptores kainato, que forman parte del grupo más amplio de receptores de glutamato que median la comunicación rápida entre neuronas. A diferencia de algunos de sus parientes, GluK3 no simplemente enciende o apaga señales; actúa más como un filtro que responde mejor a ráfagas breves y fuertes del mensajero químico glutamato. Está enriquecido en regiones cerebrales como el hipocampo, crucial para la memoria y la organización de los ritmos de la red, y los cambios en la función de GluK3 se han asociado con comportamientos relacionados con la ansiedad. Estas características hacen de GluK3 un objetivo prometedor, pero aún poco comprendido, para modular la actividad cerebral en salud y enfermedad.
Proteínas auxiliares que mueven los hilos
El equipo examinó cómo dos proteínas auxiliares, Neto1 y Neto2, modifican el comportamiento de GluK3 en células humanas diseñadas para expresar estos componentes. Ambas ralentizaron la rapidez con que GluK3 se apaga tras activarse, y ambas redujeron una forma natural de bloqueo interno que normalmente limita el flujo de corriente. Sin embargo, tuvieron efectos opuestos sobre la velocidad con que GluK3 puede reutilizarse. Con Neto1, los receptores se recuperaban rápidamente, listos para responder a señales rápidas y repetidas. Con Neto2, la recuperación se volvió mucho más lenta, favoreciendo la integración de señales durante intervalos más largos. En esencia, al elegir diferentes proteínas auxiliares, una sinapsis puede decidir si GluK3 actúa como un detector de disparos rápidos o como un sensor más lento que promedia señales.
El zinc como una segunda capa de control
Muchos terminales nerviosos que liberan glutamato también liberan zinc, que puede unirse a los receptores y cambiar su funcionamiento. Trabajos anteriores mostraron que el zinc aumenta inusualmente la actividad de GluK3, mientras que tiende a atenuar otros tipos de receptores. Aquí, los autores encontraron que este incremento depende fuertemente de qué proteína Neto esté presente. Cuando GluK3 actúa solo, el zinc aproximadamente duplica el tiempo que el receptor permanece activo y aumenta de forma modesta la corriente. Añadir Neto1 reduce este efecto. En contraste, cuando GluK3 se asocia con Neto2, el zinc y Neto2 actúan juntos para aumentar enormemente la corriente, mucho más de lo que podría cualquiera por separado. Esto sugiere que las sinapsis ricas en Neto2 y zinc pueden amplificar fuertemente las señales mediadas por GluK3 durante actividad intensa, mientras que las sinapsis ricas en Neto1 permanecen más contenidas.
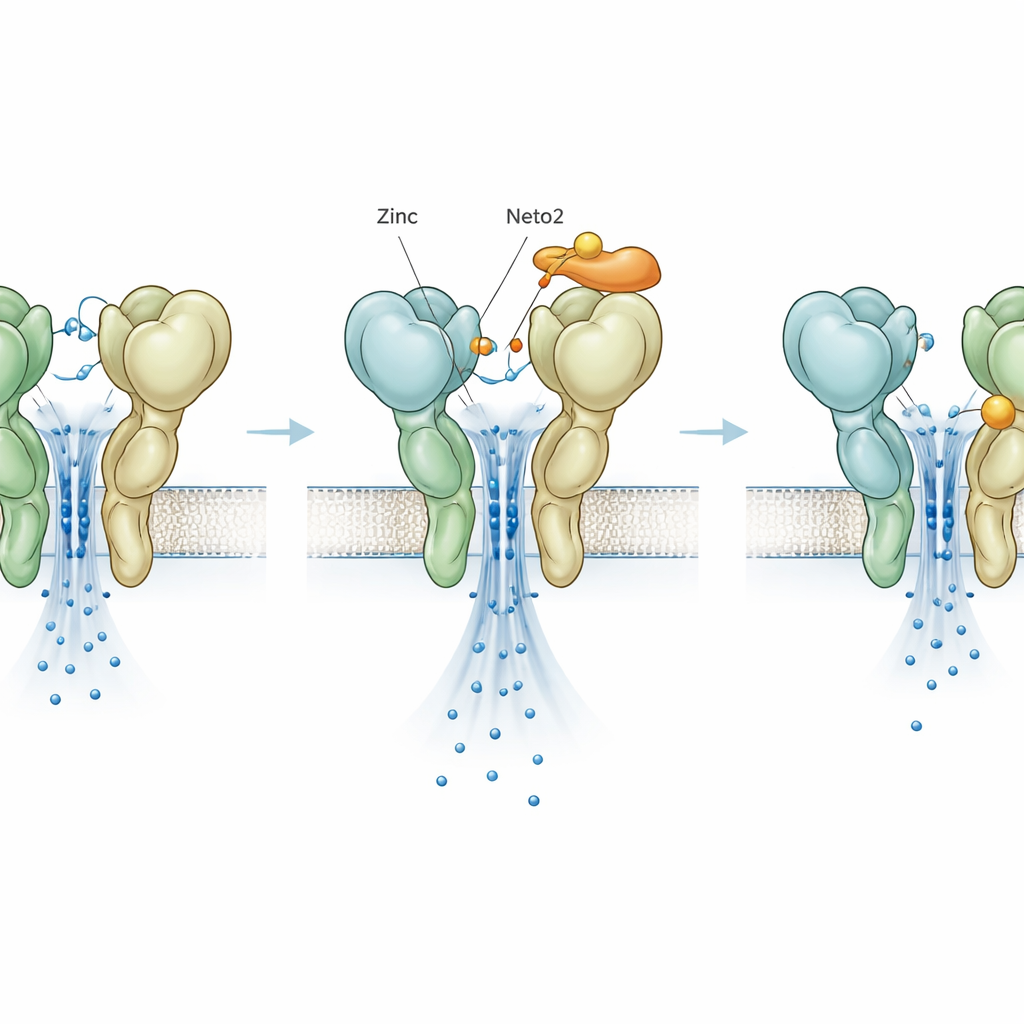
Un freno oculto revelado por una mutación
Para separar las acciones del zinc de las de las proteínas auxiliares, los investigadores introdujeron un cambio de una sola letra en GluK3, llamado D759G, que elimina un sitio conocido de unión al zinc. Como era de esperar, esta mutación por sí sola hizo que el receptor fuera más estable y más lento para apagarse, imitando el efecto habitual del zinc. Sorprendentemente, cuando se añadió zinc a este mutante, ya no incrementó la actividad; en cambio, aceleró el apagado y redujo la corriente, revelando un segundo sitio de zinc previamente oculto que actúa como un freno. Neto1 y Neto2 siguieron ejerciendo sus efectos característicos sobre el mutante, lo que muestra que su influencia principal no depende del sitio original de zinc. Sin embargo, incluso esta nueva acción inhibidora del zinc fue modulada de manera diferente por las dos auxiliares, añadiendo otro mando ajustable al sistema.
Ver la estructura detrás del comportamiento
Para conectar la función con la forma, el equipo usó criomicroscopía electrónica para visualizar el receptor GluK3 mutante congelado en un estado no activo. Las imágenes revelaron que la región que une el glutamato forma una unidad más compacta y densamente empaquetada en el mutante D759G en comparación con el GluK3 normal. Este apretamiento estructural probablemente dificulta que el receptor adopte una conformación de apagado, lo que explica por qué el mutante, al igual que GluK3 unido al zinc, permanece activo por más tiempo. Al mismo tiempo, las imágenes mostraron que no todas las partes del receptor estaban bloqueadas en una sola disposición, lo que apunta a una arquitectura inherentemente flexible que es especialmente sensible a pequeños impulsos químicos.
Qué significa esto para la salud cerebral
En conjunto, el estudio presenta a GluK3 no como un simple interruptor de encendido‑apagado, sino como un centro finamente ajustable donde convergen glutamato, proteínas auxiliares y zinc. Neto1 y Neto2 determinan la rapidez con que las señales se desvanecen y la velocidad con que los receptores pueden responder de nuevo, mientras que el zinc puede tanto potenciar como, en ciertas condiciones, frenar la actividad a través de múltiples sitios de unión. Dado que GluK3, las proteínas Neto y el zinc coexisten en sinapsis implicadas en la memoria y están relacionados con la epilepsia y trastornos psiquiátricos, comprender este control en múltiples capas puede orientar futuras terapias que reajusten suavemente la señalización sináptica en lugar de apagarla por completo.
Cita: Vinnakota, R., Dawath, B.K., Assaiya, A. et al. Multilayered regulation of GluK3 kainate receptors is mediated by Neto subunits and zinc. Commun Biol 9, 420 (2026). https://doi.org/10.1038/s42003-026-09707-7
Palabras clave: receptores kainato, GluK3, proteínas Neto, zinc sináptico, plasticidad sináptica