Clear Sky Science · es
Abuso de drogas adictivas y depresión: un enfoque en epigenética
Por qué esta investigación importa en la vida cotidiana
Las drogas adictivas y la depresión suelen tratarse como problemas separados, pero con frecuencia aparecen juntos en la misma persona. Esta revisión explica cómo el uso prolongado de sustancias como la metanfetamina, la cocaína, los opiáceos y el cannabis puede dejar “cicatrices moleculares” duraderas en el cerebro que aumentan el riesgo de depresión. Al descubrir estos cambios ocultos, el artículo apunta hacia futuras pruebas que podrían advertir quiénes son más vulnerables, y hacia tratamientos más precisos que podrían invertir el daño en lugar de limitarse a enmascarar los síntomas.
Cómo se entrelazan la adicción y el estado de ánimo bajo
Los autores comienzan exponiendo el estrecho vínculo clínico entre el abuso de drogas y la depresión. Las personas que usan repetidamente sustancias adictivas tienen muchas más probabilidades de informar tristeza persistente, pérdida de placer, problemas de sueño y pensamientos suicidas. Regiones cerebrales que controlan la recompensa, la motivación, la memoria y la toma de decisiones —el área tegmental ventral, el núcleo accumbens, la corteza prefrontal y el hipocampo— son centrales en ambas condiciones. La exposición crónica a drogas altera neurotransmisores como la dopamina y la serotonina, hormonas del estrés controladas por el eje hipotálamo–hipófisis–suprarrenal, señales inmunitarias y el suministro energético de las neuronas. Estos cambios, en conjunto, hacen que el cerebro sea menos resiliente frente al estrés y más propenso a estados depresivos, incluso mucho tiempo después de la última dosis.
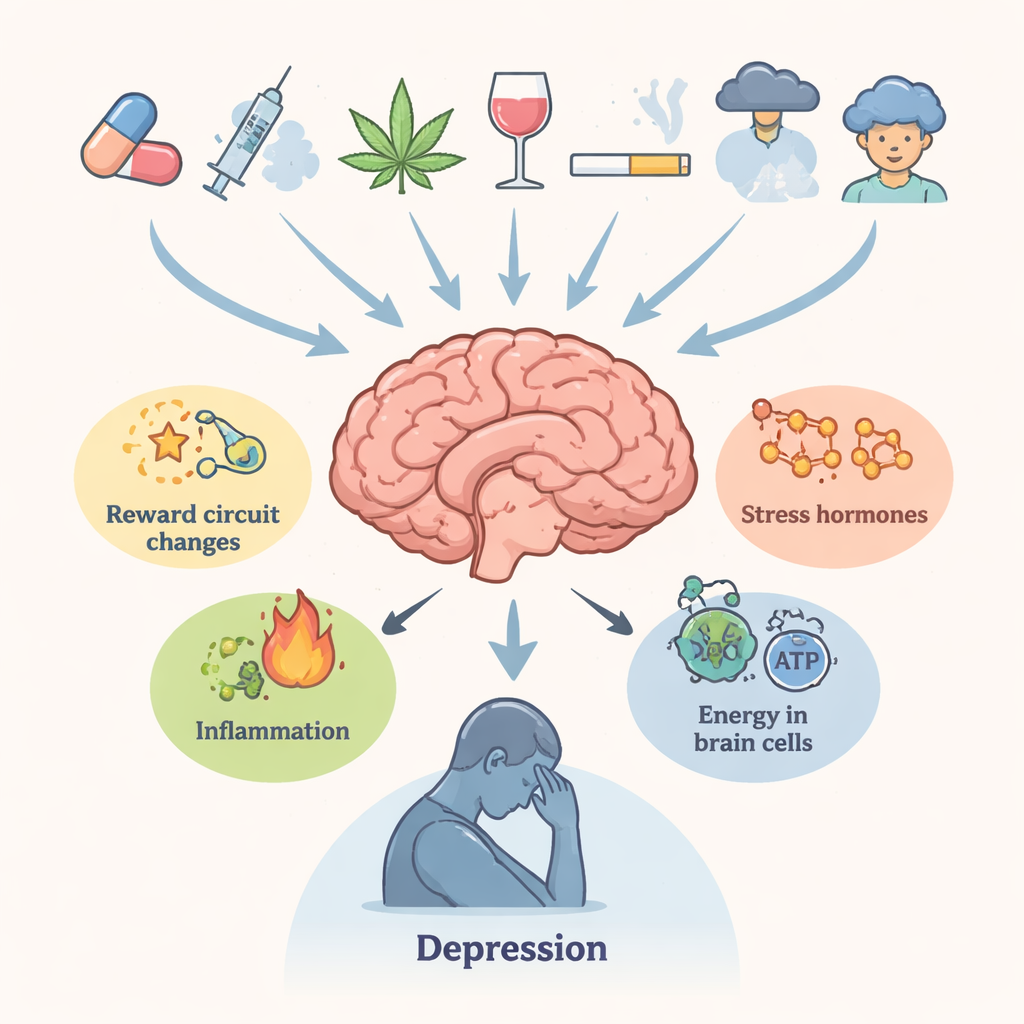
Drogas que remodelan la química cerebral
La revisión repasa varias clases principales de drogas. Los estimulantes tipo anfetamina y sus parientes, incluidos los sintéticos conocidos como “sales de baño”, provocan oleadas potentes de dopamina y otros transmisores que, con el tiempo, dañan las terminaciones nerviosas, alteran el equilibrio del glutamato, estresan el retículo endoplásmico y empujan a las células hacia una autodigestión perjudicial (autofagia). El consumo de cannabis en la adolescencia se asocia con depresión posterior y riesgo de suicidio, probablemente mediante cambios duraderos en los receptores canabinoides, la estructura de la sustancia blanca y la sensibilidad de los circuitos dopaminérgicos. Los opiáceos, aunque alivian el dolor, pueden desencadenar inflamación, fallo mitocondrial y reducción de señales de soporte del crecimiento como el factor neurotrófico derivado del cerebro (BDNF). La cocaína activa repetidamente el sistema de estrés y altera reguladores clave como FKBP5, contribuyendo a la ansiedad y al ánimo bajo durante la abstinencia. En cada caso, las alteraciones biológicas tienden a persistir, lo que ayuda a explicar por qué los síntomas emocionales pueden durar más que la intoxicación evidente.
Epigenética: la memoria de la exposición
Para entender por qué los efectos de las drogas perduran, los autores se centran en la epigenética: marcas químicas e interruptores moleculares que ajustan la actividad génica sin alterar las letras del ADN. Las drogas adictivas modifican la metilación del ADN (una marca en bases de citosina), cambian grupos químicos en las histonas que empaquetan el ADN y alteran los ARN no codificantes que afinan qué proteínas se producen. Por ejemplo, la metanfetamina y la cocaína desplazan patrones de metilación en regiones cerebrales relacionadas con la recompensa, cambiando los niveles de enzimas que añaden o eliminan estas marcas. Opiáceos y estimulantes remodelan la acetilación y metilación de histonas en genes que controlan los receptores de glutamato, la señalización del estrés y la estructura sináptica. Docenas de microARN, ARN largos no codificantes y ARN circulares aumentan o disminuyen con la exposición a drogas, influyendo en conjunto en la inflamación, el crecimiento neuronal y la fuerza de las sinapsis. Estos cambios epigenéticos actúan como una “memoria” molecular del historial de consumo.
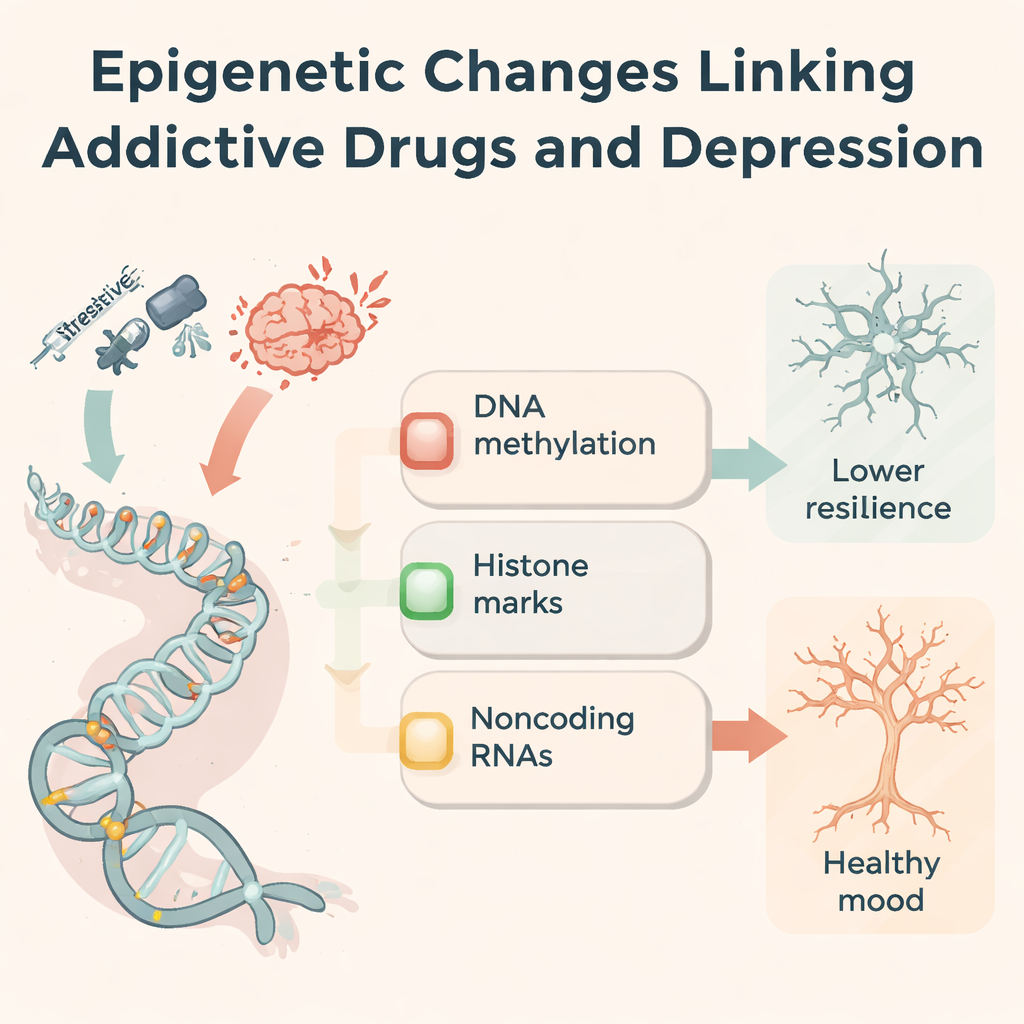
Vías moleculares compartidas en depresión y adicción
La misma maquinaria epigenética también aparece en personas y animales con depresión que nunca han consumido drogas. Las experiencias estresantes pueden alterar la metilación de receptores de hormonas del estrés (como NR3C1 y FKBP5), reducir factores de crecimiento beneficiosos como BDNF y reconfigurar vías inmunitarias y del glutamato. Muchos de los mismos ARN no codificantes cambiados por las drogas también están desregulados en la depresión, afectando cómo nacen nuevas neuronas, cómo responden las microglías a la inflamación y cuán fuertes son las conexiones sinápticas. Los autores proponen un marco de tres partes: regulación de la respuesta al estrés, remodelado de los circuitos de recompensa y plasticidad sináptica. A lo largo de estos ejes, adicción y depresión convergen repetidamente en un pequeño conjunto de genes y marcas, lo que sugiere una razón biológica por la que ambos trastornos coocurren con tanta frecuencia.
Qué significa esto para la prevención y el tratamiento futuros
Para concluir, la revisión sostiene que los cambios epigenéticos podrían convertirse en biomarcadores de alerta temprana y en dianas para tratamientos de nueva generación. Fármacos de acción amplia que borran marcas epigenéticas ya han mostrado algunos efectos similares a antidepresivos en animales, pero son demasiado imprecisos para uso humano rutinario. Nuevas herramientas —como editores del epigenoma basados en CRISPR y terapias que modulan microARN específicos o ARN largos— podrían algún día ajustar genes problemáticos en células cerebrales concretas sin afectar a otras. Los autores advierten que la mayor parte de los datos actuales proviene de roedores y de tejido cerebral a granel, y que la biología humana es más compleja. Aun así, al revelar cómo las drogas adictivas y la depresión escriben en el mismo “cuaderno” molecular, este trabajo ofrece un camino esperanzador hacia terapias más personalizadas y duraderas.
Cita: Zhang, W., Xu, M., Wang, C. et al. Addictive drug abuse and depression-a focus on epigenetics. Commun Biol 9, 297 (2026). https://doi.org/10.1038/s42003-026-09705-9
Palabras clave: adicción y depresión, epigenética, abuso de drogas, metilación del ADN, ARN no codificante