Clear Sky Science · es
La heterogeneidad entre neuronas VIP y GRP subyace a la señalización del receptor AVP en el núcleo supraquiasmático del ratón
Por qué es tan difícil reajustar nuestro reloj biológico
Cualquiera que haya salido tambaleándose de un vuelo largo o haya sufrido trabajando en turnos nocturnos sabe que nuestro reloj interno no tolera bien los cambios bruscos de horario. Este artículo plantea una pregunta muy concreta en el núcleo de ese problema: dentro del reloj maestro del cerebro, ¿por qué algunas neuronas perciben con fuerza una señal temporal mientras que sus vecinas la ignoran en gran medida? Al rastrear una única señal química a través de este pequeño circuito del reloj en ratones, los autores descubren un subgrupo oculto de células que ayudan a determinar cuán testarudo es nuestro reloj biológico frente al “jet lag”. 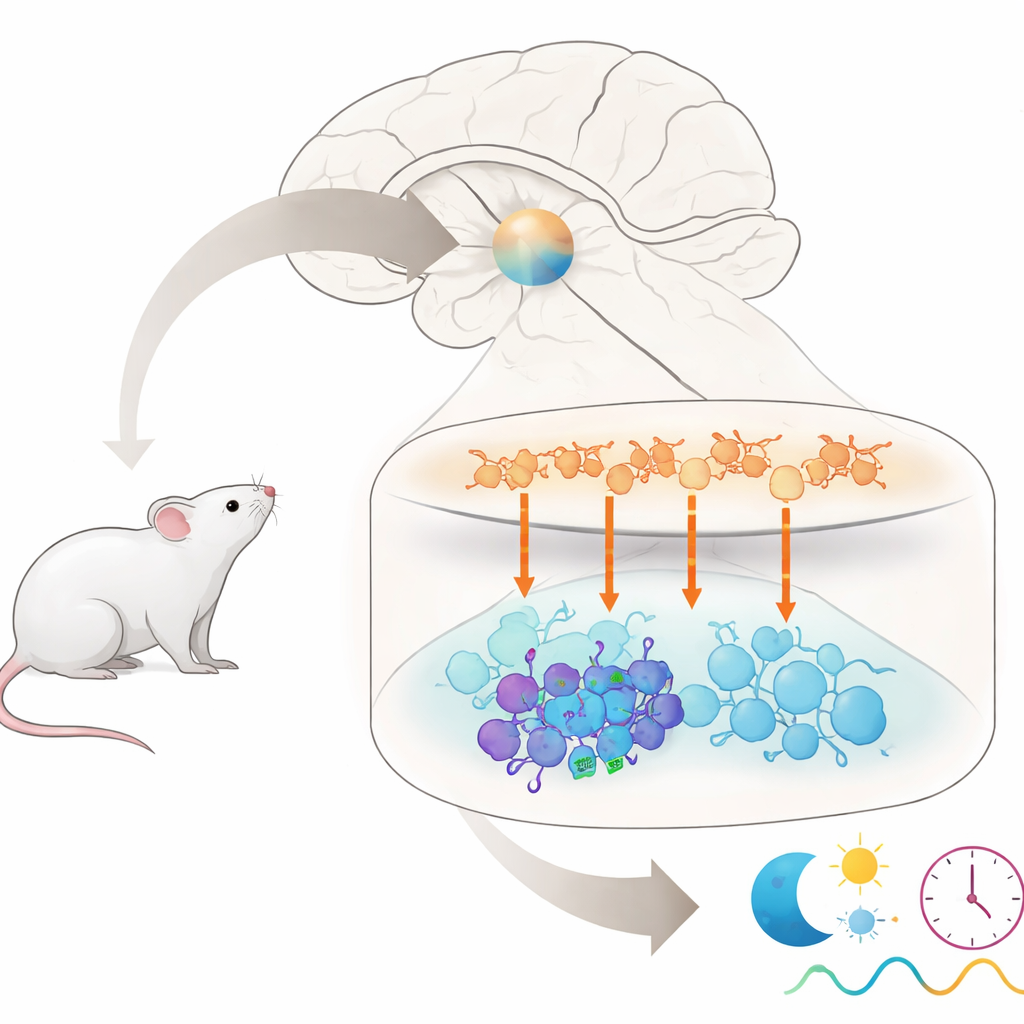
Un reloj diminuto con muchos actores distintos
El reloj maestro en los mamíferos se sitúa en una pequeña región del cerebro llamada núcleo supraquiasmático, o NSQ. Aunque contiene solo alrededor de 20.000 neuronas, está formado por varios grupos distintos que se comunican entre sí mediante diferentes mensajeros químicos. Las células en la región superior, la «corteza», liberan principalmente un mensajero llamado arginina vasopresina (AVP), mientras que las células en la región inferior, el «núcleo», suelen liberar otros mensajeros, incluidos el péptido intestinal vasoactivo (VIP) y el péptido liberador de gastrina (GRP). Juntos, estos grupos deben mantenerse sincronizados para generar los ritmos de 24 horas que regulan el sueño, la liberación hormonal y muchas otras funciones corporales. Pero no estaba claro qué células exactas del núcleo escuchan las señales procedentes de las células AVP de la corteza.
Siguiendo el cableado desde las células emisoras hasta las receptoras
Los investigadores primero mapearon cómo las células AVP de la corteza se conectan físicamente a las células VIP y GRP del núcleo. Usaron un virus para etiquetar las fibras salientes y los posibles puntos de contacto de las neuronas AVP en ratones, y luego tiñeron cortes cerebrales para ver dónde terminaban esas fibras. Encontraron que las fibras AVP formaban aparentes sitios de contacto tanto en células VIP como en GRP, pero en proporciones distintas: aproximadamente una cuarta parte de las células VIP y más de la mitad de las células GRP mostraron estas aposiciones. Esto mostró que las neuronas AVP alcanzan ambos tipos de células del núcleo, pero aún no revelaba cuáles respondían de hecho a la señal. Para probarlo, el equipo utilizó optogenética —activando las neuronas AVP con luz azul— y buscó c-Fos, un marcador de activación celular, en las neuronas VIP y GRP.
Un pequeño subgrupo de VIP que realmente “oye” AVP
Cuando las neuronas AVP fueron estimuladas por la luz, muchas de las propias células AVP activaron c-Fos, como era de esperar. De forma importante, un pequeño subconjunto de células VIP en el núcleo también mostró activación de c-Fos, aunque no expresaban directamente la proteína sensible a la luz. Esto indicó que estaban siendo activadas de forma indirecta por la entrada AVP. En contraste, las células GRP rara vez mostraron c-Fos, a pesar de recibir contactos de AVP. Los autores buscaron entonces la señal génica del receptor de AVP conocido como V1a en estas poblaciones usando métodos sensibles de imagen de ARN. Descubrieron que V1a estaba presente solo en una minoría de las células VIP y era apenas detectable en las células GRP. Así, entre las muchas neuronas VIP, parece haber un pequeño subgrupo V1a-positivo especialmente afinado para recibir y responder a señales AVP, mientras que la mayoría de las neuronas GRP no lo hacen. 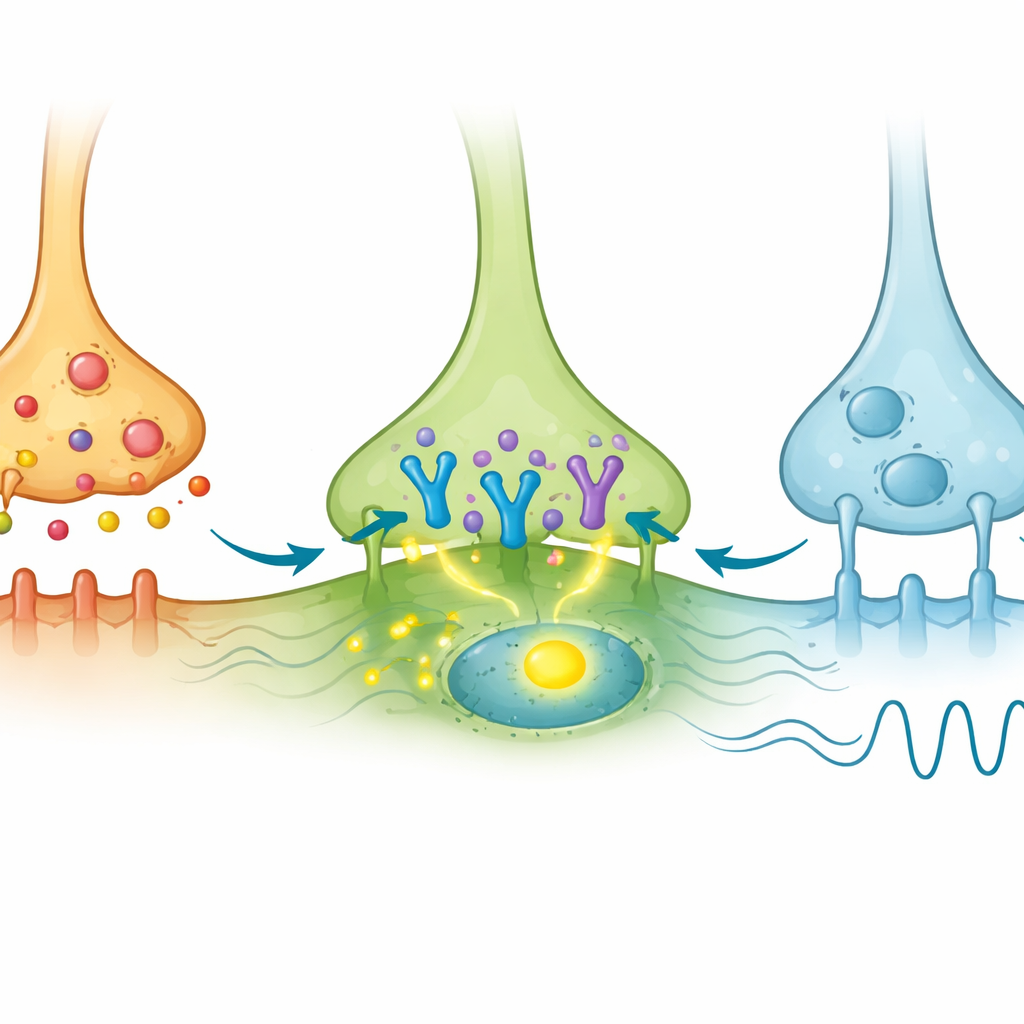
Cómo un pequeño grupo celular moldea la recuperación del jet lag
Para sondear la función de estas neuronas VIP portadoras de V1a, los investigadores crearon ratones en los que el receptor V1a fue eliminado solo de las células VIP. Estos animales mantuvieron una longitud normal del ritmo diario en oscuridad constante, lo que muestra que este receptor en las neuronas VIP no es necesario para fijar el ritmo básico del reloj. Sin embargo, cuando el ciclo luz–oscuridad se adelantó o retrasó repentinamente ocho horas para imitar el jet lag, los ratones modificados ajustaron sus patrones de actividad más rápido que sus compañeros normales, especialmente tras los adelantos y en los machos. En otros experimentos, eliminar V1a en todo el cerebro o específicamente en el NSQ había producido un comportamiento similar de «resistencia al jet lag». Los nuevos resultados sugieren por tanto que un grupo sorprendentemente pequeño de neuronas VIP que portan receptores V1a puede tener una influencia desproporcionada sobre cuán rígido o flexible es el reloj en su conjunto.
Qué significa esto para nuestra percepción del tiempo
En términos cotidianos, este estudio muestra que dentro del reloj central del cerebro, las neuronas productoras de AVP actúan como cronometradores en un nivel superior, enviando señales a través de receptores V1a a un conjunto selecto de neuronas VIP en el nivel inferior. Esas pocas células VIP ayudan a que toda la red resista cambios bruscos en el ciclo luz–oscuridad, ralentizando la velocidad con la que el reloj se reajusta tras un cambio. Eliminar su receptor sensible a AVP hace que el sistema sea más proclive a desplazarse, facilitando en ratones ajustes similares al jet lag. Al trazar esta diversidad oculta entre las neuronas del reloj, el trabajo ofrece un diagrama de cableado más detallado sobre cómo se estabiliza nuestro sentido interno del tiempo—y sugiere que modificar selectivamente vías similares en humanos podría algún día ayudar a manejar el jet lag u otros trastornos rítmicos.
Cita: Zhou, H., Moriyasu, D., Hsiao, SW. et al. Heterogeneity between VIP and GRP neurons underlies AVP receptor signaling in the mouse suprachiasmatic nucleus. Commun Biol 9, 414 (2026). https://doi.org/10.1038/s42003-026-09694-9
Palabras clave: reloj circadiano, núcleo supraquiasmático, señalización de vasopresina, neuronas VIP, jet lag