Clear Sky Science · es
Base estructural del reconocimiento del receptor de murciélagos por SARS-CoV-2 y coronavirus similares a SARS2 de murciélagos
Por qué sigue importando esta historia murciélago–virus
La pandemia de COVID-19 comenzó hace más de seis años, pero los científicos siguen recomponiendo cómo el virus que la causa, SARS-CoV-2, se volvió tan eficaz infectando a las personas. Un rompecabezas central es cómo este virus, y sus parientes cercanos hallados en murciélagos, se enganchan a una proteína llamada ACE2 en la superficie celular: un primer y crucial paso para la infección. Comprender estas interacciones microscópicas de llave y cerradura puede aclarar de dónde provino el virus, cómo se adaptó y qué podría ocurrir si virus relacionados saltan a humanos en el futuro. 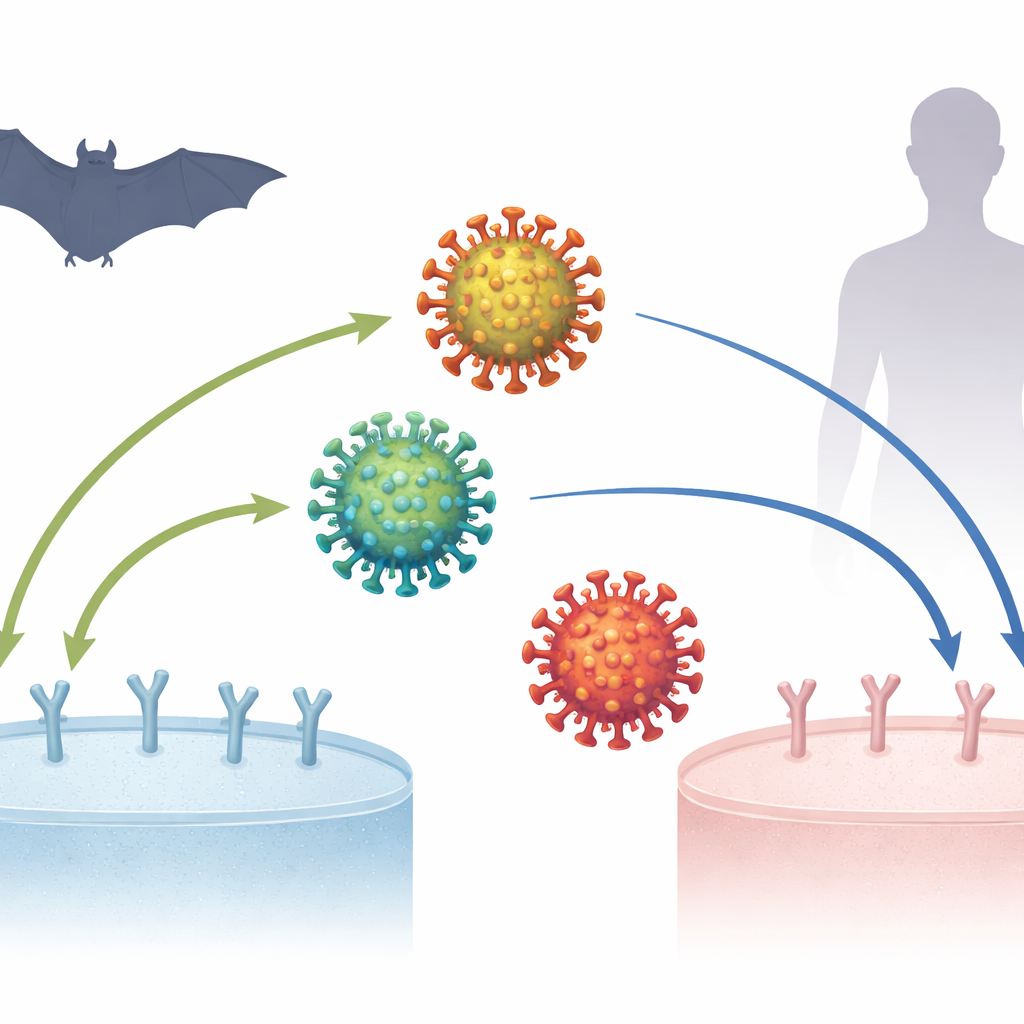
Mirando el apretón viral
El estudio se centra en la proteína spike, la estructura con forma de corona en la superficie viral que agarra ACE2. Una pequeña región de la spike, el dominio de unión al receptor (RBD), actúa como una punta del dedo que sujeta el “pomo” ACE2. Trabajos previos mostraron que cuando los coronavirus saltan entre especies —por ejemplo, de murciélagos a civetas y luego a humanos— el RBD a menudo acumula mutaciones que mejoran su agarre del ACE2 del nuevo hospedador. Pero SARS-CoV-2 planteó un enigma: su forma original ya se unía muy bien al ACE2 humano, incluso antes de que hubiese mucho tiempo para la adaptación, y algunos virus de murciélagos relacionados con SARS-CoV-2 parecían unirse al ACE2 humano mejor que al ACE2 de murciélago. Esto llevó a algunos a preguntarse si SARS-CoV-2 podría ser una excepción a las reglas evolutivas habituales.
Poniendo a prueba receptores de murciélago y humanos
Para explorar este misterio, los investigadores examinaron dos coronavirus de murciélagos estrechamente relacionados con SARS-CoV-2, conocidos como BANAL-52 y BANAL-236. Compararon cuán fuertemente los RBD de estos virus y de SARS-CoV-2 se unían al ACE2 de humanos y de varias especies de murciélagos. Usando ensayos celulares de unión, mediciones biosensoras de alta precisión y pruebas de infección con “pseudovirus” inocuos, encontraron un patrón claro. El RBD de BANAL-52 se unió con mayor fuerza al ACE2 de una especie de murciélago, Rhinolophus sinicus, y algo menos al ACE2 humano. En contraste, el RBD de SARS-CoV-2 mostró una preferencia modesta por el ACE2 humano frente al ACE2 de murciélago. En conjunto, el RBD de BANAL-52 agarró tanto a los receptores de murciélago como a los humanos con más firmeza que el de SARS-CoV-2, pero estaba más finamente ajustado a ese ACE2 de murciélago en particular. 
Cómo un ajuste a escala atómica inclina la balanza
El equipo recurrió luego a la cristalografía de rayos X, que revela estructuras a nivel atómico, para ver exactamente cómo el “dedo” viral y el “pomo” ACE2 se tocan. Se centraron en dos posiciones clave: una en el RBD viral (llamada residuo 498) y otra en ACE2 (residuo 41). En BANAL-52, tanto el sitio viral como el del ACE2 de murciélago usan el mismo bloque constituyente, la histidina, lo que permite una interacción muy ceñida y apilada —como dos monedas— y además forma un enlace de hidrógeno. En el ACE2 humano, ese mismo puesto contiene un bloque relacionado pero levemente distinto, la tirosina, que sigue apilándose bien con la histidina de BANAL-52 pero carece del enlace de hidrógeno extra. SARS-CoV-2, en cambio, usa glutamina en esa posición viral, que no puede apilarse de la misma manera, lo que resulta en una unión más débil tanto al ACE2 de murciélago como al humano. Al intercambiar deliberadamente estos aminoácidos en el ACE2 de murciélago, los investigadores confirmaron que fortalecer o debilitar este único punto de contacto podía invertir cuál virus o hospedador se favorecía.
Por qué el ACE2 humano es una entrada tan acogedora
Más allá de este contacto único, los autores preguntaron por qué el ACE2 humano en general es una puerta de entrada tan eficiente para los coronavirus. Comparando ACE2 de murciélago y humano lado a lado, identificaron varias características específicas humanas que mejoran el apretón viral. Dos posiciones en el ACE2 humano, que contienen los aminoácidos histidina (en la posición 34) y metionina (en la posición 82), crean enlaces de hidrógeno más fuertes y parches hidrofóbicos que ayudan al RBD viral a asentarse con mayor firmeza. Otro residuo humano, treonina en la posición 27, en realidad debilita un poco la unión respecto a la versión de murciélago, pero en conjunto los contactos favorables adicionales se imponen. Estos detalles concuerdan con trabajos previos que muestran que el ACE2 humano tiene múltiples “puntos calientes” que lo hacen naturalmente un receptor atractivo para una amplia gama de coronavirus.
Reenmarcando la historia de origen
Con todos los datos juntos, el estudio sostiene que SARS-CoV-2 y sus parientes de murciélagos siguen el guion evolutivo habitual. La spike de BANAL-52 parece estar mejor adaptada al ACE2 de ciertas especies de murciélagos, aunque también es compatible con el ACE2 humano. La spike de SARS-CoV-2, a su vez, está mejor afinada para el ACE2 humano que para el de murciélago, ayudada por puntos de contacto especiales en el receptor humano. Pequeños cambios en solo unas pocas posiciones —particularmente en el residuo viral 498 y sitios vecinos— pueden cambiar la balanza de qué hospedador se favorece. Para no especialistas, la conclusión es que no hace falta invocar explicaciones exóticas: principios estructurales estándares y bien entendidos de interacción proteína–proteína son suficientes para explicar cómo estos virus reconocen células de murciélagos y humanas, y respaldan un vínculo evolutivo cercano entre SARS-CoV-2 y coronavirus de murciélagos relacionados.
Cita: Hsueh, FC., Shi, K., Aihara, H. et al. Structural basis for bat receptor recognition by SARS-CoV-2 and bat SARS2-like coronaviruses. Commun Biol 9, 398 (2026). https://doi.org/10.1038/s42003-026-09682-z
Palabras clave: Evolución de SARS-CoV-2, coronavirus de murciélagos, receptor ACE2, rango de hospedadores virales, unión de la proteína spike