Clear Sky Science · es
La proteína codificada por el virus de la peste porcina africana MGF 505–3R perjudica la inmunidad innata mediante la degradación de MyD88 mediada por ubiquitina
Por qué esto importa para la salud animal y más allá
La peste porcina africana ha devastado granjas porcinas en todo el mundo, amenazando el suministro de alimentos y provocando enormes pérdidas económicas. El virus que la causa es letal en parte porque elude los sistemas de alarma temprana del organismo. Este estudio revela cómo una proteína viral, llamada MGF 505–3R, sabotea silenciosamente un interruptor de alarma clave dentro de las células y muestra que un pequeño fragmento de esta proteína también puede convertirse en una potente herramienta antiinflamatoria en ratones.
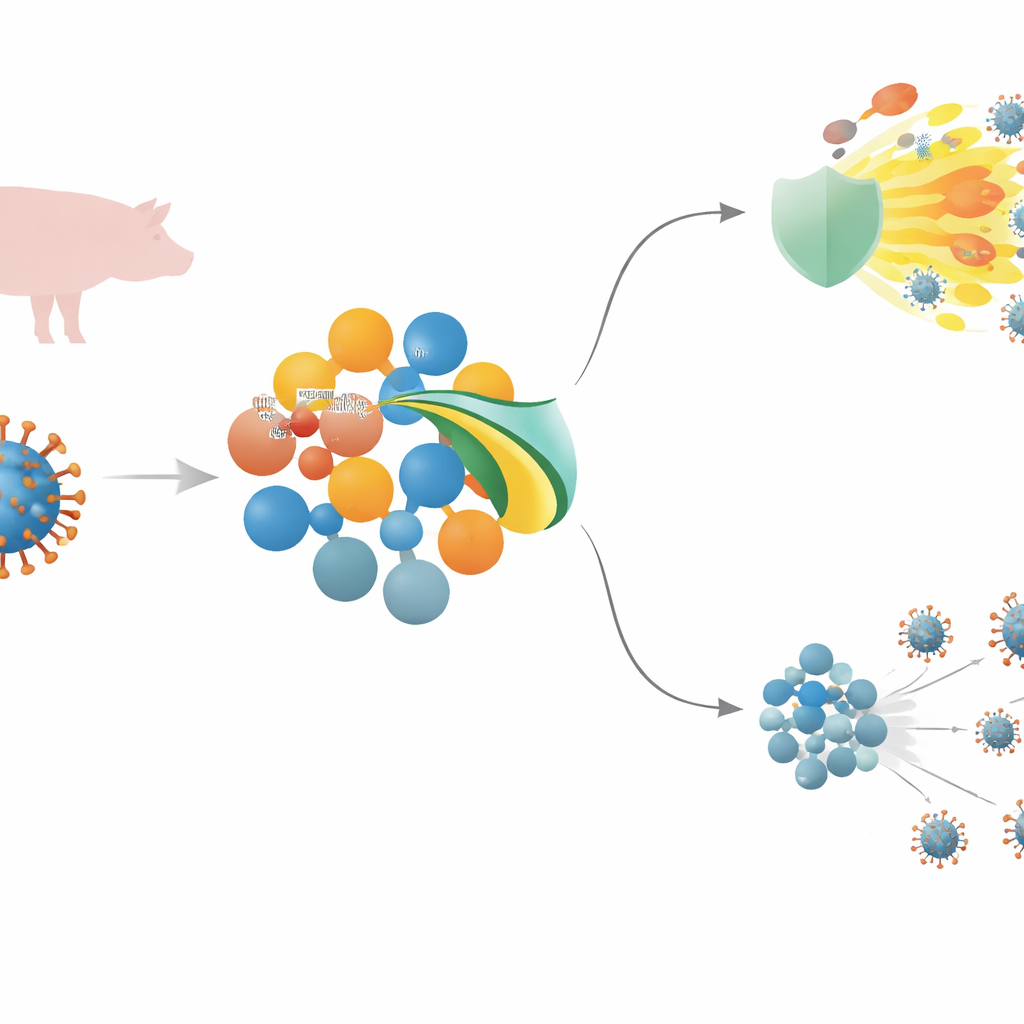
Un virus mortal para los cerdos y la primera línea de defensa del organismo
El virus de la peste porcina africana (ASFV) es un virus grande de ADN que puede matar a casi todos los cerdos infectados. Para establecerse, debe burlar la inmunidad innata —la defensa rápida y de primera línea que detecta invasores y desencadena inflamación y moléculas antivirales. En el centro de esta respuesta está una cadena de señalización que incluye sensores en la superficie celular, una proteína de relevo llamada MyD88 y un interruptor maestro conocido como NF–κB, que en conjunto impulsan la producción de mensajeros inflamatorios e interferones antivirales. El ASFV porta muchos genes que se cree interfieren con estas señales, pero de varios de ellos, incluida MGF 505–3R, no se entendían bien sus mecanismos exactos.
Cómo el virus corta los cables de la alarma inmunitaria
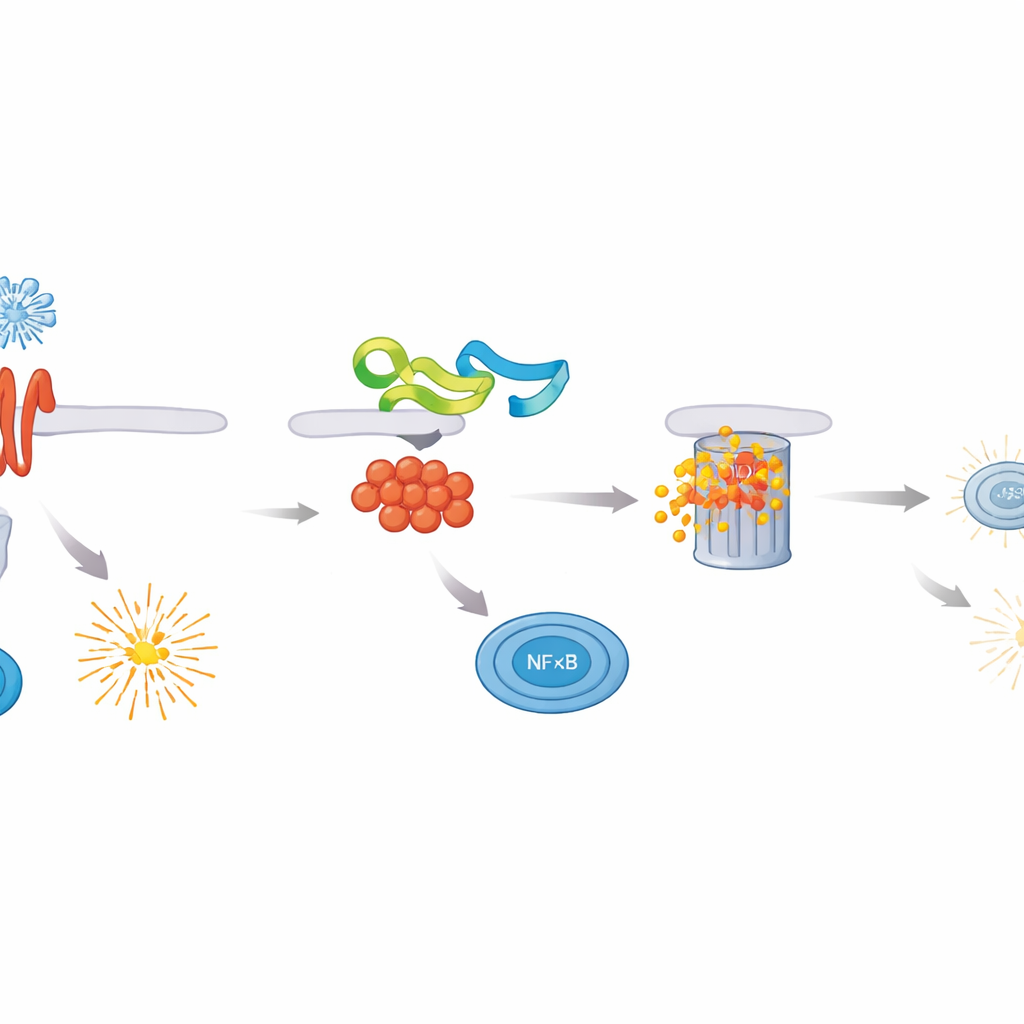
Los investigadores examinaron proteínas del ASFV para ver su capacidad de atenuar la actividad de NF–κB y encontraron que MGF 505–3R era un inhibidor particularmente potente. Cuando esta proteína viral estaba presente, las células expuestas a distintos desencadenantes inmunitarios producían muchas menos citocinas inflamatorias y niveles mucho más bajos de interferones tipo I y tipo III. Una inspección más detallada mostró que MGF 505–3R actúa directamente sobre MyD88, el adaptador central que conecta muchos sensores inmunitarios con NF–κB. MGF 505–3R se une a MyD88 y lo marca para su eliminación mediante la maquinaria celular de degradación de proteínas, usando una forma de etiquetado llamada ubiquitinación unida en K48. A medida que MyD88 se degrada, NF–κB no consigue trasladarse al núcleo ni activar genes protectores, dejando a las células más permisivas al crecimiento viral.
Acercándose a un fragmento proteico pequeño pero potente
Para identificar la parte crucial de MGF 505–3R, el equipo creó versiones acortadas de la proteína y evaluó sus efectos. Descubrieron que los aminoácidos 89–277 eran tanto necesarios como suficientes para unirse a MyD88, promover su ubiquitinación y bloquear la activación de NF–κB. Guiados por predicciones computacionales de la estructura proteica, segmentaron dos péptidos cortos de esta región. Uno de ellos, pep3R–1, destacó: redujo drásticamente la actividad de NF–κB, bloqueó la fosforilación y el tránsito nuclear de la subunidad p65 de NF–κB, y disminuyó la expresión de citocinas inflamatorias e interferones en células inmunitarias estimuladas con múltiples señales de peligro. En cultivo celular, tanto la MGF 505–3R de longitud completa como pep3R–1 no solo atenuaron la señalización antiviral, sino que también permitieron que un virus de prueba se replicara con mayor eficiencia, subrayando lo potente que es esta vía para controlar las infecciones.
Convertir un truco viral en un posible medicamento
El equipo se preguntó entonces si el péptido podría aprovecharse para calmar la inflamación dañina en lugar de favorecer a los virus. En un modelo murino de colitis inducida por un químico llamado DSS, los animales normalmente pierden peso, desarrollan diarrea sanguinolenta y muestran daños severos e invasión de células inmunitarias en el colon. Los ratones tratados con pep3R–1 evolucionaron mucho mejor: las puntuaciones de la enfermedad fueron menores, los colonos eran más largos y saludables, y el examen microscópico reveló una estructura tisular preservada con muchas menos células inflamatorias. Los niveles de moléculas inflamatorias clave como TNF–α, IL–1β, IL–6 y una enzima asociada al reclutamiento de leucocitos se redujeron tanto en el tejido colónico como en la sangre. En un experimento separado, pep3R–1 también atenuó la respuesta inflamatoria a una toxina bacteriana sistémica, lo que indica que puede moderar tanto tormentas inflamatorias locales como generalizadas.
Qué significa esto para los cerdos, las personas y futuros tratamientos
Este trabajo muestra que la proteína del ASFV MGF 505–3R ayuda al virus a prosperar al desmantelar un relevo inmune central, MyD88, cerrando así tanto las defensas inflamatorias como las de interferón. Al mismo tiempo, un pequeño fragmento de esta proteína viral, pep3R–1, puede reutilizarse para reducir de forma segura la inflamación excesiva en ratones, incluso en un modelo de enfermedad intestinal. Aunque queda mucho por hacer —como mejorar la estabilidad, la administración y las pruebas en más contextos patológicos—, el estudio revela tanto un punto débil crítico que las estrategias antivirales podrían atacar como un diseño prometedor para desarrollar nuevos fármacos antiinflamatorios basados en péptidos inspirados en la evasión inmune viral.
Cita: Liu, H., Sun, L., Wang, F. et al. African swine fever virus–encoded protein MGF 505–3R impairs innate immunity via ubiquitin–mediated degradation of MyD88. Commun Biol 9, 407 (2026). https://doi.org/10.1038/s42003-026-09681-0
Palabras clave: Peste porcina africana, inmunidad innata, NF-kappaB, MyD88, péptido antiinflamatorio