Clear Sky Science · es
SREBF2 potencia el metabolismo de lípidos y reprime las respuestas inmunitarias antitumorales en el cáncer de cuello uterino al incrementar ACAT2
Por qué el cáncer y el colesterol pertenecen a la misma historia
El cáncer de cuello uterino suele discutirse en términos de virus y vacunas, pero este estudio muestra que moléculas parecidas a grasas dentro de las células tumorales pueden inclinar silenciosamente la batalla entre el cáncer y el sistema inmune. Los investigadores descifraron cómo una enzima encargada del manejo del colesterol en las células de cáncer cervical ayuda a los tumores a crecer y a esconderse de las defensas naturales del organismo—y cómo otra proteína puede cambiar ese guion y restaurar el ataque inmunitario.
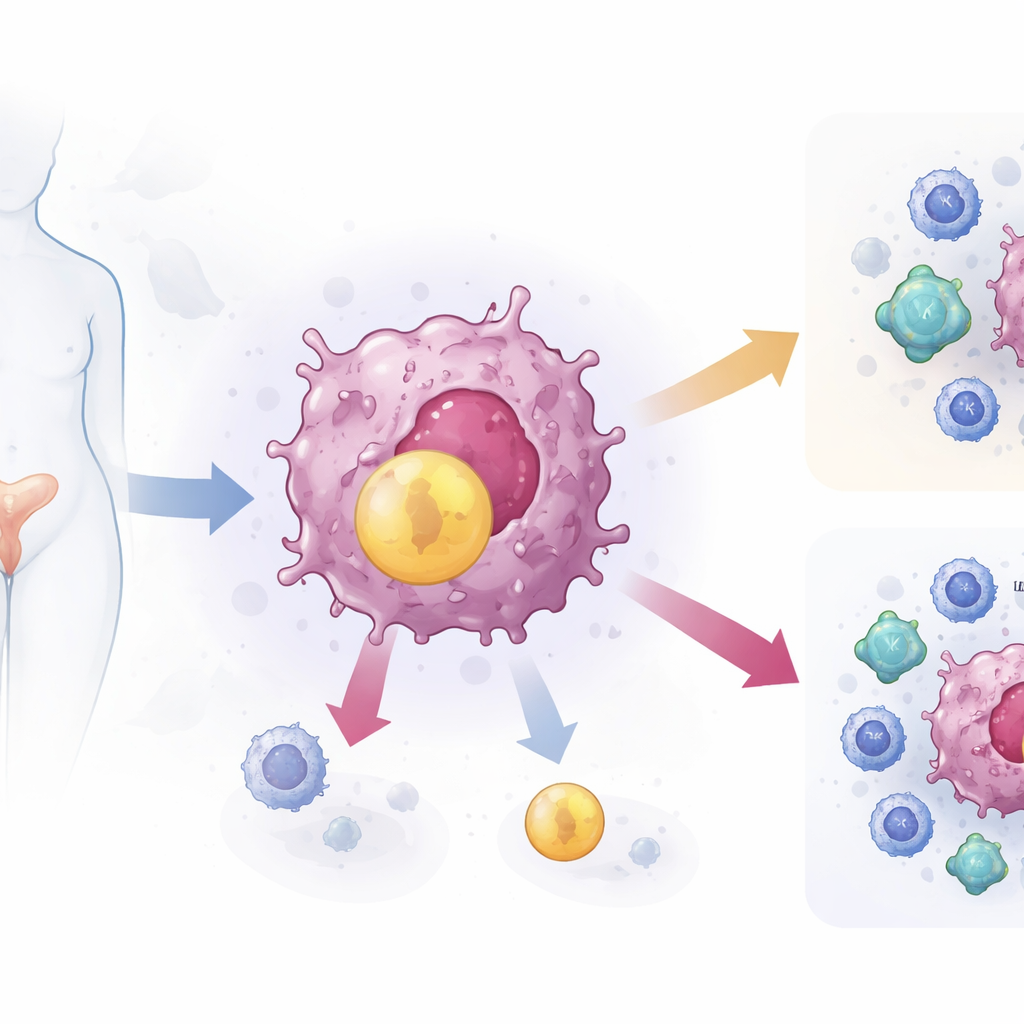
Un vínculo oculto entre las grasas y las defensas tumorales
El equipo comenzó examinando grandes bases de datos de cáncer para buscar genes implicados en el metabolismo de grasas y colesterol que estuvieran inusualmente activos en tumores cervicales. Entre miles de genes, uno destacó: ACAT2, una enzima que convierte el colesterol en formas de almacenamiento. Los pacientes cuyos tumores presentaban más ACAT2 tendían a tener una supervivencia peor y mostraban con mayor frecuencia signos de enfermedad avanzada, como afectación de los ganglios linfáticos. Al analizar muestras tumorales de 47 mujeres, encontraron que ACAT2 estaba fuertemente presente en las células cancerosas pero apenas detectable en el tejido sano circundante.
Cómo los tumores ricos en colesterol debilitan el ataque inmune
A continuación, los científicos se preguntaron si un nivel elevado de ACAT2 se vinculaba con la infiltración de células inmunitarias en los tumores. Usando herramientas computacionales y tinción fluorescente de secciones tisulares, observaron que los cánceres con alta ACAT2 tenían menos de dos células clave en la lucha contra el cáncer: células T CD8 y células NK (natural killer), especialmente en sus formas “activadas”. En experimentos en cultivo celular, las células de cáncer cervical producían menos colesterol cuando ACAT2 se silenciaba, creían más lentamente y eran más fácilmente eliminadas por células NK y T CD8. Las moléculas antitumorales liberadas por estas células inmunitarias aumentaron, mientras que añadir colesterol adicional al sistema revirtió esos beneficios, restaurando el crecimiento de las células cancerosas y su escape inmune.
Poniendo la idea a prueba en ratones
Los investigadores pasaron luego a un modelo murino de cáncer cervical. Cuando redujeron ACAT2 en células tumorales de ratón antes de implantarlas en animales, los tumores resultantes crecieron más despacio, contenían menos colesterol y mostraron mayor infiltración por células NK y T CD8 cargadas de gránulos tóxicos. Los ratones portadores de tumores con niveles reducidos de ACAT2 sobrevivieron más tiempo. Estos hallazgos sugieren que bajar el almacenamiento de colesterol en las células tumorales puede hacer que el microambiente tumoral sea más propicio para el ataque inmune y menos favorable para el crecimiento del cáncer.
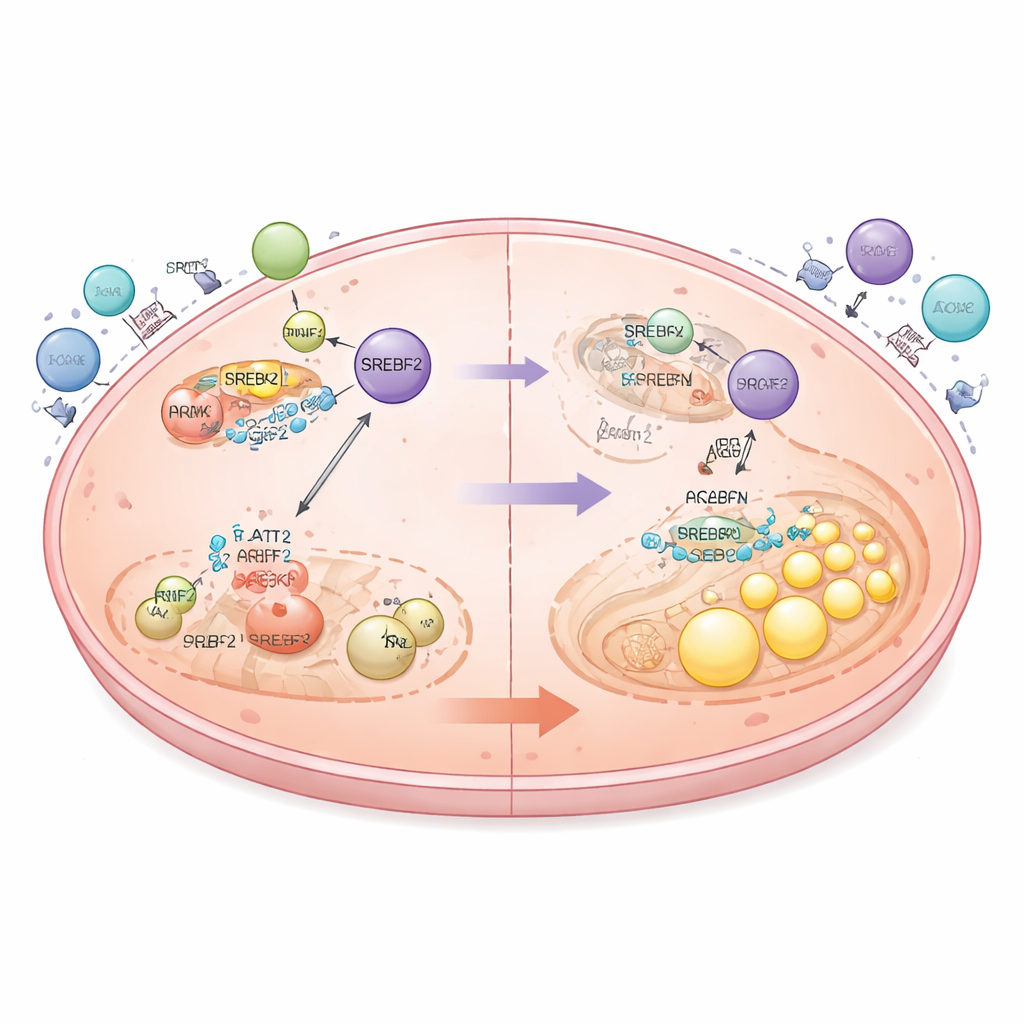
Los interruptores aguas arriba que controlan el colesterol en los tumores
Profundizando, el equipo se preguntó por qué ACAT2 era tan alto en el cáncer cervical en primer lugar. Identificaron una proteína llamada SREBF2, un regulador maestro de genes relacionados con el colesterol, como un interruptor directo que activa el gen ACAT2 en las células tumorales. Los niveles de SREBF2 estaban elevados a nivel proteico, no porque las células produjeran más ARN, sino porque su degradación estaba alterada. Otra proteína, PRKN, suele ayudar a etiquetar a SREBF2 para su eliminación. En el cáncer cervical, PRKN estaba reducido, lo que condujo a una SREBF2 más estable, mayor ACAT2 y acumulación de colesterol. Cuando se restableció PRKN en las células cancerosas, SREBF2 se degradó con mayor eficacia, los niveles de ACAT2 y colesterol disminuyeron, y se activó un proceso llamado mitofagia—limpieza de mitocondrias dañadas. Esto, a su vez, redujo señales que normalmente amortiguan las respuestas inmunitarias, como la proteína de control PD-L1 y el factor inmunosupresor TGF-β1.
Qué podría significar esto para tratamientos futuros
Juntando las piezas, el estudio describe una cadena de eventos: PRKN baja permite la acumulación de SREBF2, que potencia ACAT2, conduciendo a células cancerosas ricas en colesterol que resisten el ataque inmune y crecen con más agresividad. Interferir con esta vía—inhibiendo ACAT2, atenuando la actividad de SREBF2 o restaurando PRKN—podría hacer que los tumores cervicales sean más vulnerables a inmunoterapias existentes como los inhibidores de puntos de control o tratamientos basados en células. Para los pacientes, este trabajo sugiere que algo aparentemente tan corriente como el manejo del colesterol dentro de las células tumorales puede convertirse en una palanca útil para fortalecer las defensas propias del organismo contra el cáncer de cuello uterino.
Cita: Zhang, Y., Shao, Y., Li, X. et al. SREBF2 enhances lipid metabolism and represses anti-tumor immune responses in cervical cancer by increasing ACAT2. Commun Biol 9, 373 (2026). https://doi.org/10.1038/s42003-026-09678-9
Palabras clave: cáncer de cuello uterino, metabolismo del colesterol, evasión inmune tumoral, ACAT2, vía PRKN SREBF2