Clear Sky Science · es
Una guía práctica de las tecnologías de secuenciación de ARN unicelular dirigida
Por qué importa observar células individuales
Cada célula de tu cuerpo contiene el mismo ADN, pero distintas células se comportan de maneras muy diferentes. Lo hacen activando o desactivando genes concretos y modificando las moléculas de ARN de formas sutiles. La secuenciación moderna de ARN unicelular puede leer qué ARNs están presentes en miles de células a la vez, pero actualmente pasa por alto gran parte del mensaje. Esta revisión explica dónde las técnicas actuales pierden información y cómo se están desarrollando nuevos métodos “dirigidos” para enfocar las partes más importantes de las moléculas de ARN con fines de investigación, diagnóstico y diseño de tratamientos.
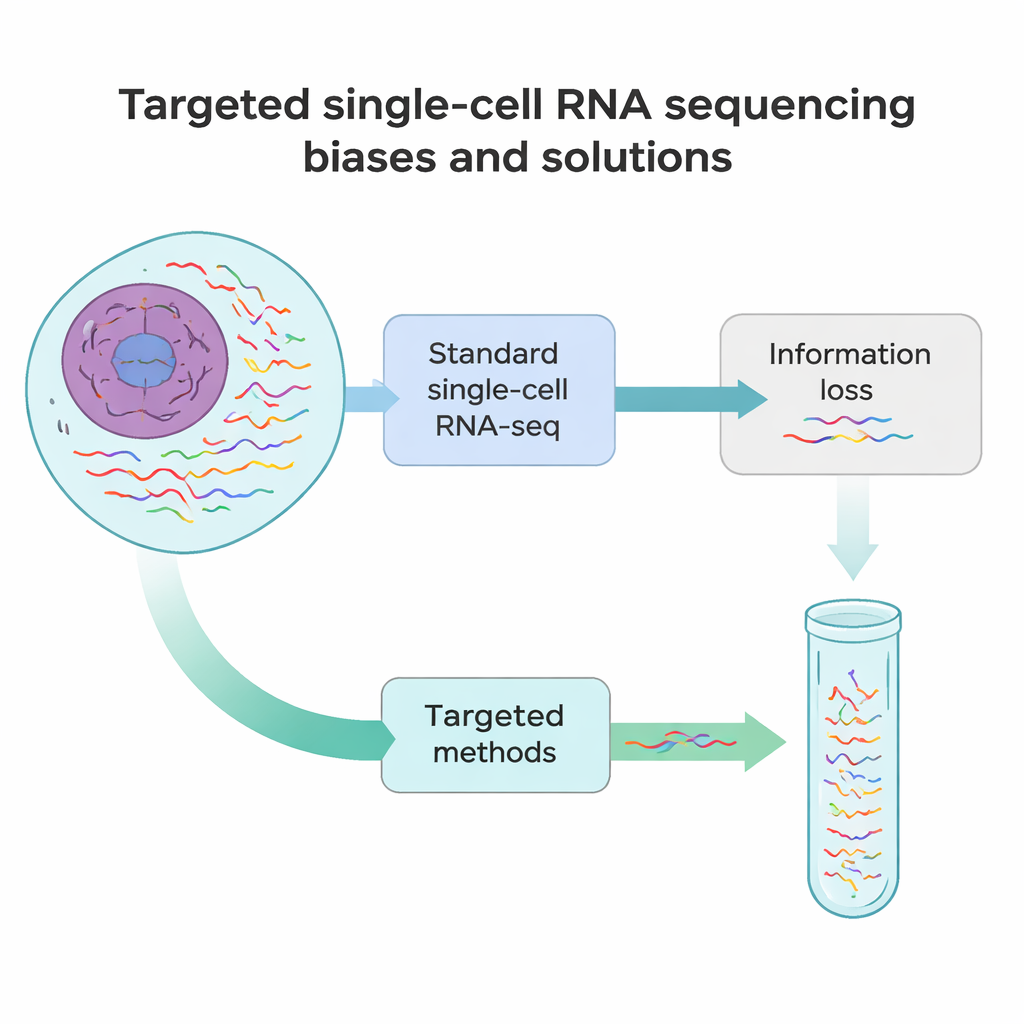
Dónde fallan los métodos actuales
La secuenciación estándar de ARN unicelular funciona un poco como tomar una instantánea rápida de cada mensaje en una célula en lugar de una película completa. En la mayoría de los experimentos, solo se detecta entre el 10 y el 40 % de todos los ARNs de una célula, y solo se leen su inicio o su extremo. Eso significa que muchos ARNs raros pero importantes —como marcadores que definen la identidad celular o variantes génicas que llevan mutaciones causantes de enfermedad— se pierden con facilidad. Además, varios pasos técnicos, desde disociar tejidos en células individuales hasta copiar ARN en ADN y amplificarlo, introducen sesgos sistemáticos. Algunos ARNs se cortan prematuramente, otros se sobrerrepresentan y otros desaparecen por completo de los datos.
Por qué importan los detalles internos del ARN
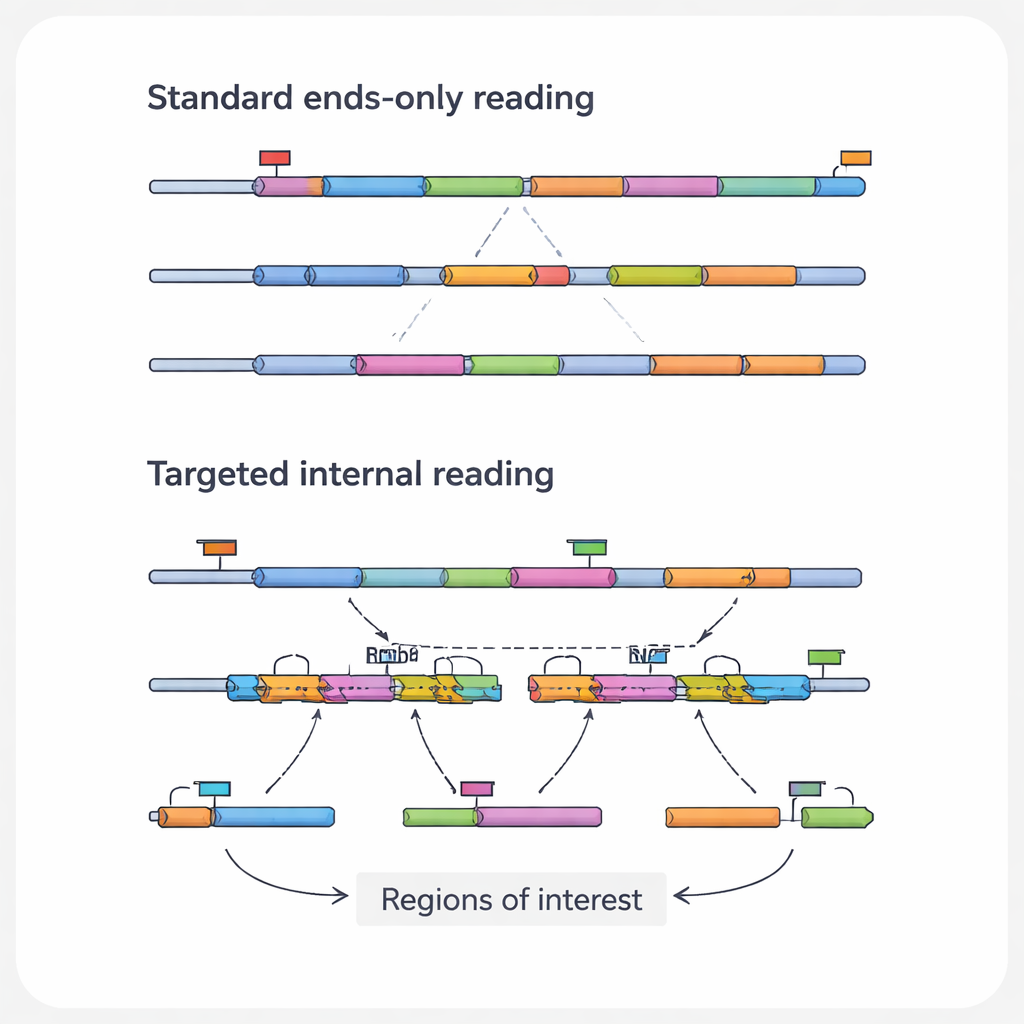
La información más relevante desde el punto de vista médico en una molécula de ARN suele hallarse en sus regiones internas, no en los extremos que ven los métodos estándar. Estas secciones internas pueden contener mutaciones puntuales que impulsan el cáncer, puntos de fusión donde dos genes se han unido anómalamente, o empalmes que generan variantes proteicas distintas a partir del mismo gen. También pueden registrar la huella de herramientas de edición genética como CRISPR. Los autores denominan estas características específicas “regiones de interés” y a los ARNs que las contienen “transcritos de interés”. Dado que las plataformas de alto rendimiento comunes leen principalmente las puntas de los ARNs, pasan rutinariamente por alto estos detalles cruciales, especialmente en transcritos largos o de baja abundancia.
Nuevas formas de dirigir el foco
Para superar estos puntos ciegos, los investigadores han desarrollado una familia de enfoques de secuenciación de ARN unicelular dirigidos. En lugar de intentar leer todos los ARNs por igual, estos métodos enriquecen deliberadamente transcritos o regiones seleccionadas. Algunas estrategias rediseñan las perlas de captura para que se unan a secuencias internas de ARN en lugar de solo a la cola, incorporando los mensajes elegidos en la biblioteca desde el primer paso. Otras añaden cebadores personalizados que comienzan la copia en un punto interno, o pasos adicionales de PCR que amplifican específicamente una lista corta de genes a partir de una biblioteca existente. Otro grupo emplea sondas de ADN que se hibridan con ARNs objetivo o sus copias y luego los recuperan, a menudo con etiquetas químicas sencillas. Cada categoría intercambia sensibilidad, número de células, número de objetivos y coste, pero todas comparten el mismo objetivo: recuperar más detalle significativo con las mismas o menos lecturas de secuenciación.
Aplicaciones desde virus hasta tumores
Estos métodos dirigidos ya están transformando varias áreas de la biología y la medicina. En infecciones, pueden finalmente capturar ARNs virales o bacterianos que carecen de las colas poli(A) que esperan los protocolos estándar, revelando en qué células hospedadoras se encuentran y cómo alteran la actividad génica del huésped. En el cáncer, la secuenciación unicelular dirigida puede identificar qué tipos celulares portan mutaciones específicas o genes de fusión y vincularlos con programas génicos alterados, ayudando a explicar por qué algunas células se vuelven resistentes a la terapia. Otros métodos se centran en el empalme alternativo, descubriendo qué tipos celulares usan qué isoformas, o en poblaciones celulares raras y marcadores sutiles que de otro modo quedarían por debajo del umbral de detección. En cribados combinados con CRISPR, una mejor captura de los ARN guía permite a los científicos vincular cada perturbación genética con su respuesta celular precisa.
Elegir la herramienta adecuada y qué seguirá
Dado que ahora existe un conjunto de herramientas dirigido y diverso, los autores proponen un árbol de decisiones para ayudar a los investigadores a elegir un método. Las preguntas clave incluyen si se necesita un perfil completo del transcriptoma, cuántos genes o regiones deben dirigirse, qué distancia tienen esas regiones respecto a los extremos del ARN y cuántas células se pueden procesar. Mirando hacia el futuro, sostienen que las mayores mejoras vendrán de perfeccionar los primeros pasos de captura, ampliar las estrategias ingeniosas basadas en sondas y combinar el direccionamiento con plataformas emergentes de lectura larga y secuenciación directa de ARN. Hasta que sea práctico leer cada ARN en cada célula de extremo a extremo, la secuenciación de ARN unicelular dirigida seguirá siendo esencial para ver las partes del mensaje celular que más importan para la biología y la enfermedad.
Cita: Moro, G., Brunner, E. & Basler, K. A practical guide to targeted single-cell RNA sequencing technologies. Commun Biol 9, 250 (2026). https://doi.org/10.1038/s42003-026-09675-y
Palabras clave: secuenciación de ARN unicelular, secuenciación dirigida, transcriptómica, mutaciones en cáncer, transcriptómica espacial