Clear Sky Science · es
Activación del receptor acoplado a proteína G codificado por citomegalovirus UL33 mediante un péptido N‑terminal innato
Cómo un virus común reprograma nuestras células
El citomegalovirus humano (HCMV) infecta silenciosamente a la mayoría de las personas en el mundo y por lo general pasa desapercibido. Sin embargo, en recién nacidos, receptores de trasplantes y otras personas con sistemas inmunitarios debilitados, puede causar enfermedades graves. Este estudio revela, con detalle molecular, cómo una proteína viral llamada UL33 actúa como un interruptor incorporado que empuja constantemente a las células infectadas a favorecer al virus. Entender este interruptor oculto ayuda a explicar cómo el HCMV persiste de por vida y señala nuevas maneras de desactivarlo sin dañar la señalización celular normal.
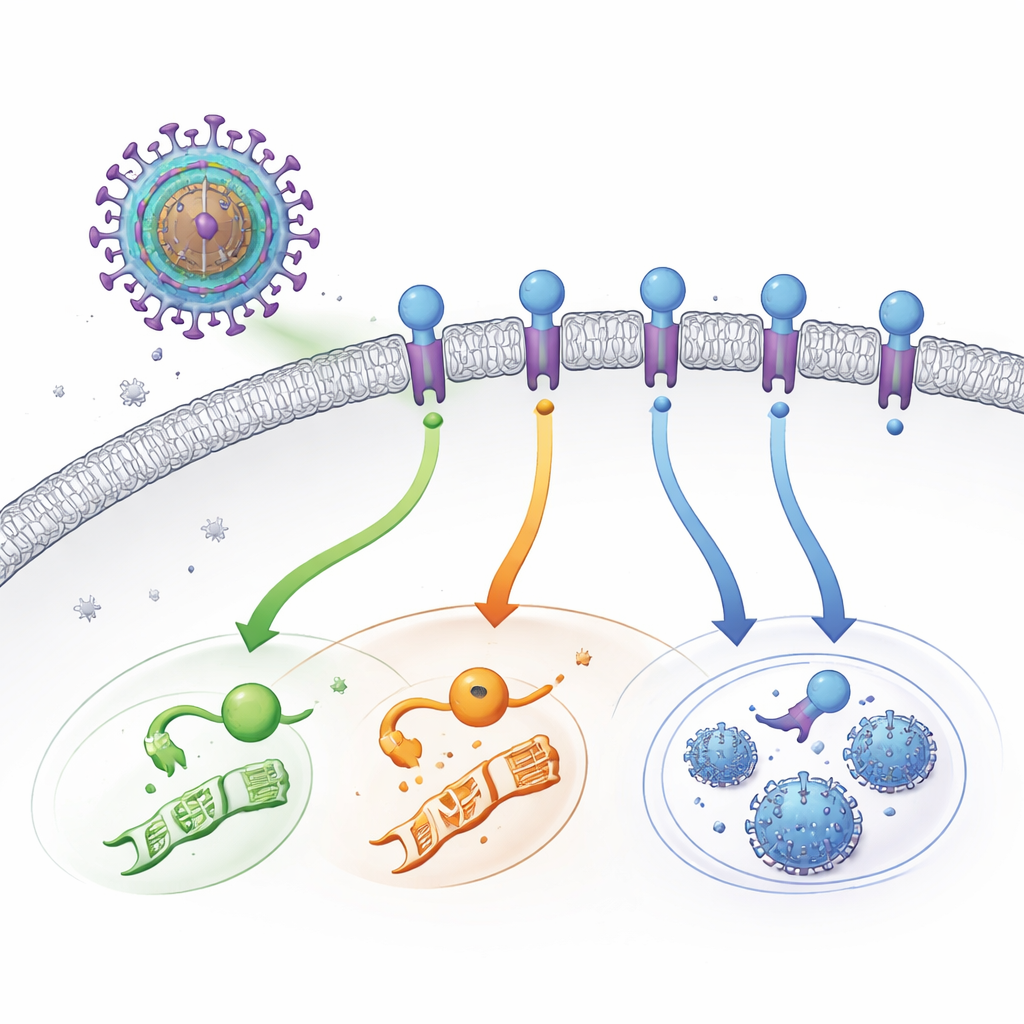
Un interruptor viral sigiloso en la superficie celular
El HCMV lleva sus propias versiones de receptores en la superficie celular: proteínas que normalmente detectan hormonas o señales inmunitarias. UL33 es uno de estos receptores virales. A diferencia de los receptores típicos, que esperan una señal externa, UL33 está “siempre activo”. Una vez inserto en la membrana externa de una célula infectada, puede conectarse a varias de las principales vías de comunicación celular a la vez. Estas vías controlan procesos como la actividad génica, el metabolismo y la decisión de permanecer latente o producir más virus. Durante años, los científicos sabían que UL33 estaba activo pero no conocían qué lo activaba, especialmente porque nunca se había identificado una molécula externa activadora (ligando).
Un iniciador propio: el receptor que trae su propia llave
Empleando microscopía crioelectrónica avanzada, los autores capturaron instantáneas tridimensionales de UL33 unido a uno de los socios de señalización de la célula, una proteína G llamada Gs. Las imágenes muestran que el extremo muy inicial de la proteína UL33—su corta cola N‑terminal—se pliega hacia atrás dentro de una cavidad del propio receptor, como una llave que se deja permanentemente en la cerradura. Esta cola “anclada” se aloja en un pequeño bolsillo lateral que, en receptores humanos relacionados, normalmente recibiría parte de una proteína de señalización inmunitaria llamada quimiocina. Al ocupar este bolsillo desde el inicio, UL33 evita que las quimiocinas externas se unan en absoluto, lo que explica por qué se comporta como un receptor “huérfano” que no responde a los mensajeros normales del hospedador.
Átomos cruciales en el interruptor viral
Para confirmar que esta cola incorporada es realmente el disparador, el equipo alteró sistemáticamente bloques individuales de construcción de UL33 en células humanas. Se centraron en los primeros aminoácidos de la cola y en los puntos coincidentes dentro del bolsillo que la sujetan. Cuando intercambiaron estos residuos clave por otros más neutrales o eliminaron uno de ellos por completo, la capacidad de UL33 para señalizar caía hasta casi cero, aunque los receptores alterados seguían alcanzando la superficie celular en cantidades normales. En otras palabras, la proteína estaba presente pero muda. Esto demuestra que la cola no es solo una decoración estructural; es la pieza esencial autoactivadora que mantiene a UL33 encendido.
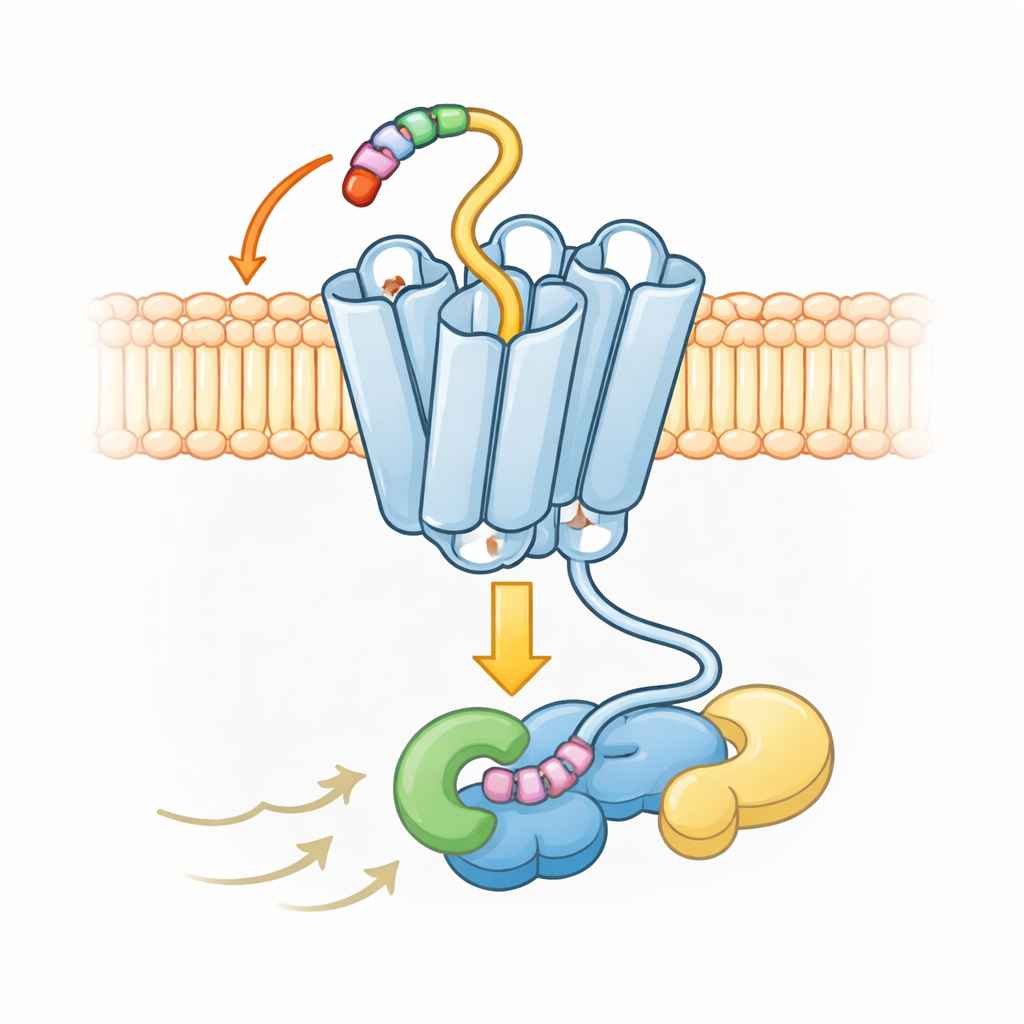
Una forma inusual para una señalización amplia pero controlada
Los mapas estructurales también revelan que UL33 adopta una conformación activa algo distinta respecto a los receptores humanos típicos. En la mayoría de los receptores de esta familia, una de las siete hélices cercanas al interior celular se desplaza mucho hacia afuera al activarse, abriendo una cavidad amplia para que las proteínas G se acoplen. En UL33, esa hélice permanece mucho más cerca del centro, creando un ajuste más ceñido. A pesar de ello, UL33 puede aun así interactuar con varios tipos de proteínas G—Gs, Gq y Gi—mediante contactos precisos con la punta de la proteína G que encaja en el receptor. Estos contactos favorecen a algunas proteínas G y excluyen a otras, como el grupo G12/13, lo que permite al virus sesgar las respuestas de la célula sin desencadenar una señalización descontrolada.
Nuevas vulnerabilidades para un virus antiguo
Combinando imágenes estructurales con pruebas funcionales, el estudio dibuja una imagen clara: UL33 es un receptor viral autoarrancable cuya propia cola actúa como un activador permanentemente unido. Este diseño permite al HCMV afinar de forma suave pero persistente la señalización de las células del hospedador para apoyar la replicación viral y la reactivación, en especial potenciando vías que activan genes virales. Al mismo tiempo, el trabajo expone puntos débiles que los fármacos podrían explotar, como un túnel estrecho que conduce al bolsillo donde se une la cola. Moléculas diseñadas para clavarse en esa región o desalojar la cola podrían silenciar la actividad de UL33 y reducir el daño viral, preservando los receptores normales del organismo. Para pacientes en riesgo por HCMV, dirigirse a este “interruptor maestro” viral podría algún día ofrecer una forma más precisa de mantener el virus bajo control.
Cita: Drzazga, A.K., Suzuki, S., Wouters, C. et al. Activation of cytomegalovirus-encoded G protein-coupled receptor UL33 by an innate N-terminal peptide. Commun Biol 9, 415 (2026). https://doi.org/10.1038/s42003-026-09660-5
Palabras clave: citomegalovirus, GPCR viral, señalización celular, estructura cryo-EM, diana farmacológica