Clear Sky Science · es
Investigando las respuestas de biofilm de Salmonella al tratamiento con antibióticos mediante espectroscopía fototérmica infrarroja óptica
Por qué importan las ciudades pegajosas de microbios
Muchas bacterias causantes de enfermedades prefieren vivir en comunidades densamente empaquetadas llamadas biofilms, donde las células se adhieren entre sí y a superficies dentro del cuerpo o en dispositivos médicos. Dentro de estas “ciudades” viscosas, los microbios pueden resistir antibióticos que normalmente los matarían. Este estudio presenta una nueva forma de mirar en detalle los biofilms, revelando qué células están activamente creciendo y cómo reaccionan cuando se añaden fármacos potentes. Comprender estos patrones de actividad invisibles podría ayudar a los médicos a diseñar tratamientos que finalmente rompan las defensas obstinadas de los biofilms.
Vida oculta dentro de las ciudades bacterianas
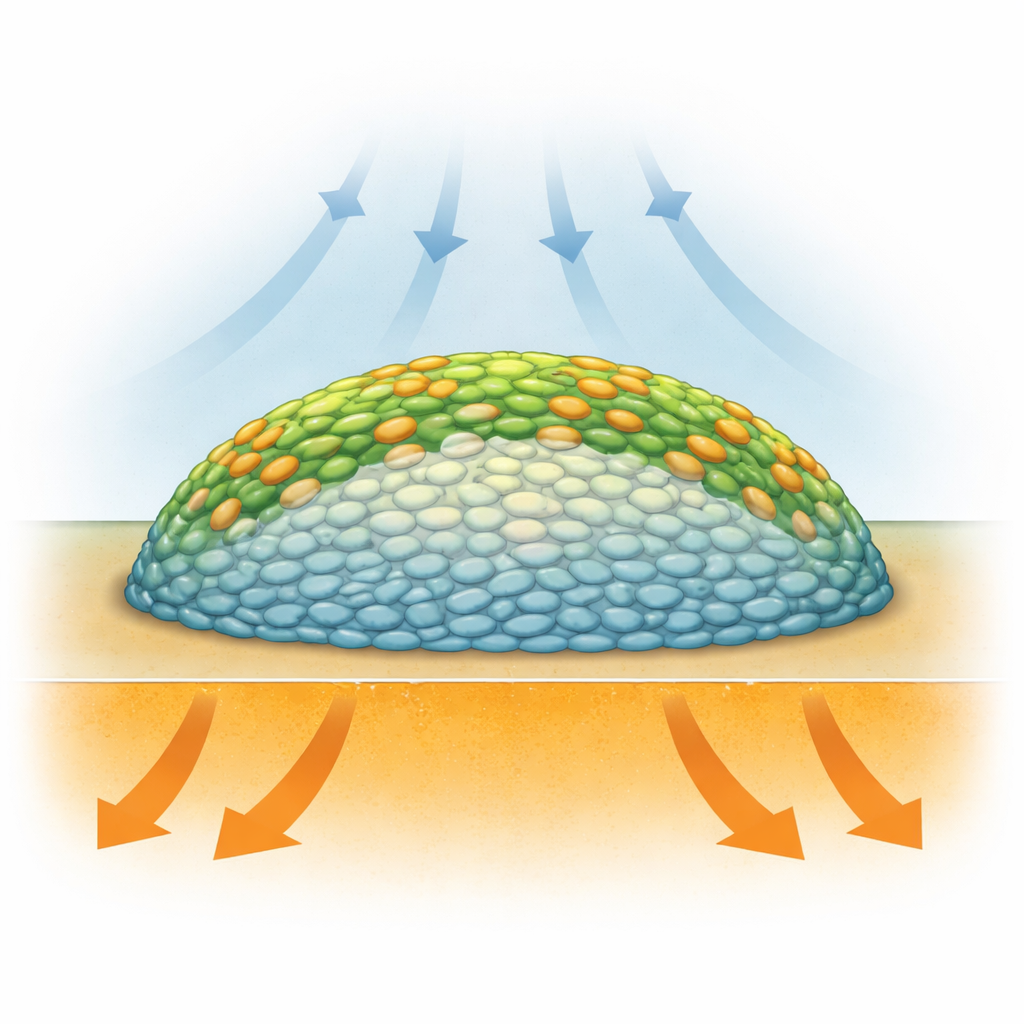
Los biofilms no son solo agregados aleatorios de gérmenes: son estructuras en capas donde las bacterias viven en condiciones muy diferentes según su ubicación. Las células en el exterior tienen mayor acceso a oxígeno del aire, mientras que las enterradas en el centro se quedan sin oxígeno y pueden ralentizarse o entrar en un estado de latencia. Métodos previos como la microscopía de fluorescencia podían mostrar la estructura, pero a menudo requerían colorantes añadidos o etiquetas genéticas que podrían alterar la biología, y no medían directamente qué estaban haciendo las células a nivel químico. Los investigadores necesitaban una forma de “ver” la química de los biofilms vivos, capa por capa, sin desmenuzarlos ni modificarlos en gran medida.
Ver la química con luz invisible
El equipo recurrió a una técnica llamada espectroscopía fototérmica infrarroja óptica (O-PTIR), que utiliza pulsos de luz infrarroja invisible y un láser visible para detectar vibraciones diminutas en las moléculas. Estas vibraciones actúan como huellas dactilares de componentes celulares clave, como proteínas, lípidos y ADN. Para rastrear el metabolismo—el uso activo de nutrientes—alimentaron biofilms de Salmonella Typhimurium con una forma especial de azúcar en la que los átomos de carbono eran ligeramente más pesados de lo habitual (un isótopo estable conocido como carbono-13). Cuando las células están ocupadas creciendo y fabricando nuevas proteínas, incorporan estos átomos más pesados en sus propias estructuras, lo que provoca desplazamientos sutiles pero detectables en la señal infrarroja. Mediante criocorte del biofilm y el escaneo de secciones transversales finas, los investigadores produjeron mapas químicos que mostraban dónde en el biofilm se había incorporado este carbono pesado.
Anillos de actividad y núcleos tranquilos
La imagen infrarroja de biofilms de Salmonella no tratados reveló un patrón llamativo: las regiones exteriores y las capas superficiales mostraron una fuerte incorporación del carbono pesado, mientras que un gran núcleo central mostró muy poco. En otras palabras, el biofilm se comportó como un anillo de células activas rodeando un interior silencioso. El análisis estadístico de los espectros infrarrojos confirmó que las señales relacionadas con vibraciones de proteínas se desplazaban más en las capas exteriores que en el centro, lo que indica una mayor producción de proteínas en los bordes. Estos hallazgos respaldan la idea de que la disponibilidad de oxígeno, que es mayor cerca de la superficie, es el principal impulsor de las “zonas calientes” metabólicas en este modelo de colonia, aunque los nutrientes fluyan desde abajo. El estudio proporcionó una de las vistas más claras y de mayor resolución hasta ahora sobre cómo se estratifica el metabolismo dentro de un biofilm.
Cómo distintos antibióticos remodelan la actividad del biofilm
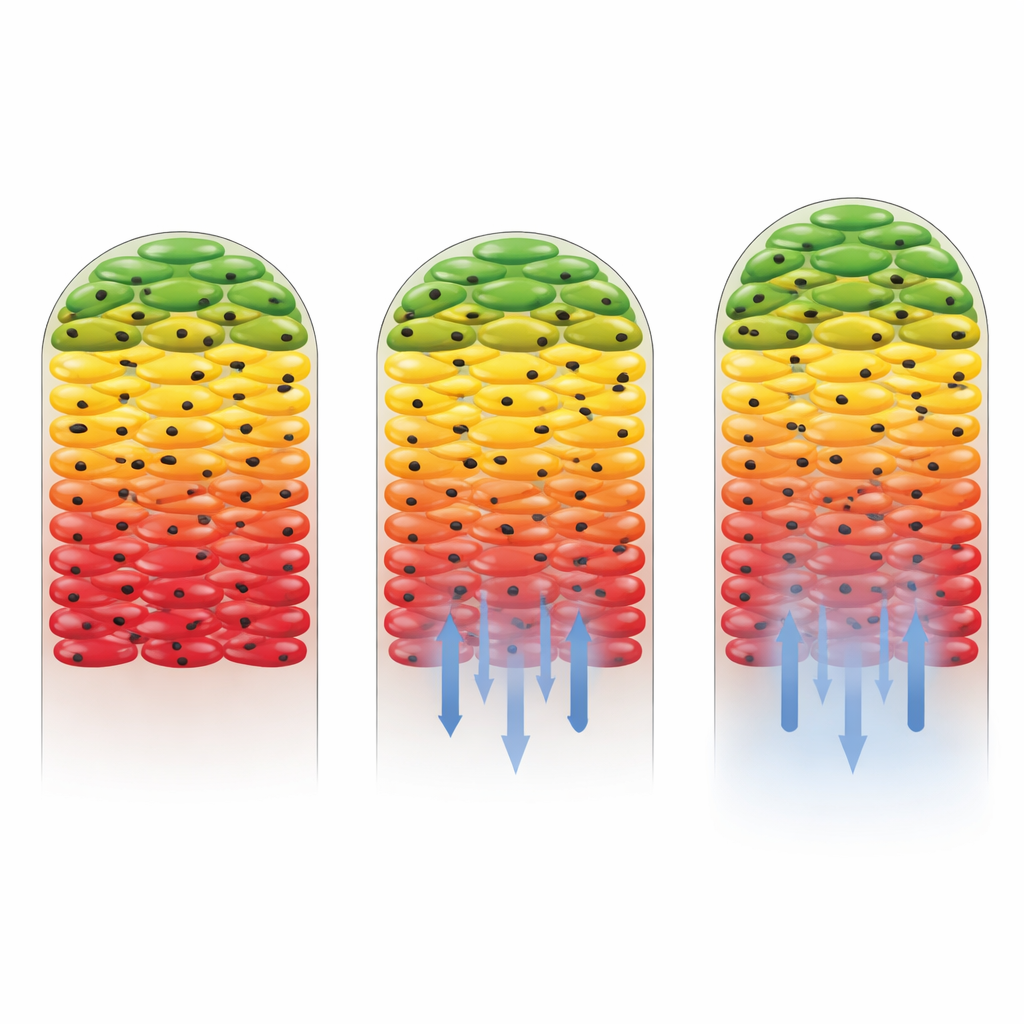
Los investigadores preguntaron entonces qué ocurre cuando se introducen antibióticos. Usaron dos fármacos: kanamicina, a la que la cepa de Salmonella es sensible, y gentamicina, a la que la cepa había sido diseñada para ser en gran medida no susceptible. Cuando estaba presente la gentamicina, el patrón general de capas externas activas y un núcleo silencioso apenas cambió, lo que muestra que las células resistentes continuaron creciendo e incorporando carbono pesado en gran parte del biofilm. En contraste, la kanamicina redujo drásticamente la actividad metabólica, especialmente cerca de la base del biofilm donde la concentración del fármaco era mayor. Solo una delgada banda de células más alejada de la fuente del antibiótico mostró signos de captación de carbono. Esto reveló no solo que el fármaco era efectivo, sino también que la propia estructura del biofilm ayudaba a proteger a algunas células al debilitar el antibiótico a medida que éste se difundía hacia el interior.
Nuevas ventanas para tratar infecciones difíciles
Desde una perspectiva divulgativa, el mensaje clave es que este trabajo ofrece un potente “microscopio químico” para observar cómo las comunidades bacterianas viven y sobreviven al tratamiento en tres dimensiones. Al combinar un método de imagen infrarroja no destructivo con una forma segura de carbono pesado, los investigadores pudieron localizar dónde las bacterias estaban activamente creciendo y cómo esa actividad cambiaba bajo distintos antibióticos. Sus resultados confirman que los biofilms albergan una mezcla de células activas y casi dormidas, y que incluso los fármacos efectivos pueden verse amortiguados por la barrera física del biofilm. En el futuro, este enfoque podría usarse para probar nuevas terapias, explorar cómo distintas especies cooperan o comparten resistencia dentro de biofilms mixtos y, en última instancia, ayudar a diseñar estrategias más inteligentes para eliminar infecciones persistentes.
Cita: Smaje, D., Zhu, X., Hinton, J.C.D. et al. Investigating Salmonella biofilm responses to antibiotic treatment using optical photothermal infrared spectroscopy. Commun Biol 9, 405 (2026). https://doi.org/10.1038/s42003-026-09655-2
Palabras clave: biofilms, Salmonella, resistencia a antibióticos, imagen infrarroja, sondeo con isótopos estables