Clear Sky Science · es
Selección de modelos en la investigación preclínica de terapias con ácidos nucleicos
Convertir genes en medicamentos
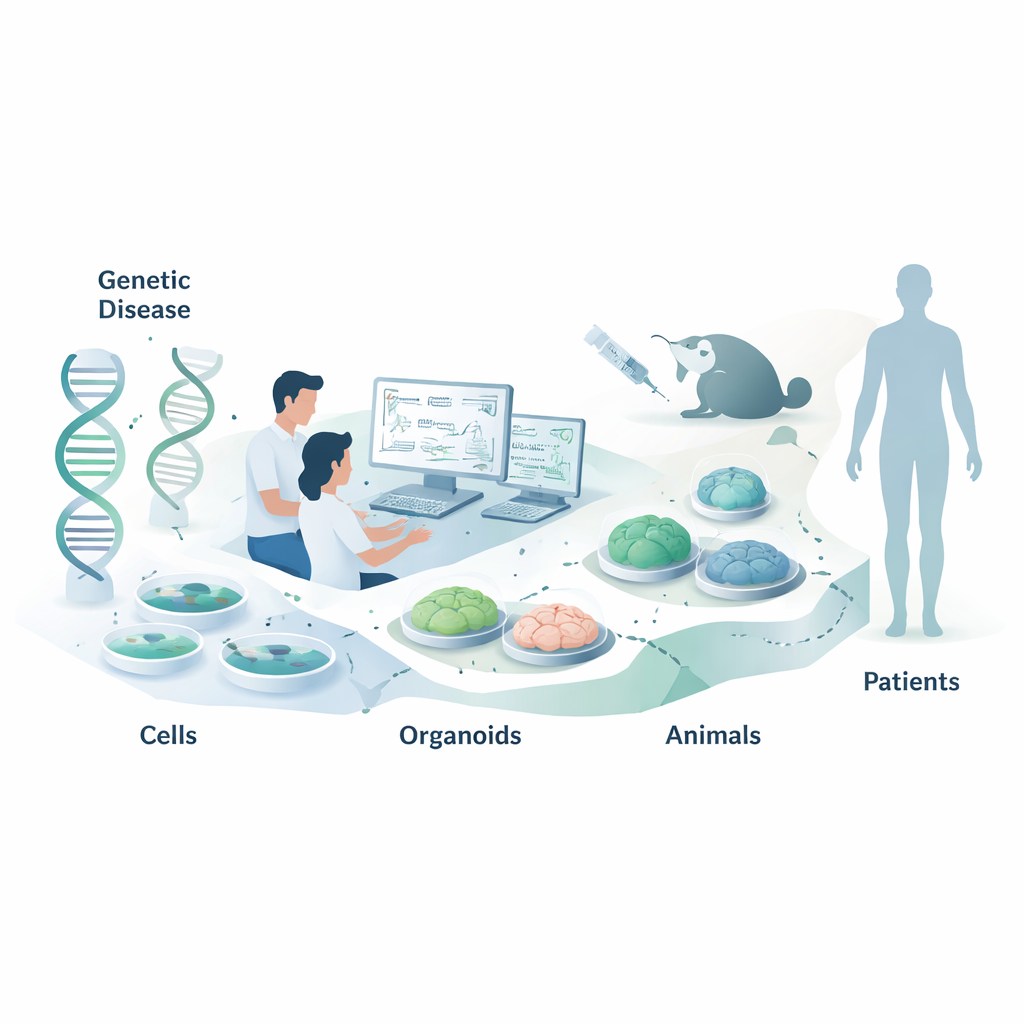
Las terapias con ácidos nucleicos son un tipo nuevo de medicamento que no actúa bloqueando proteínas, como hacen la mayoría de los fármacos, sino interviniendo un paso antes, a nivel de nuestros mensajes genéticos. Esta revisión explica cómo los científicos eligen los modelos de laboratorio y animales adecuados para probar estos fármacos dirigidos al ARN antes de que lleguen a los pacientes. A un lector no especializado le puede interesar porque una buena elección de modelos puede traducirse en tratamientos para enfermedades genéticas más rápidos, seguros y eficaces, incluidas enfermedades infantiles raras y afecciones más comunes como las cardiopatías.
¿Qué hace diferentes a estos medicamentos genéticos?
Las terapias con ácidos nucleicos (TAN) incluyen cadenas cortas llamadas oligonucleótidos antisentido (ASO) y pequeños ARN interferentes (siRNA). En lugar de depender de la forma y la química de dianas proteicas, estos fármacos reconocen sus objetivos mediante reglas de apareamiento de bases—el mismo emparejamiento A‑T y G‑C que subyace al ADN. Eso los hace programables: una vez conocida la secuencia de ARN que se quiere modificar, a menudo se pueden diseñar muchos candidatos con rapidez sin años de química tradicional. Lo difícil deja de ser «¿podemos fabricar un compuesto activo?» y pasa a ser «¿cómo medimos si realmente funciona en un entorno biológico realista?» Porque incluso una diferencia de una sola letra en la secuencia puede determinar la actividad, elegir los sistemas de prueba adecuados se vuelve crítico.
Pruebas celulares sencillas: rápidas pero incompletas
La primera parada para la mayoría de las TAN es un panel de líneas celulares relativamente fáciles de cultivar, como HeLa o HEK293, que ya expresan el ARN diana. Los investigadores añaden grandes bibliotecas de ASO o siRNA candidatos y miden cuánto disminuye el ARN diana y su proteína, usando técnicas como PCR y Western blot. También pueden trabajar con células derivadas de pacientes, que capturan mejor el trasfondo genético individual y permiten probar fármacos «selectivos por alelo» que silencian solo la copia defectuosa de un gen. Cuando el gen natural no se expresa convenientemente, los científicos a veces introducen minigenes artificiales o plásmidos reporteros que brillan cuando el ARN se corta o se empalma correctamente. Estos sistemas son potentes para comparar muchos diseños con rapidez, pero pueden pasar por alto detalles importantes, como la estructura natural del ARN o el procesamiento específico de tipos celulares, por lo que los resultados deben confirmarse en contextos más realistas.
De correcciones moleculares al comportamiento real de las células
Muchas TAN no buscan solo destruir ARN defectuosos sino repararlos alterando el empalme, el proceso que une los fragmentos del mensaje génico. Los ASO cuidadosamente diseñados pueden hacer que las células omitan un exón perjudicial, restauren una parte faltante o eviten la inserción de un «pseudo‑exón» que rompa el código. Para ver si esos cambios realmente mejoran la función celular, los investigadores van más allá de lecturas simples de niveles de ARN y proteína. En células derivadas de pacientes, prueban si vuelve la actividad enzimática, si se normaliza el transporte iónico en células pulmonares o si las vías de señalización en células inmunes responden correctamente. Cada vez más usan organoides tridimensionales—miniórganos cultivados a partir de células madre de pacientes—que pueden imitar latidos cardíacos, actividad de redes cerebrales u otros comportamientos complejos. Estos modelos 3D están más cerca de órganos reales pero son más difíciles, lentos y caros de manejar, por lo que los equipos deben equilibrar realismo y rendimiento.
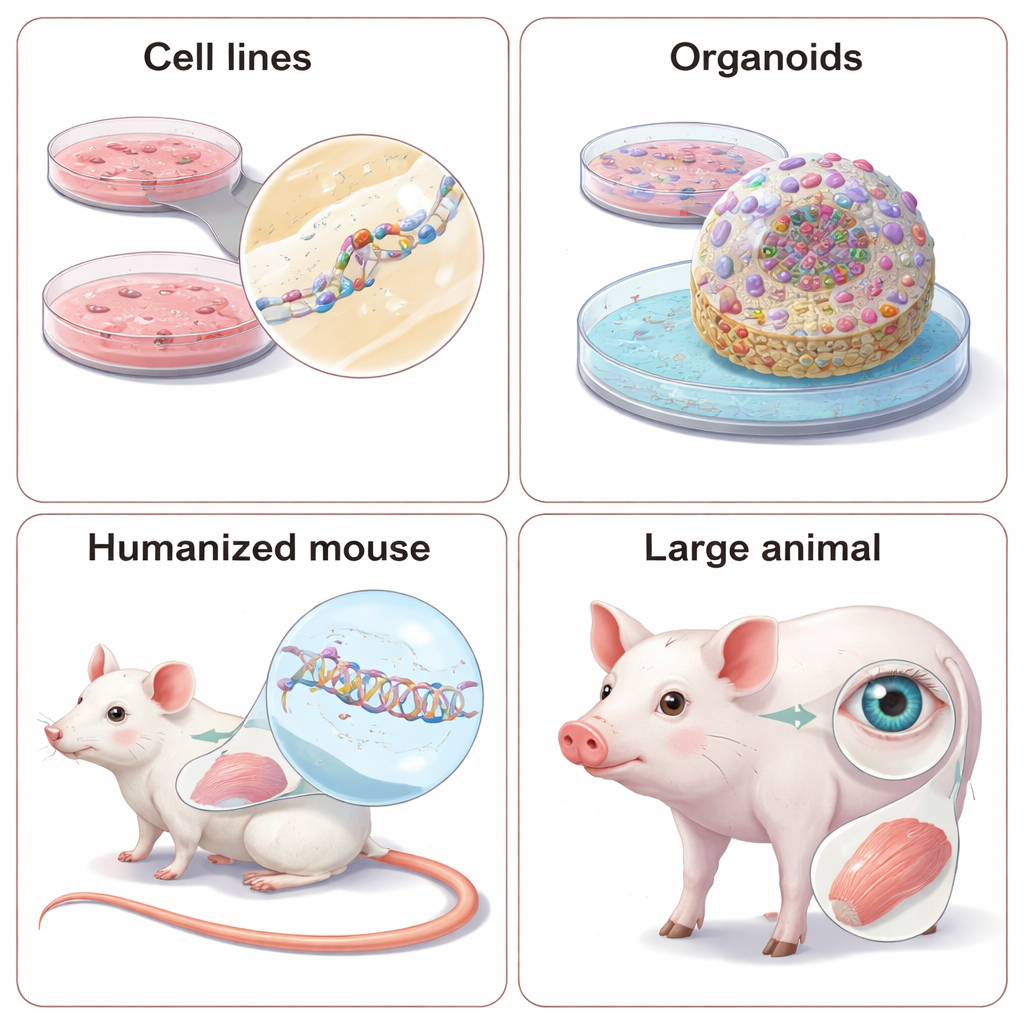
Por qué los animales siguen siendo importantes — y cómo humanizarlos
Algunas características de la enfermedad, como el metabolismo a nivel corporal, las interacciones órgano a órgano o el comportamiento, sencillamente no pueden capturarse en placas. Para esto, las TAN se prueban en animales vivos. Dado que estos fármacos dependen de secuencias exactas de ARN, los científicos se enfrentan a una elección: diseñar fármacos «sustitutos» que coincidan con la versión del gen del animal, o reingenierizar al animal para que porte secuencias genéticas humanas. Los ASO y siRNA sustitutos pueden revelar si reducir un gen mejora los síntomas en modelos de ratón bien establecidos, pero no reproducen perfectamente el fármaco dirigido al humano. Los modelos humanizados—ratones o incluso mini‑cerdos con secciones o copias completas de genes humanos—permiten probar el candidato clínico real, pero requieren tiempo y coste significativos, y las diferencias sutiles en la regulación génica entre especies aún pueden provocar sorpresas. La revisión también destaca el uso creciente de animales grandes, especialmente para enfermedades del ojo y del músculo, donde la anatomía se asemeja más a la humana.
Mirando al futuro: modelos más inteligentes y menos conjeturas
Los autores concluyen que no existe un «mejor» modelo único para los fármacos de ácidos nucleicos; en su lugar, cada proyecto necesita una trayectoria a medida que comienza con ensayos rápidos y simples y avanza hacia sistemas más complejos y relevantes para el humano. A medida que reguladores y financiadores impulsan la reducción del uso de animales, se espera que organoides sofisticados, dispositivos órgano‑en‑un‑chip y modelos computacionales asuman más carga, sobre todo cuando se combinan con herramientas de aprendizaje automático que predicen qué secuencias y químicas funcionarán mejor. En última instancia, al entender las fortalezas y los puntos ciegos de cada modelo—y compartiendo buenas prácticas y datos en todo el campo—los investigadores podrán convertir con mayor fiabilidad las ideas genéticas programables en medicamentos seguros y eficaces para los pacientes.
Cita: Oliver, P.L., Hill, A.C. Model selection in preclinical nucleic acid therapeutics research. Commun Biol 9, 200 (2026). https://doi.org/10.1038/s42003-026-09650-7
Palabras clave: terapias con ácidos nucleicos, oligonucleótidos antisentido, siRNA, modelos preclínicos, terapia génica