Clear Sky Science · es
Análisis estructural revela que moléculas de agua median la autoactivación de GPR99
Por qué este receptor importa en la inflamación
Nuestras vías respiratorias y otros tejidos están constantemente detectando señales químicas que indican infección o irritación. Un sensor de este tipo, una proteína llamada GPR99 localizada en la superficie celular, está emergiendo como un interruptor importante en enfermedades inflamatorias como el asma y los pólipos nasales. Este estudio explica, con detalle atómico, cómo GPR99 puede activarse por sí mismo incluso sin un disparador químico externo —y cómo pequeños cúmulos de agua le ayudan a hacerlo— ofreciendo pistas para diseñar nuevos fármacos antiinflamatorios.
Un interruptor incorporado dentro de un sensor celular
GPR99 pertenece a una gran familia de proteínas de membrana que transmiten mensajes desde el exterior hacia el interior celular, a menudo cambiando de forma y reclutando proteínas asociadas llamadas proteínas G. A diferencia de la mayoría de estos receptores, GPR99 es inusualmente activo aun cuando no hay una molécula señalizante unida. Los autores muestran que un bucle flexible en el lado externo de GPR99, conocido como el segundo bucle extracelular, actúa como una llave interna: se pliega dentro del bolsillo de unión habitual, imitando una señal activadora y encendiendo el receptor por sí solo.
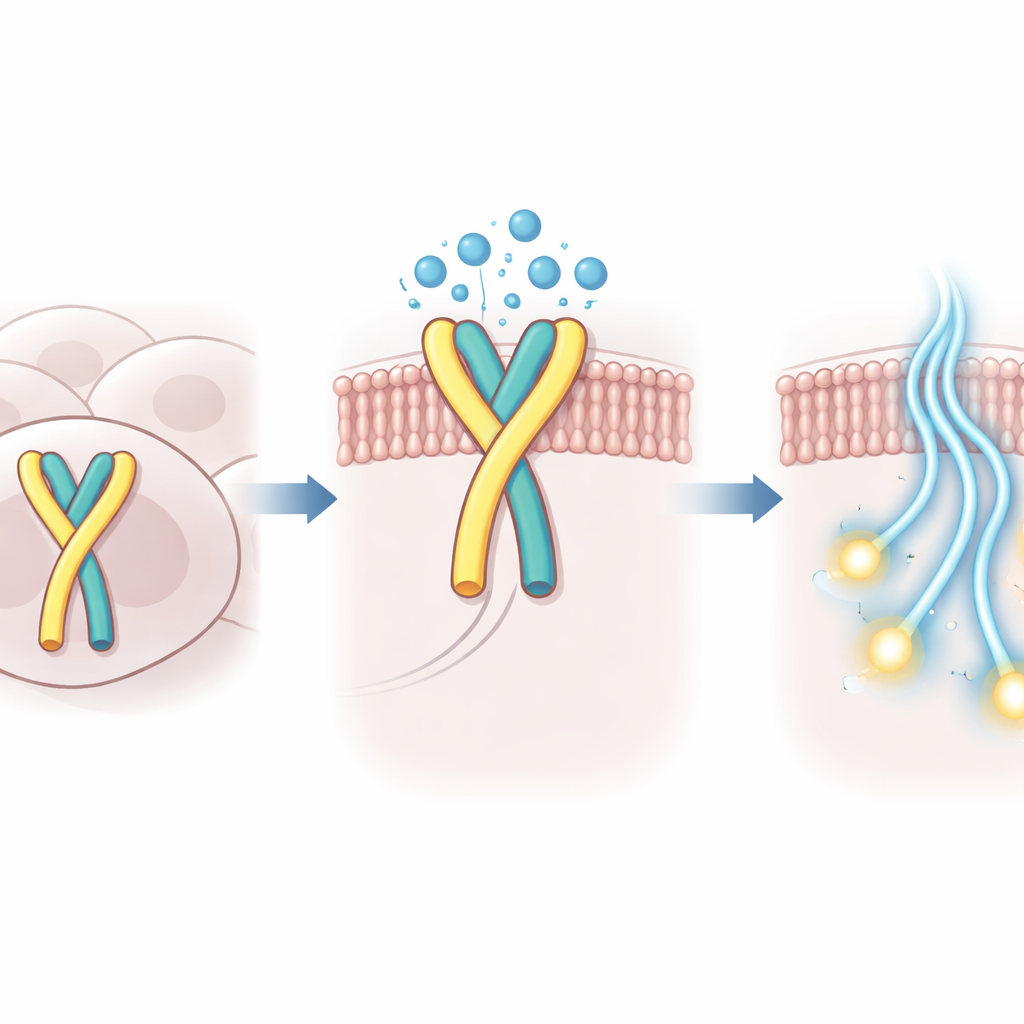
Cómo el agua ayuda a mantener el interruptor en su lugar
Usando criomicroscopía electrónica de alta resolución, los investigadores capturaron la estructura tridimensional de la GPR99 humana unida a su proteína G asociada en este estado autoactivado. En el bolsillo de unión donde normalmente se alojarían moléculas externas, observaron no solo el bucle plegado, sino también un pequeño cúmulo de moléculas de agua ordenadas. Estas moléculas de agua forman un puente polar entre el bucle y la proteína circundante, compensando la inserción más superficial del bucle y estabilizando la forma activa del receptor. Cuando aminoácidos clave en el bucle o en el bolsillo vecino se alteraron de modo que estos contactos mediados por agua se debilitaban, la actividad incorporada de GPR99 cayó drásticamente en ensayos celulares.
Reordenamiento del funcionamiento interno para señalización constante
El equipo comparó su estructura autoactivada con otros miembros de la familia, incluido un receptor estrechamente relacionado que une el subproducto metabólico succinato y una forma activa de GPR99 unida al metabolito 2‑oxoglutarato. Encontraron que GPR99, en ausencia de cualquier ligando externo, ya está completamente predispuesto en una conformación activa: varios “microswitches” conservados dentro de su núcleo helicoidal adoptan formas normalmente vistas solo cuando estos receptores son estimulados. Posiciones críticas que habitualmente ayudan a mantener los receptores en un estado inactivo están reemplazadas o reorientadas en GPR99, aflojando las restricciones internas y favoreciendo la configuración abierta que acoge a la proteína G asociada.
Transmitiendo el mensaje al interior celular
En el lado interno de la membrana, la estructura revela cómo GPR99 agarra a la proteína G de tipo Gq que transmite su señal. Una cola helicoidal de la proteína G se acomoda en una cavidad abierta por el giro hacia fuera de una de las hélices de GPR99, estableciendo una red de contactos polares e hidrofóbicos con los bucles internos y la cola del receptor. Mutaciones que alteran esta interfaz también reducen la señalización, confirmando que la autoactivación creada por el bucle externo y el cúmulo de agua se acopla de forma eficaz a los socios intracelulares. En conjunto, estas instantáneas estructurales conectan los cambios en la superficie externa del receptor con las oleadas de señalización por calcio que desencadena dentro de las células.
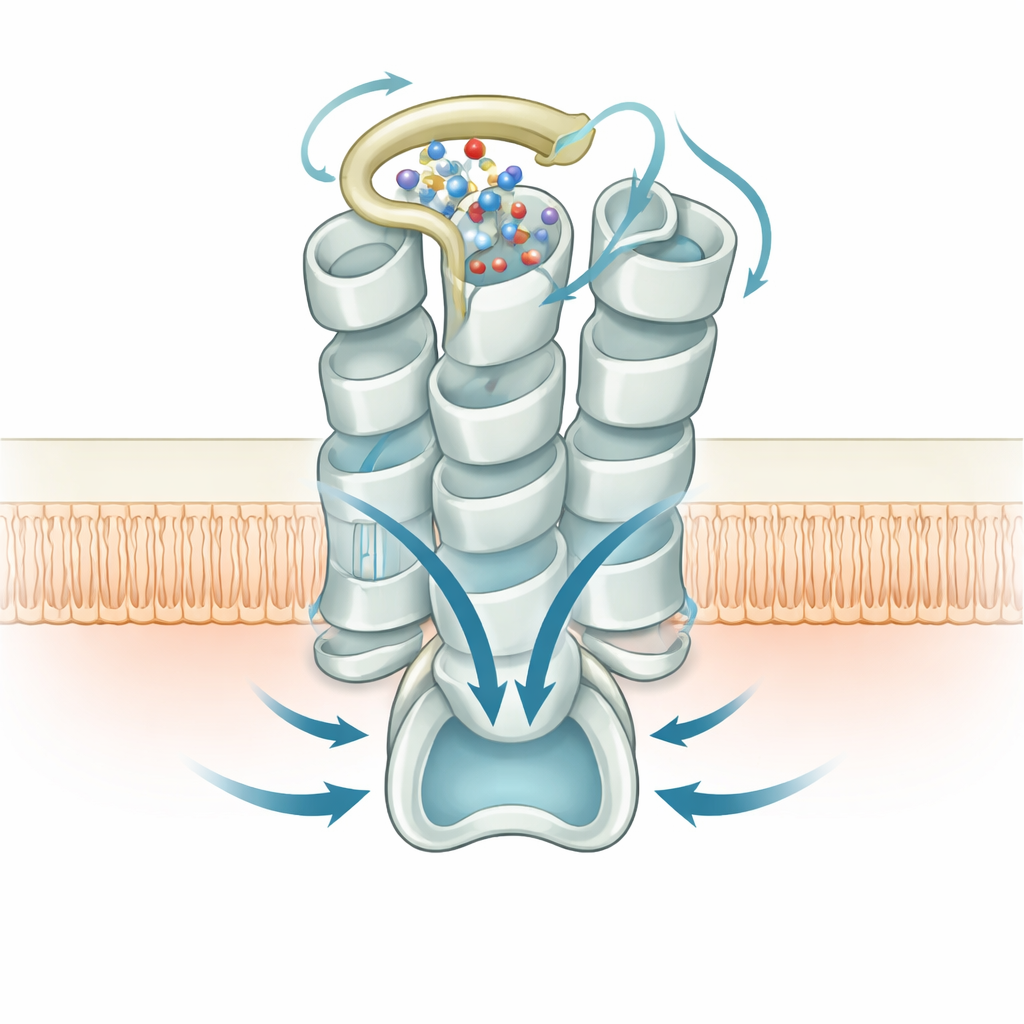
Implicaciones para la respiración y más allá
Los autores sugieren que la actividad incorporada de GPR99, reforzada por moléculas de agua estructurales, puede mantener los tejidos de las vías aéreas en un modo de “espera”, preparados para liberar moco y montar una respuesta inmune cuando aparecen lípidos inflamatorios o cambios metabólicos. Dado que GPR99 es muy activo incluso sin señales externas, y porque su activación depende de una disposición específica de bucle y agua, estos conocimientos estructurales ofrecen objetivos concretos para los diseñadores de fármacos. Moléculas pequeñas que interrumpan este interruptor interno o su red de agua podrían reducir la inflamación excesiva, mientras que compuestos que afinan la interacción podrían aprovechar la sensibilidad de GPR99 con fines terapéuticos.
Cita: Xiao, M., Bao, X., Guo, Y. et al. Structural analysis reveals that water molecules mediate self-activation of GPR99. Commun Biol 9, 342 (2026). https://doi.org/10.1038/s42003-026-09644-5
Palabras clave: GPR99, activación de GPCR, biología estructural, inflamación, señalización mediada por agua