Clear Sky Science · es
Mecanismo estructural de un anticuerpo anti-MHC-I que bloquea receptores inhibidores de células NK en la inmunidad antitumoral
Despertando a los silenciosos asesinos del cuerpo
Nuestro sistema inmune cuenta con poderosos centinelas llamados células asesinas naturales (NK) que pueden detectar y destruir células cancerosas o infectadas por virus. Sin embargo, los tumores suelen aprender a silenciar a estos centinelas. Este artículo revela, con detalle atómico, cómo un anticuerpo diseñado específicamente puede retirar ese “botón de silencio”, reactivando a las NK para que ataquen los tumores con mayor eficacia. El trabajo combina biología estructural de vanguardia con experimentos en ratón para mostrar cómo un anticuerpo podría complementar las inmunoterapias oncológicas existentes.
Las etiquetas de identidad inmune en nuestras células
Cada célula de nuestro organismo muestra en su superficie “etiquetas de identidad” moleculares llamadas moléculas MHC de clase I. Estas etiquetas ayudan a las células inmunitarias a distinguir el tejido normal de las células peligrosas que se han vuelto cancerosas o han sido infectadas por virus. Las NK escanean constantemente estas etiquetas. Cuando detectan patrones normales, los receptores inhibidores en las NK envían una señal calmante que evita el ataque. Los tumores a menudo mantienen visibles estas etiquetas, usándolas como un escudo protector: mientras fluya la señal inhibitoria, las NK contienen su respuesta y el cáncer puede crecer.
Un anticuerpo que arrebata el escudo
Los investigadores estudiaron un anticuerpo monoclonal llamado B1.23.2 que se une con fuerza a muchas variantes humanas de MHC clase I en células tumorales. Empleando criomicroscopía electrónica y cristalografía de rayos X, mapearon exactamente cómo se asienta este anticuerpo sobre la superficie del MHC. B1.23.2 se fija en una cresta conservada de la molécula MHC —una hélice α2— sin tocar a su cadena ligera asociada y apenas percibiendo el péptido presentado. Esto significa que el anticuerpo puede reconocer una amplia gama de moléculas humanas MHC-A, -B y -C con afinidad muy alta, siendo relativamente insensible a los fragmentos proteicos específicos que el MHC exhibe.
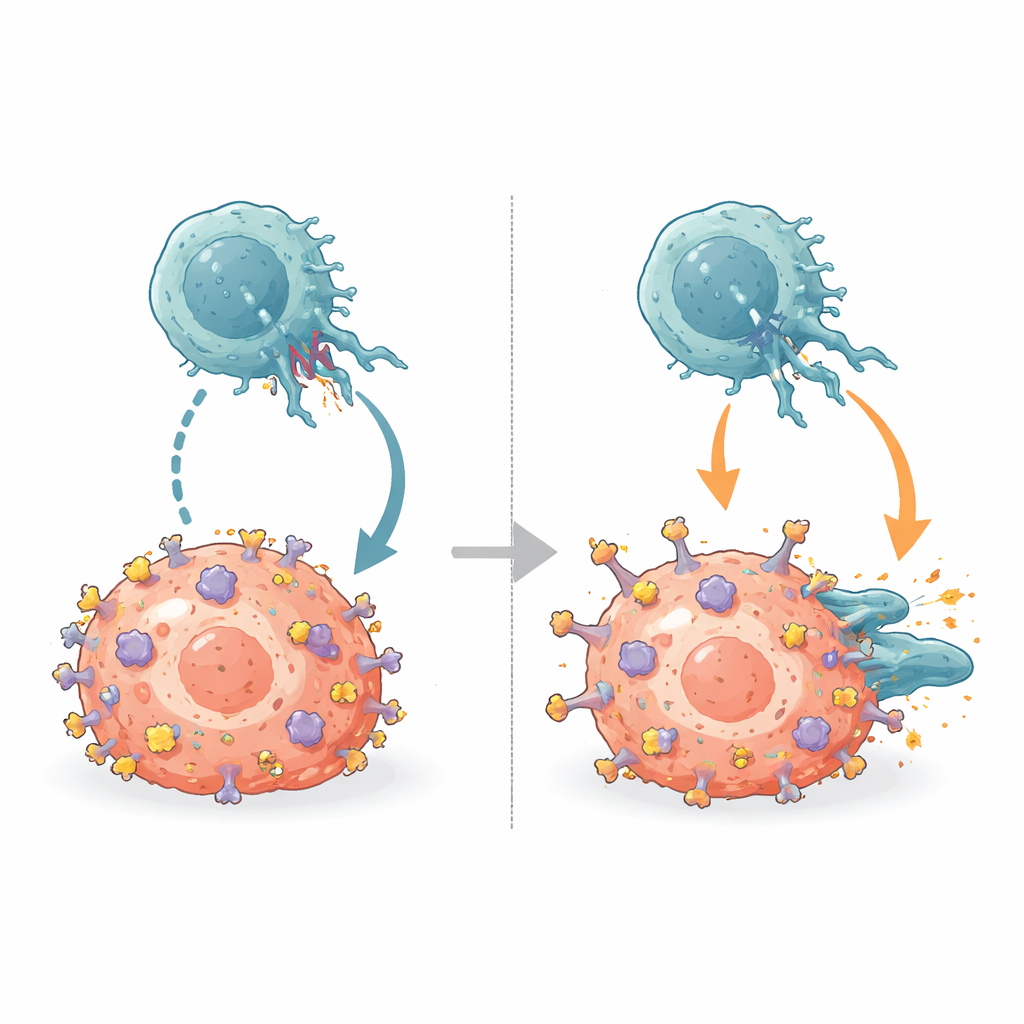
Venciendo los frenos inmunitarios
Las NK portan receptores inhibidores denominados KIR que normalmente se acoplan a la misma cresta α2 del MHC. Alineando las nuevas estructuras anticuerpo–MHC con estructuras conocidas de KIR–MHC, el equipo mostró que B1.23.2 ocupa físicamente el parche del MHC que los KIR necesitan para agarrarse. El sitio de unión del anticuerpo y las huellas de los KIR se solapan tan extensamente que ambos no pueden unirse al mismo tiempo. B1.23.2 además se une al MHC con mayor afinidad que los KIR, por lo que gana esta pulseada molecular. Como resultado, cuando el anticuerpo recubre las moléculas MHC de las células tumorales, los KIR en las NK ya no pueden transmitir sus señales inhibitorias, desplazando el equilibrio hacia la activación de las NK.
Ajustando el encaje y ampliando el alcance
Aunque B1.23.2 se dirige principalmente a la superficie conservada del MHC, los autores hallaron que pequeñas diferencias en el péptido unido al MHC pueden ajustar sutilmente la fuerza del anticuerpo. Mediante el intercambio sistemático de una única posición de aminoácido en el péptido, mostraron cambios modestos en la unión —generalmente dentro de un rango de aproximadamente diez veces— sin perder el reconocimiento global. También investigaron por qué ciertos tipos comunes de MHC, como HLA-A*02:01, eluden la unión. Trasplantando residuos clave de contacto desde una variante de MHC receptiva a HLA-A*02:01, el equipo diseñó versiones que el anticuerpo pudo reconocer, confirmando con precisión qué posiciones forman la superficie crítica de acoplamiento. Estos hallazgos sugieren que en el futuro podrían diseñarse variantes de anticuerpos para abarcar aún más tipos de MHC o evitarlos selectivamente.
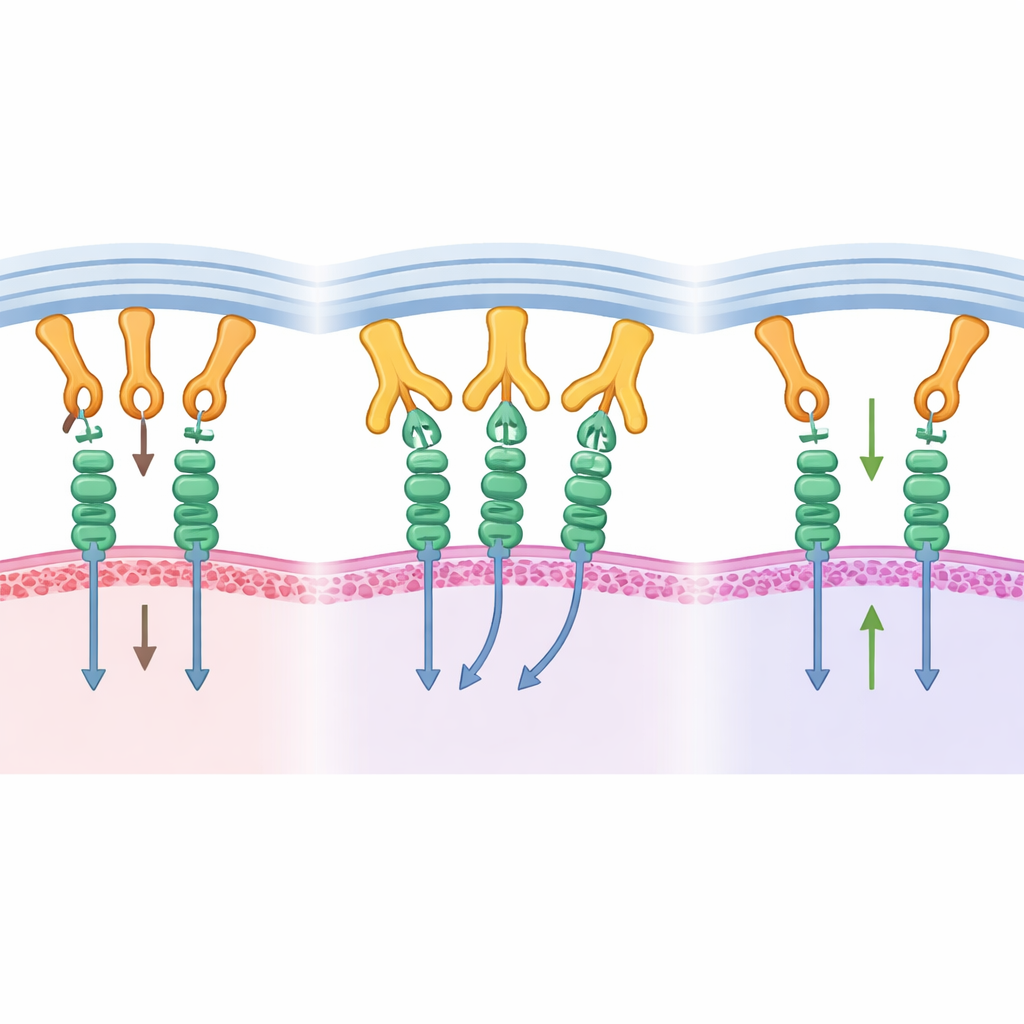
Convertir la visión estructural en control tumoral
¿Ayuda realmente este bloqueo molecular a combatir los tumores? Para probarlo, los investigadores usaron un modelo de ratón humanizado portador de un cáncer pancreático humano. Diseñaron una forma de B1.23.2 incapaz de señalizar a través de su propia cola Fc, de modo que cualquier efecto proviniera principalmente del bloqueo de la interacción MHC–KIR. Cuando los ratones recibieron el anticuerpo junto con células NK humanas, los tumores crecieron mucho más despacio. Las NK mostraron mayor proliferación, mayor actividad de vías de crecimiento y señalización, y mayor producción de moléculas inflamatorias asociadas con la destrucción de células cancerosas. Dentro de los tumores, las NK exhibieron más receptores activadores, coherente con haber sido liberadas de una entrada inhibitoria constante.
Qué podría significar esto para futuras terapias contra el cáncer
En términos sencillos, este estudio muestra cómo un único anticuerpo puede colarse entre las células tumorales y los frenos del sistema inmunitario, deteniendo la señal de “no atacar” que normalmente mantiene en silencio a las NK. Al cartografiar la interacción a resolución atómica y confirmar sus efectos en animales, el trabajo ofrece un plano para una nueva clase de tratamientos: anticuerpos que se unen a las etiquetas de identidad del tumor en lugar de hacerlo a los propios receptores inmunes. Estos agentes podrían combinarse con inhibidores de punto de control existentes o con terapias celulares para movilizar tanto a NK como a linfocitos T, proporcionando al sistema inmune otro ángulo de ataque contra cánceres difíciles de tratar.
Cita: Jiang, J., Panda, A.K., Natarajan, K. et al. Structural mechanism of anti-MHC-I antibody blocking of inhibitory NK cell receptors in tumor immunity. Commun Biol 9, 350 (2026). https://doi.org/10.1038/s42003-026-09641-8
Palabras clave: células asesinas naturales, MHC clase I, inmunoterapia del cáncer, anticuerpos monoclonales, receptores inhibidores