Clear Sky Science · es
LukS-PV dirigido a C5aR inhibe la EMT en el carcinoma hepatocelular a través del eje BCL6/HDAC6/HSPD1
Convertir un arma bacteriana en un luchador contra el cáncer
El carcinoma hepatocelular, la forma más común de cáncer de hígado, suele ser mortal porque se disemina del hígado a otros órganos. Este artículo explora un aliado inesperado contra esa difusión: una proteína, LukS‑PV, que originalmente forma parte de una toxina producida por la bacteria Staphylococcus aureus. Los investigadores muestran cómo esta proteína puede unirse a un receptor específico en las células del cáncer hepático y, en lugar de dañar el tejido normal, bloquear pasos clave que permiten a las células cancerosas desprenderse, desplazarse y formar nuevos tumores.
Por qué importa frenar a las células cancerosas que cambian de forma
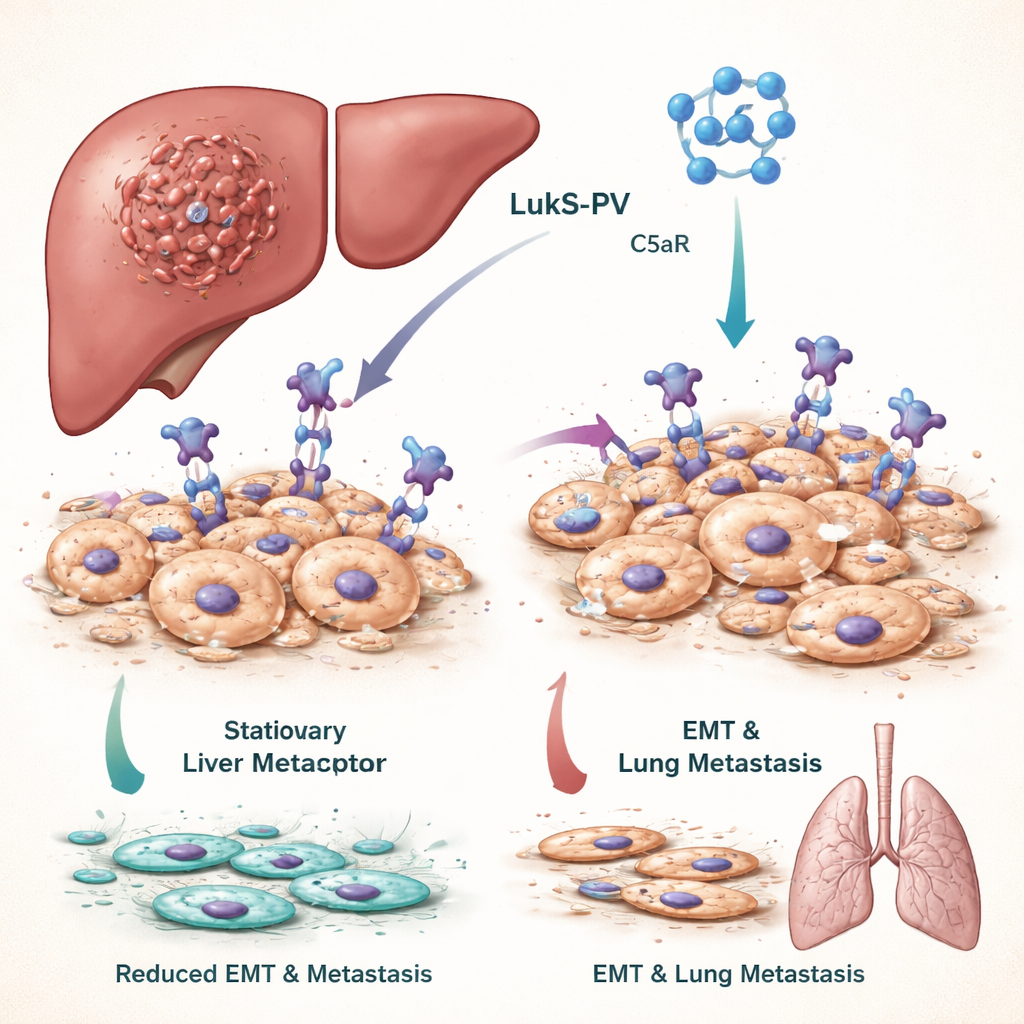
Para que el cáncer de hígado se disemine, las células tumorales deben sufrir un cambio drástico de forma y comportamiento llamado transición epitelio‑mesenquimal, o EMT. En la EMT, células compactas que normalmente se mantienen en su lugar se vuelven más flexibles, móviles e invasivas, lo que les permite infiltrarse en vasos sanguíneos y sembrar órganos distantes como los pulmones. Los pacientes cuyos tumores muestran una actividad marcada de EMT tienden a tener peores resultados. El equipo se centró en una vía de señalización impulsada por una molécula llamada C5a y su receptor C5aR, que está inusualmente abundante en muchas células tumorales y se sabe que promueve la EMT y la metástasis.
Un componente de toxina que apunta a una señal del cáncer
La leucocidina de Panton‑Valentine, una toxina de Staphylococcus aureus, contiene un componente llamado LukS‑PV que reconoce y se une de forma natural a C5aR. Trabajos previos de los autores mostraron que una versión recombinante no formadora de poros de LukS‑PV puede frenar el crecimiento de varios cánceres sin toxicidad evidente en animales. En este estudio, trataron líneas celulares de cáncer hepático con LukS‑PV y observaron que las células se volvieron menos migratorias e invasivas. Pruebas moleculares revelaron que aumentaron marcadores de células estacionarias y bien comportadas, mientras que disminuyeron marcadores de células agresivas y móviles. En ratones inyectados con células de cáncer hepático, el tratamiento con LukS‑PV llevó a un número mucho menor de nódulos tumorales en los pulmones, lo que indica una reducción de la metástasis.
Bloquear una reacción en cadena dentro de las células tumorales
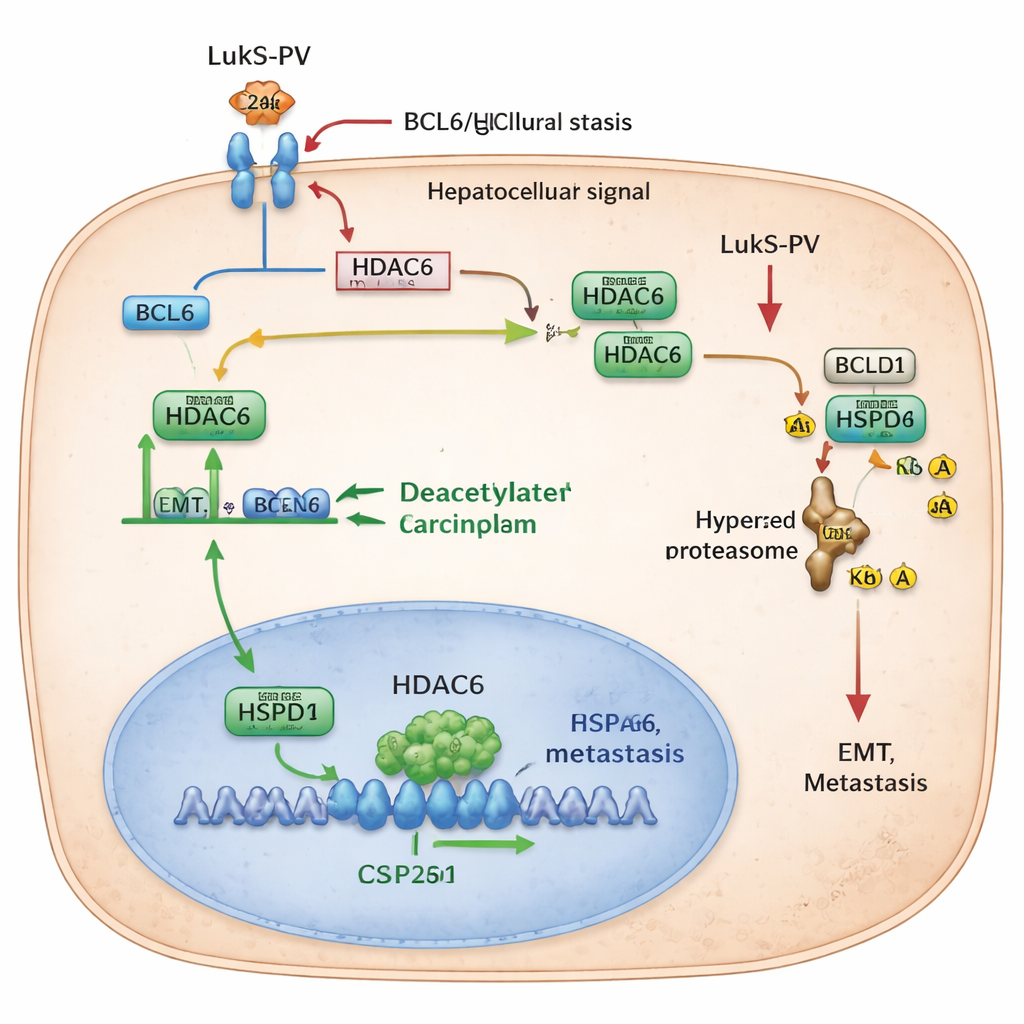
Indagando más, los investigadores descubrieron una cadena de proteínas reguladoras dentro de las células cancerosas que LukS‑PV altera. Primero, LukS‑PV se une a C5aR en la superficie celular y bloquea eficazmente la señal prometastásica de C5a. Esta atenuación de la señalización de C5aR reduce los niveles de una proteína llamada BCL6, un factor de transcripción que normalmente activa ciertos genes en el núcleo. Uno de los objetivos de BCL6 es HDAC6, una enzima que elimina pequeños grupos químicos conocidos como grupos acetilo de otras proteínas. Cuando BCL6 es abundante, los niveles de HDAC6 aumentan y la célula se vuelve más propensa a la EMT y al movimiento. La interferencia de LukS‑PV con C5aR reduce BCL6, lo que a su vez disminuye la producción de HDAC6 y frena este programa prometastásico.
Etiquetar a una chaperona para su destrucción
El equipo identificó entonces a un socio clave de HDAC6 llamado HSPD1, también conocido como HSP60, una proteína «chaperona» que ayuda a otras proteínas a plegarse y mantenerse estables. En el cáncer hepático, los niveles de HSPD1 son más altos que en el tejido normal circundante y se asocian con una peor supervivencia de los pacientes. Los investigadores descubrieron que HDAC6 interactúa físicamente con HSPD1 y le remueve grupos acetilo en dos posiciones específicas. Cuando se eliminan estas etiquetas acetilo, HSPD1 se vuelve más estable y favorece la EMT y la metástasis. Cuando HDAC6 se reduce —ya sea por manipulaciones genéticas o por el tratamiento con LukS‑PV— HSPD1 se vuelve más acetilada. Esta forma hiperacetilada es reconocida por la maquinaria de eliminación celular, etiquetada con ubiquitina y degradada. A medida que descienden los niveles de HSPD1, las células cancerosas pierden parte de su capacidad para migrar, invadir y colonizar los pulmones.
De vías complejas a una conclusión sencilla
Para un público no especialista, el mensaje es que los autores han trazado un efecto dominó dentro de las células de cáncer hepático: un receptor de superficie (C5aR) aumenta una proteína controladora (BCL6), que eleva una enzima (HDAC6) que protege a una chaperona (HSPD1) de ser destruida. Juntos, estos elementos ayudan a las células cancerosas a cambiar de forma, moverse y propagarse. LukS‑PV, una proteína bacteriana reaprovechada en el laboratorio, interrumpe esta secuencia justo en la superficie celular, conduciendo finalmente a la degradación de HSPD1 y a un freno de la metástasis. Aunque aún en fase experimental, este trabajo sugiere que fármacos modelados a partir de LukS‑PV —o dirigidos a BCL6, HDAC6 o HSPD1— podrían ofrecer nuevas formas de impedir la diseminación de tumores hepáticos y mejorar el pronóstico de los pacientes.
Cita: Ding, P., Shi, L., Xu, X. et al. LukS-PV targeting C5aR inhibits EMT in hepatocellular carcinoma via the BCL6/HDAC6/HSPD1 axis. Commun Biol 9, 314 (2026). https://doi.org/10.1038/s42003-026-09640-9
Palabras clave: carcinoma hepatocelular, metástasis, transición epitelio‑mesenquimal, HDAC6, terapia con toxinas bacterianas