Clear Sky Science · es
La migración celular confinada periódica induce una reorganización cromatina parcialmente reversible en líneas celulares cancerosas
Cómo las células cancerosas apretadas recuerdan haber estado sometidas a estrés
Las células cancerosas que se desprenden de un tumor deben arrastrarse por diminutas aberturas en los tejidos y vasos sanguíneos del cuerpo. Para ello, comprimen sus contenidos blandos—y en particular su núcleo, que alberga el ADN—a través de espacios a veces más pequeños que el propio núcleo. Este estudio explora qué ocurre con el empaquetamiento del ADN durante esos exprimidos repetidos y plantea una pregunta clave: ¿el núcleo simplemente vuelve a su estado normal, o conserva una especie de «memoria mecánica» que podría facilitar la diseminación del cáncer?
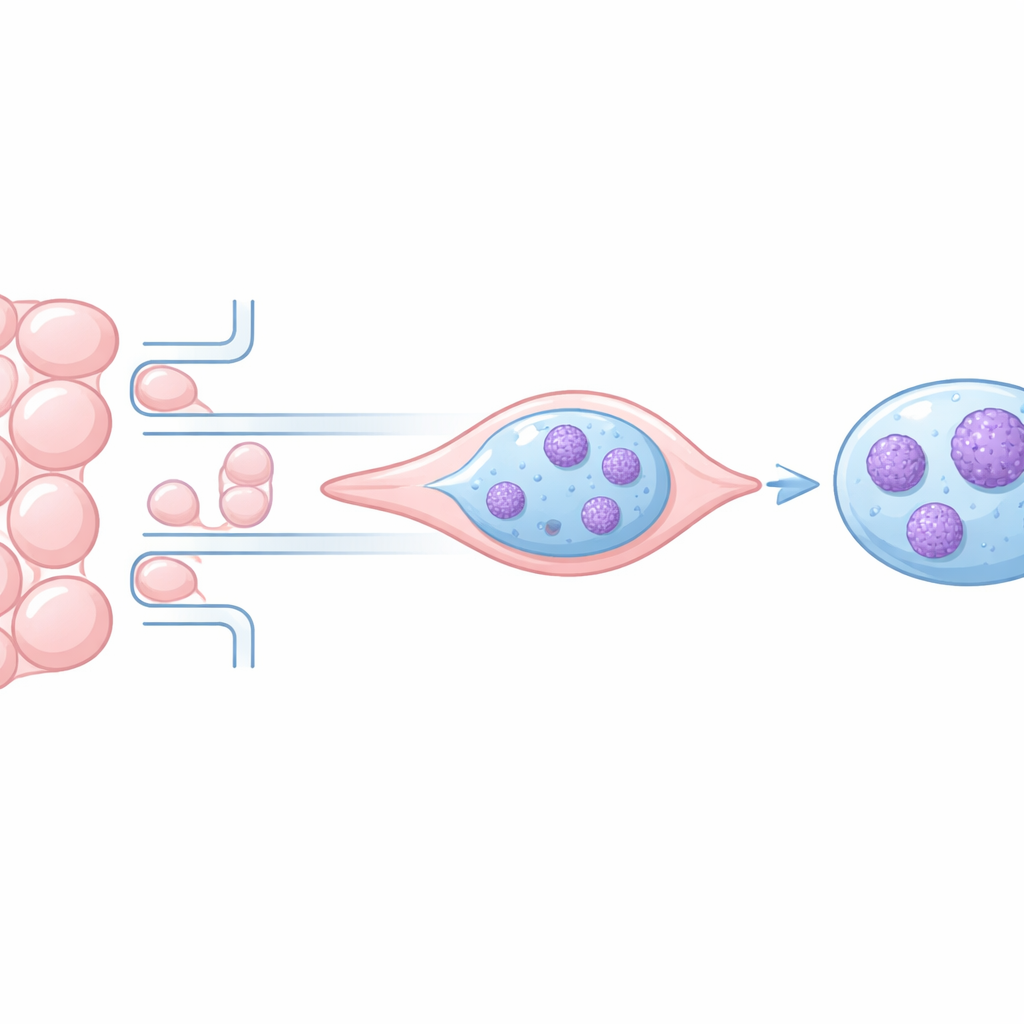
Por qué importa el empaquetamiento del ADN cuando las células se mueven
Dentro del núcleo, el ADN se envuelve alrededor de proteínas y se pliega en cromatina, que puede estar pobremente empaquetada o fuertemente condensada. Las regiones más sueltas tienden a ser activas, albergando genes que se usan con frecuencia, mientras que las regiones más compactas suelen estar silenciosas. Cuando las células migran por espacios estrechos, el núcleo se deforma, y trabajos previos han mostrado que esto puede compactar la cromatina temporalmente e incluso dañar el ADN. Pero no estaba claro si esos cambios se revierten por completo o dejan huellas duraderas que podrían alterar cuán agresivas se vuelven las células cancerosas.
Un laberinto diminuto para exprimir células cancerosas individuales
Los investigadores construyeron un dispositivo microfluídico a medida—un chip transparente que contiene docenas de canales microscópicos que alternan repetidamente entre segmentos anchos y estrechos. Dos líneas celulares cancerosas diferentes, ambas diseñadas para que su cromatina brille bajo el microscopio, fueron guiadas a desplazarse por estos canales usando un atractante químico. Imágenes de alta resolución en lapso de tiempo permitieron al equipo seguir cada núcleo celular a medida que se movía, midiendo el tamaño nuclear y mapeando cuadro a cuadro los racimos de cromatina altamente condensada y brillantes en más de 100 células individuales.
Qué le ocurre al núcleo bajo presión
Siempre que una célula entraba en una constricción estrecha, su núcleo se reducía bruscamente en área proyectada, reflejando una disminución reversible del volumen nuclear. Al mismo tiempo, la fracción del núcleo ocupada por cromatina altamente condensada se disparaba—a menudo de dos a tres veces—y luego volvía a su línea de base una vez que la célula emergía a una región más ancha. Este patrón se repitió a lo largo de varias constricciones sucesivas y en ambos tipos de células cancerosas, lo que sugiere que la cantidad global de cromatina densa es una respuesta flexible y de corto plazo al estrés mecánico más que un cambio permanente. Sin embargo, una observación más detallada de los patrones de fluorescencia reveló que aumentaban los píxeles con intensidad muy alta y muy baja durante el exprimido, lo que apunta a una reorganización interna más compleja que una simple compactación uniforme.
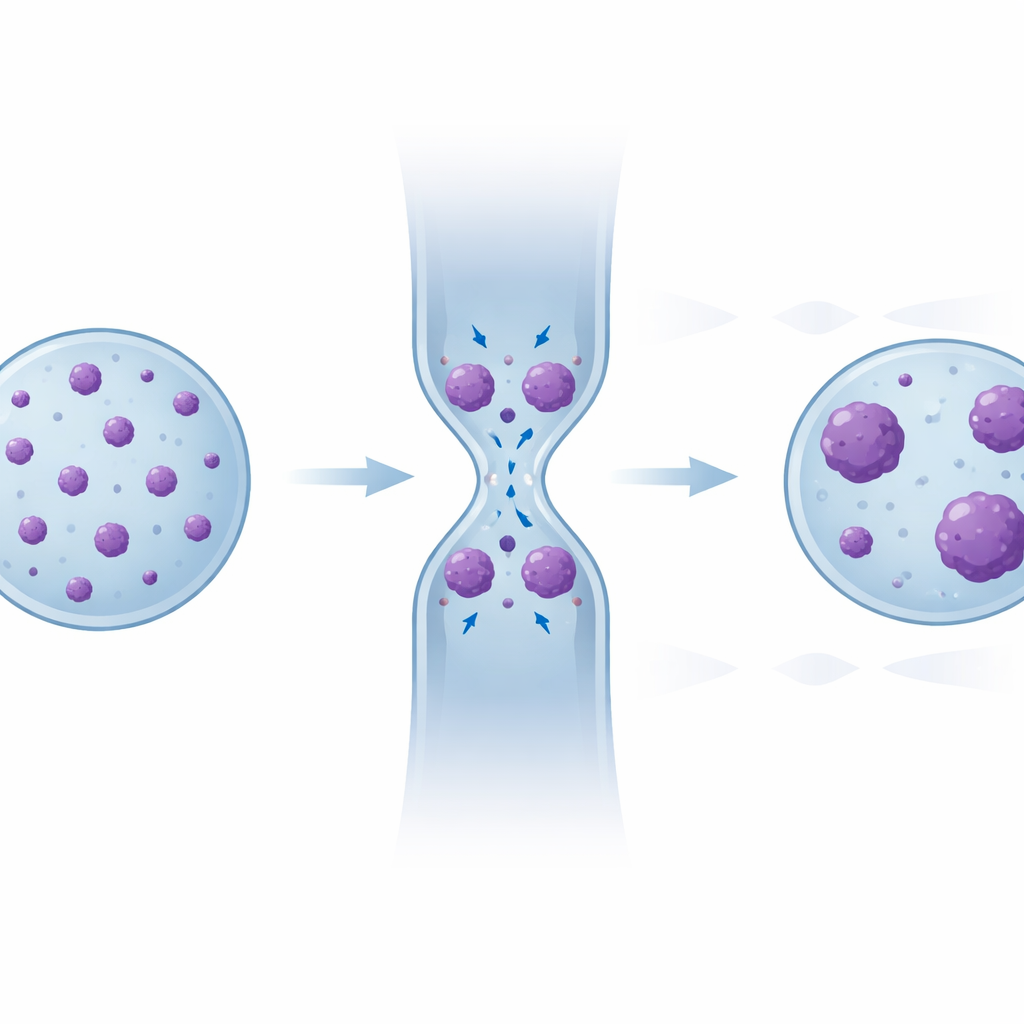
Memoria oculta en el patrón de los racimos de ADN
Para descubrir esa reorganización oculta, el equipo examinó cada racimo condensado individual—su tamaño y cuántos racimos contenía cada núcleo—antes, durante y después del confinamiento. Durante el exprimido, los racimos pequeños tendían a unirse formando otros más grandes. Tras la relajación del núcleo, el área condensada total volvió a su nivel original, pero el patrón no lo hizo: en comparación con el estado inicial, las células que habían pasado por varias constricciones mostraron en conjunto menos racimos, con un sesgo hacia tamaños mayores. Comparaciones estadísticas confirmaron que las distribuciones en las regiones de «recuperación» posteriores se parecían cada vez más a las observadas durante el confinamiento. La inmunofluorescencia mostró además que muchas de estas regiones densas solapaban marcas cromatínicas «silenciosas» bien establecidas, y un modelo computacional de la cromatina como un polímero interactuante reprodujo esta relajación parcial pero no completa simplemente a partir de la física de segmentos de ADN adhesivos que se juntan por deformación.
Qué significa esto para la diseminación del cáncer y futuras terapias
En términos cotidianos, el estudio encuentra que cuando los núcleos de las células cancerosas se exprimen repetidamente, el empaquetamiento del ADN se comporta como una pelota antiestrés con memoria. El núcleo puede recuperar su tamaño y la cantidad global de empaquetamiento denso puede restablecerse, pero el patrón detallado de los grumos de ADN denso no vuelve por completo a su estado original. Tras muchos ciclos de exprimido, el núcleo termina con menos regiones densas pero de mayor tamaño, lo que potencialmente altera qué genes son más o menos accesibles. Esta «memoria mecánica» podría ayudar a las células cancerosas a tolerar mejor deformaciones futuras mientras invaden nuevos tejidos. Entender y, en última instancia, dirigirse a este acoplamiento entre fuerzas físicas y organización del ADN podría abrir nuevas vías para limitar la metástasis interrumpiendo cómo las células cancerosas se adaptan al estrés mecánico.
Cita: Blazquez-Romero, M.d.V., Mendivil-Carboni, M., Sarasquete-Martinez, M. et al. Periodic confined cell migration drives partially reversible chromatin reorganization in cancer cell lines. Commun Biol 9, 366 (2026). https://doi.org/10.1038/s42003-026-09637-4
Palabras clave: migración celular confinada, condensación de la cromatina, mecánica nuclear, memoria mecánica, metástasis del cáncer