Clear Sky Science · es
PTBP1 sostiene la espermatogénesis en ratones facilitando la organización del citoesqueleto mediante la vía mTORC2–PKCα en las células de Sertoli
Por qué este estudio importa para la fertilidad masculina
La infertilidad masculina a menudo parece misteriosa, pero en su esencia depende de una colaboración muy fina entre los espermatozoides en desarrollo y las células «nodrizas» que los sostienen. Este estudio indaga en uno de los ayudantes moleculares ocultos dentro de esas células nodrizas y muestra cómo su fallo puede detener la producción de espermatozoides. Comprender esta capa oculta de control podría señalar el camino hacia nuevos diagnósticos o tratamientos para ciertas formas de infertilidad masculina.
Las células de apoyo que hacen posible el esperma
Los espermatozoides se producen dentro de túbulos largos y enroscados en el testículo llamados túbulos seminíferos. En el revestimiento de esos túbulos se encuentran las células de Sertoli, un tipo de célula de apoyo especializada que acuna a las células germinales en desarrollo, las alimenta y las guía mientras se dividen y maduran hasta convertirse en espermatozoides. Las células de Sertoli también construyen una pared protectora conocida como la barrera hemato-testicular, que separa las células en etapas tempranas del sistema inmunitario. Para hacer todo esto, dependen de un andamiaje interno de filamentos de actina y microtúbulos que se remodela constantemente a medida que olas de células germinales se desplazan por los túbulos. Si este andamiaje se altera, la barrera pierde su integridad y las células germinales en maduración pueden desprenderse o morir, poniendo en riesgo la fertilidad.
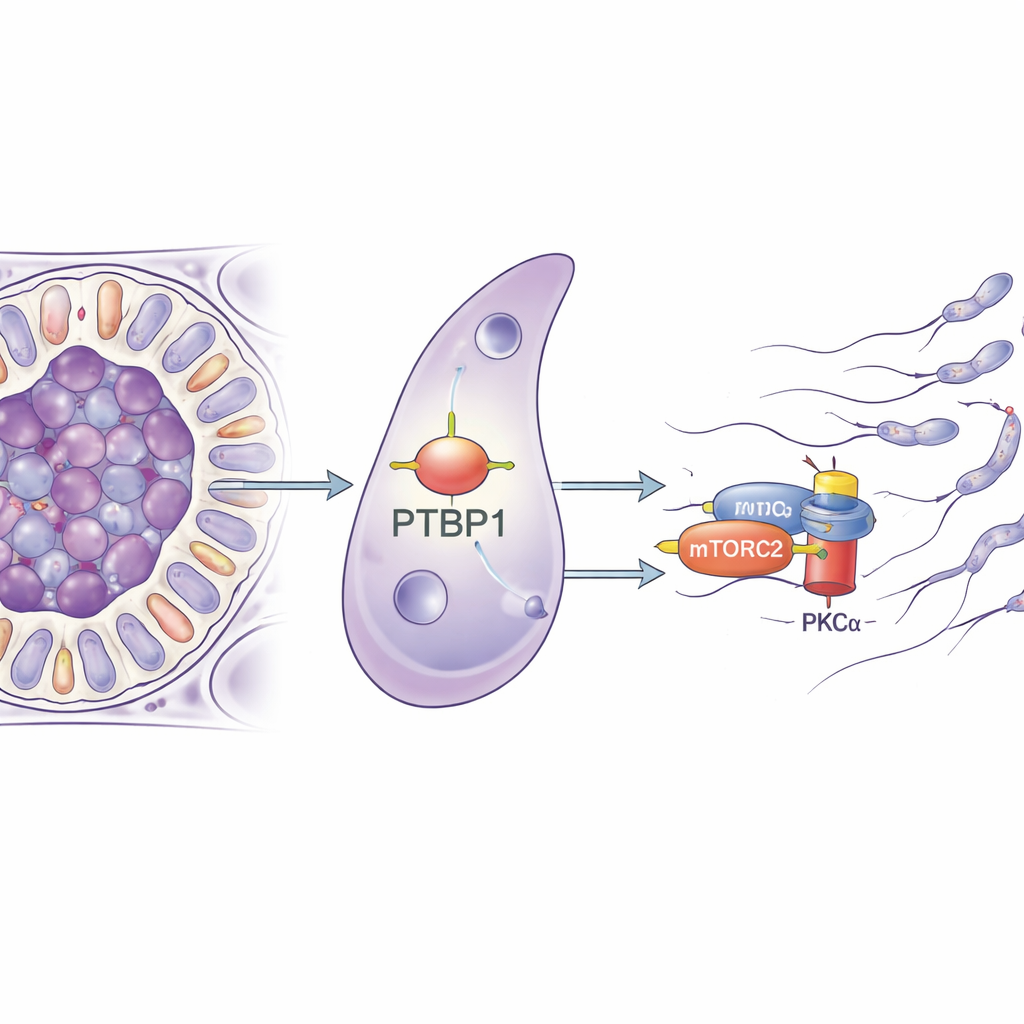
Un pequeño gestor de ARN con una gran misión
Los investigadores se centraron en una proteína llamada PTBP1, conocida por su papel en la gestión de moléculas de ARN dentro de las células: decide cómo se empalman los genes, la estabilidad de sus mensajes y cuán eficientemente se traducen en proteínas. PTBP1 es abundante tanto en las células germinales como en las células de Sertoli, y trabajos previos mostraron que eliminarla de las células germinales dificulta la producción de esperma. En este estudio, el equipo eliminó específicamente PTBP1 solo en las células de Sertoli de ratones. A primera vista, los ratones jóvenes parecían normales, pero al alcanzar la madurez sexual sus testículos se encogieron, el número de espermatozoides en el epidídimo se desplomó y ninguno de los machos pudo engendrar descendencia, revelando una pérdida completa de fertilidad.
Cuando el andamiaje celular se desmorona
El examen microscópico de los testículos de estos ratones mostró que la espermatogénesis se detenía a mitad de proceso. Muchos túbulos contenían espacios vacíos, agregados anormales de núcleos germinales fusionados y escasez de espermatozoides completamente alargados. Los núcleos de las células de Sertoli, que normalmente se adhieren a la pared externa de los túbulos, a menudo estaban desplazados hacia el centro, lo que sugiere que estas células de apoyo estaban perdiendo su anclaje en la estructura circundante. El marcado de componentes clave de las uniones y proteínas estructurales confirmó que la barrera hemato-testicular se debilitó y que los haces habituales de filamentos de actina fueron reemplazados por hebras desorganizadas y excesivamente intensas que se extendían desde la base hasta el centro del túbulo. Una molécula trazadora que normalmente permanece en el lado “sanguíneo” de la barrera, filtró en cambio profundamente dentro de los túbulos, demostrando directamente la rotura de la barrera.
Trazando el fallo hasta un centro de señalización
Para entender cómo una proteína fijadora de ARN podía causar problemas mecánicos tan contundentes, el equipo purificó células de Sertoli y analizó qué genes cambiaban su actividad cuando faltaba PTBP1. Muchos de los genes afectados intervenían en el control del esqueleto celular y en la adhesión entre células, señalando un defecto de remodelado amplio. Luego los investigadores capturaron las moléculas de ARN que se unen físicamente a PTBP1 y hallaron que ésta se fija al mensaje para Rictor, una pieza central de un complejo de señalización llamado mTORC2. Este complejo, a su vez, activa una enzima llamada PKCα que da forma a los filamentos de actina. En las células de Sertoli sin PTBP1, la cantidad de proteína RICTOR disminuyó y PKCα estaba mucho menos activa, aunque el nivel del ARN subyacente para Rictor casi no cambió. Esto sugiere con fuerza que PTBP1 ayuda a las células de Sertoli a producir suficiente proteína RICTOR a partir de su mensaje de ARN, manteniendo así activa la vía mTORC2–PKCα.
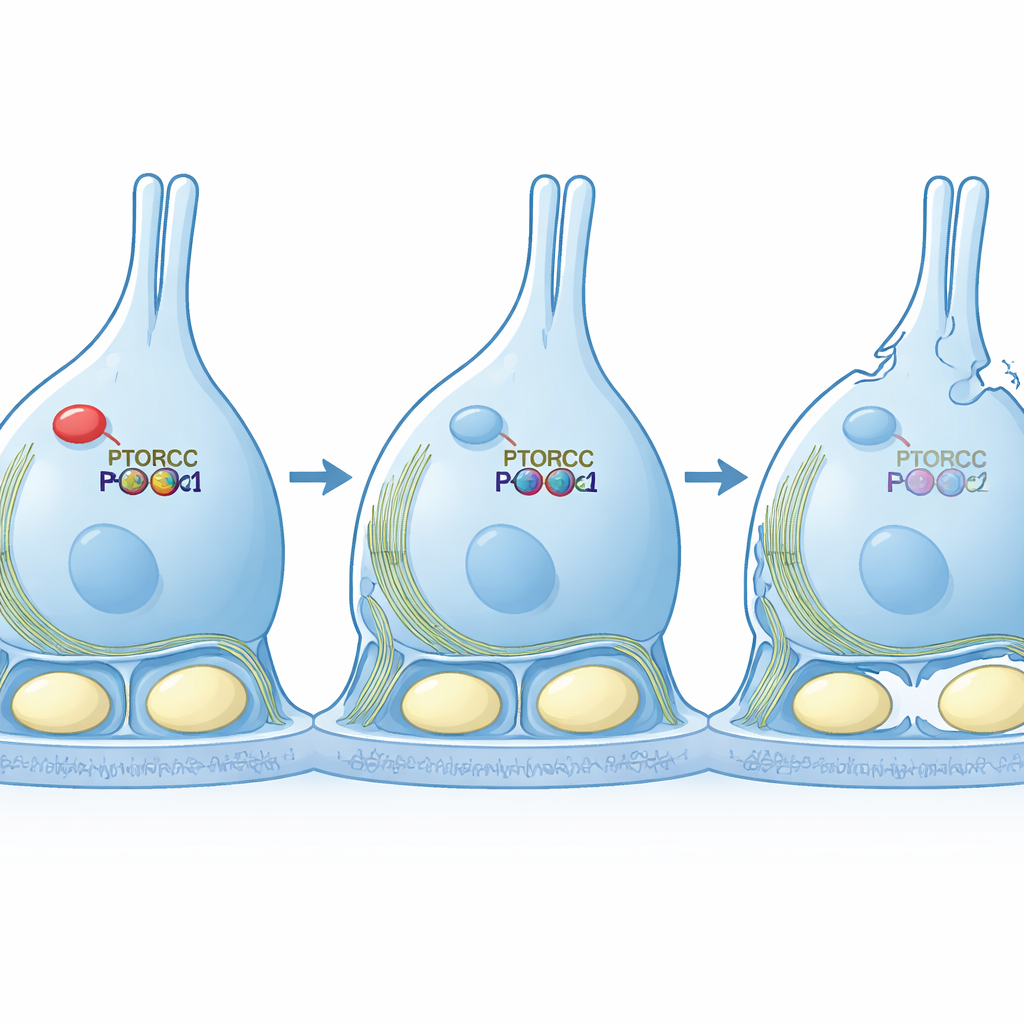
Rescatando el andamiaje restaurando la señal
El equipo pasó luego a modelos de cultivo celular para probar la causalidad. Cuando redujeron PTBP1 en una línea celular similar a Sertoli, las células se estiraron en formas largas y delgadas y mostraron una red de actina desordenada —señales típicas de una señalización mTORC2 debilitada. De forma importante, cuando obligaron a esas células a producir una versión permanentemente activa de PKCα, las células recuperaron su forma compacta y estructuras de actina más ordenadas, aunque RICTOR permaneciera bajo. Este experimento de rescate muestra que la función principal de PTBP1 en este contexto es mantener la vía mTORC2–PKCα lo suficientemente activa como para organizar el andamiaje interno de la célula.
Qué implica esto para entender la infertilidad
En términos sencillos, este trabajo revela una cadena de dependencia dentro del testículo: PTBP1 ayuda a las células de Sertoli a construir un centro de señalización clave; ese centro organiza su esqueleto interno; y un esqueleto intacto les permite sujetar y proteger a los espermatozoides en desarrollo. Rompe la cadena en PTBP1, y las células de Sertoli pierden su estructura, la barrera protectora falla y la formación de esperma se colapsa, resultando en infertilidad masculina. Aunque esta investigación se hizo en ratones, las mismas moléculas están presentes en humanos, lo que abre la posibilidad de que defectos sutiles en el control del ARN dentro de las células de Sertoli subyacen a algunos casos inexplicados de infertilidad masculina y ofrece un nuevo conjunto de dianas moleculares para futuros estudios.
Cita: Ozawa, M., Taguchi, J., Mori, H. et al. PTBP1 supports mouse spermatogenesis by facilitating cytoskeletal organization through the mTORC2–PKCα pathway in Sertoli cells. Commun Biol 9, 341 (2026). https://doi.org/10.1038/s42003-026-09636-5
Palabras clave: fertilidad masculina, células de Sertoli, espermatogénesis, citoesqueleto, proteínas fijadoras de ARN