Clear Sky Science · es
Regulación negativa de la vía NF-κB por la ligasa de ubiquitina Nedd4-1(NE)
Por qué apagar la inflamación importa
Nuestro sistema inmunitario depende de ráfagas rápidas de inflamación para combatir infecciones y reparar daños, pero esas mismas fuerzas pueden dañar tejidos y alimentar el cáncer si permanecen activas demasiado tiempo. Este artículo explora cómo las células humanas y de otros primates evitan ese peligro mediante un "freno" incorporado recién caracterizado que silencia uno de los sistemas de alarma centrales del organismo cuando ha cumplido su función.
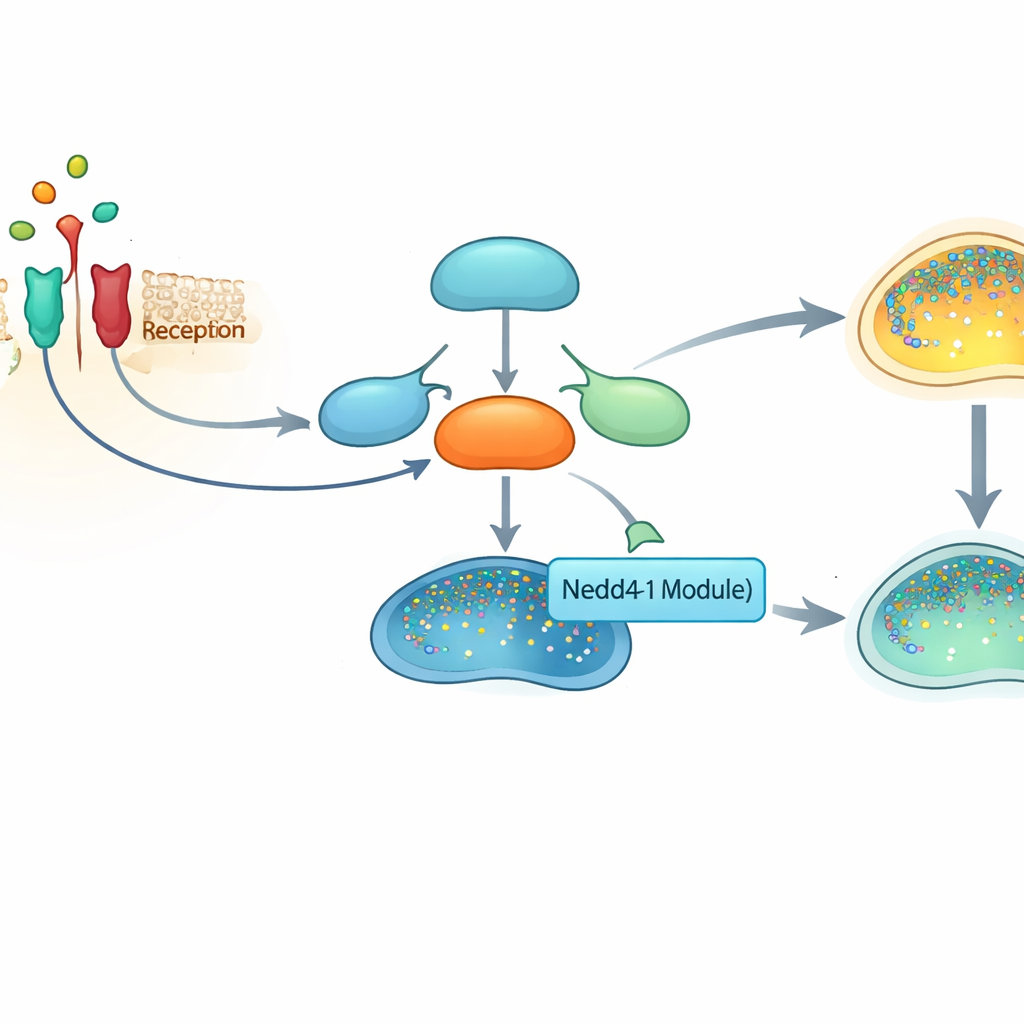
Un interruptor de alarma central en nuestras células
En el corazón de esta historia está NF-κB, una familia de proteínas que actúa como un interruptor maestro para cientos de genes implicados en la inflamación, la supervivencia celular y la inmunidad. Cuando las células detectan señales de estrés, como la molécula inflamatoria TNFα, una cadena de acontecimientos libera a NF-κB de sus "chaperonas" proteicas en el fluido interior de la célula y le permite moverse al núcleo, donde activa genes proinflamatorios y prosupervivencia. Debido a que esta vía es tan potente, las células deben ajustar con precisión tanto su activación como su apagado. La incapacidad para detenerla se ha relacionado con enfermedades inflamatorias crónicas y muchos cánceres.
Un freno exclusivo de los primates
Los investigadores se centraron en Nedd4-1, un miembro de una amplia familia de enzimas que marcan a otras proteínas con una pequeña molécula llamada ubiquitina. Esta etiqueta suele señalar proteínas para su destrucción o reubicación dentro de la célula, remodelando las redes de señalización. Una variante de empalme de Nedd4-1 previamente descubierta, denominada Nedd4-1(NE), se encuentra solo en primates y presenta un segmento largo adicional en su extremo N que altera su localización celular y lo que reconoce. En contraste con la forma estándar de Nedd4-1, que puede potenciar la actividad de NF‑κB mediante otros socios, el equipo halló que Nedd4-1(NE) tiene el efecto opuesto: atenúa la señalización de NF‑κB, especialmente tras una exposición prolongada a TNFα.
Dos maneras de mantener a NF-κB bajo control
Para descubrir cómo funciona este freno, los autores usaron etiquetado por proximidad y métodos de captura de proteínas para ver qué moléculas se asocian físicamente con Nedd4-1(NE). Identificaron componentes clave de la vía NF‑κB, incluida la quinasa IKKβ y la proteína precursora NF‑κB1 (también llamada p105). Experimentos posteriores mostraron que Nedd4-1(NE) añade etiquetas de ubiquitina a IKKβ, conduciendo a su degradación. Con menos IKKβ disponible, su diana habitual IκBα ya no se fosforila y destruye con la misma eficiencia. Como resultado, IκBα permanece más estable y mantiene la subunidad activa de NF‑κB, p50, secuestrada en el citosol, impidiendo que entre en el núcleo para activar genes inflamatorios.
Un traspaso guiado por un adaptador hacia el freno
Nedd4-1(NE) también actúa más aguas abajo limitando los niveles de NF‑κB1. Aquí, la enzima no trabaja sola: colabora con otra proteína que etiqueta con ubiquitina llamada KPC1. KPC1 ayuda a procesar el precursor NF‑κB1 p105 en la forma activa p50 y reside en compartimentos celulares conocidos como endosomas tardíos, donde también se encuentra Nedd4-1(NE). El equipo demostró que Nedd4-1(NE) puede ubiquitinar a KPC1 y que este KPC1 modificado actúa como adaptador, reclutando NF‑κB1 hacia Nedd4-1(NE) en los endosomas tardíos. Este complejo triple promueve la inestabilización tanto de p105 como de p50, reduciendo de nuevo la reserva de NF‑κB que puede alcanzar el núcleo.
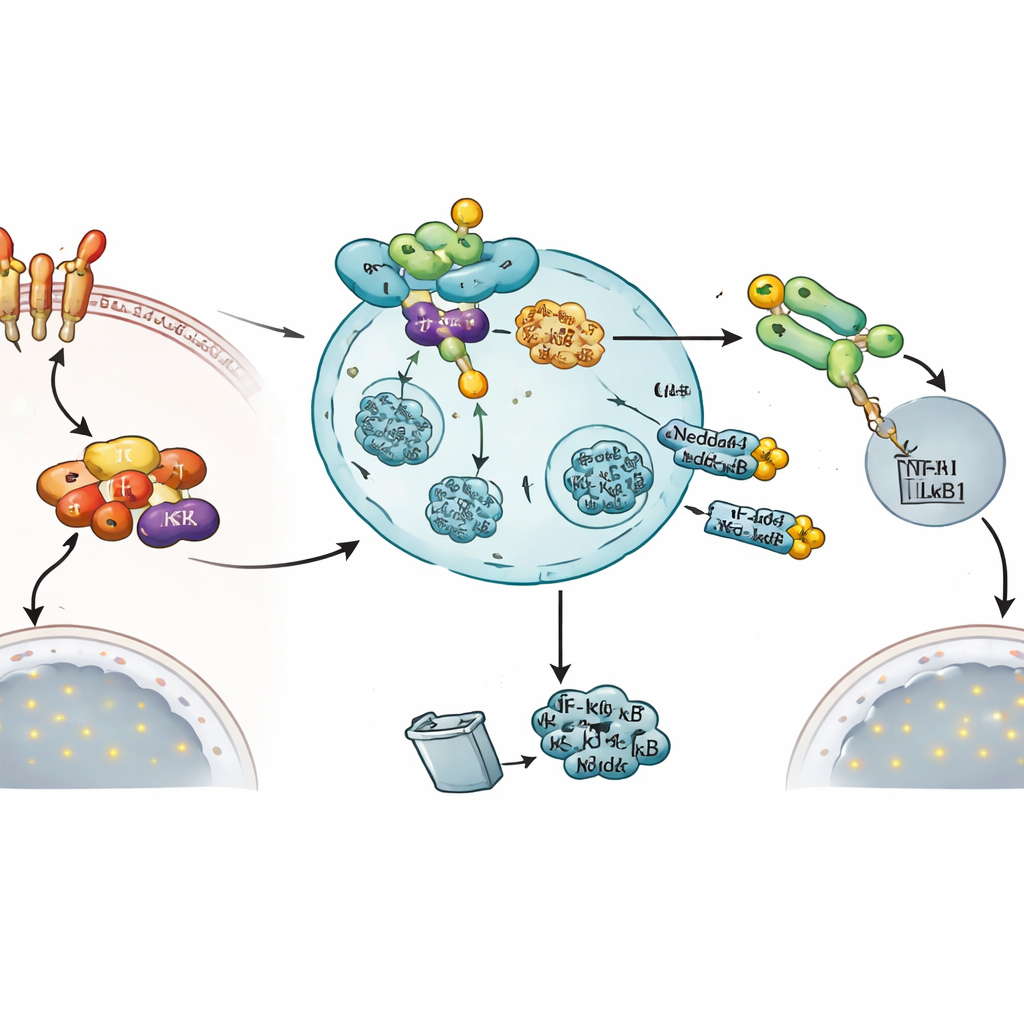
Un circuito de retroalimentación incorporado para terminar la señal
De forma llamativa, la misma señal que activa NF‑κB también parece inducir este freno. Cuando las células se trataron con TNFα, los niveles de ARN mensajero de Nedd4-1(NE) aumentaron de forma notable, mientras que la forma estándar de Nedd4-1 no cambió. Mediciones funcionales respaldaron la idea de que Nedd4-1(NE) actúa como una válvula de cierre: aumentar Nedd4-1(NE) activo redujo la entrada de NF‑κB1 en el núcleo, disminuyó la actividad de un gen reportero sensible a NF‑κB y redujo la expresión de un gen inflamatorio regulado por NF‑κB, TNFAIP3. En conjunto, estos hallazgos describen un bucle de retroalimentación negativa en el que la activación de la vía NF‑κB finalmente aumenta Nedd4-1(NE), que a su vez apunta a dos nodos críticos—IKKβ y NF‑κB1—para rebajar la respuesta inflamatoria.
Qué significa esto para la salud y la enfermedad
Para un público general, el mensaje clave es que nuestras células incorporan un mecanismo de seguridad adicional, específico de primates, para evitar que la señalización inflamatoria se descontrole. Al etiquetar y recortar selectivamente componentes centrales del sistema NF‑κB, Nedd4-1(NE) ayuda a terminar la respuesta a TNFα y puede contribuir al equilibrio inmunitario a largo plazo. Comprender este freno incorporado podría abrir nuevas vías para tratar enfermedades en las que NF‑κB está crónicamente sobreactivado, como trastornos autoinmunes y ciertos cánceres, al sugerir formas de imitar o potenciar este proceso natural de apagado.
Cita: Persaud, A., Kefalas, G., Shteiman, A. et al. Negative regulation of the NF-κB pathway by the ubiquitin ligase Nedd4-1(NE). Commun Biol 9, 374 (2026). https://doi.org/10.1038/s42003-026-09634-7
Palabras clave: Señalización NF-kB, inflamación, ligasa de ubiquitina, Nedd4-1(NE), TNF alfa