Clear Sky Science · es
Notch3 regula la plasticidad fenotípica de los pericitos en el cáncer colorrectal
Por qué importan los vasos sanguíneos alrededor de los tumores
El cáncer colorrectal es uno de los cánceres más comunes y letales en todo el mundo, pero la mayoría de las terapias se dirigen directamente a las células tumorales y con frecuencia pasan por alto el sistema de apoyo circundante que ayuda a que los tumores crezcan. Este trabajo se centra en un grupo de células de soporte menos conocidas llamadas pericitos, que envuelven los pequeños vasos sanguíneos. Al desvelar cómo un interruptor de señalización llamado Notch3 modifica el comportamiento de los pericitos, los autores muestran cómo el suministro sanguíneo del tumor puede inclinarse hacia vasos permeables y caóticos que favorecen al cáncer, o hacia vasos más normales que pueden frenar la enfermedad y mejorar el tratamiento. 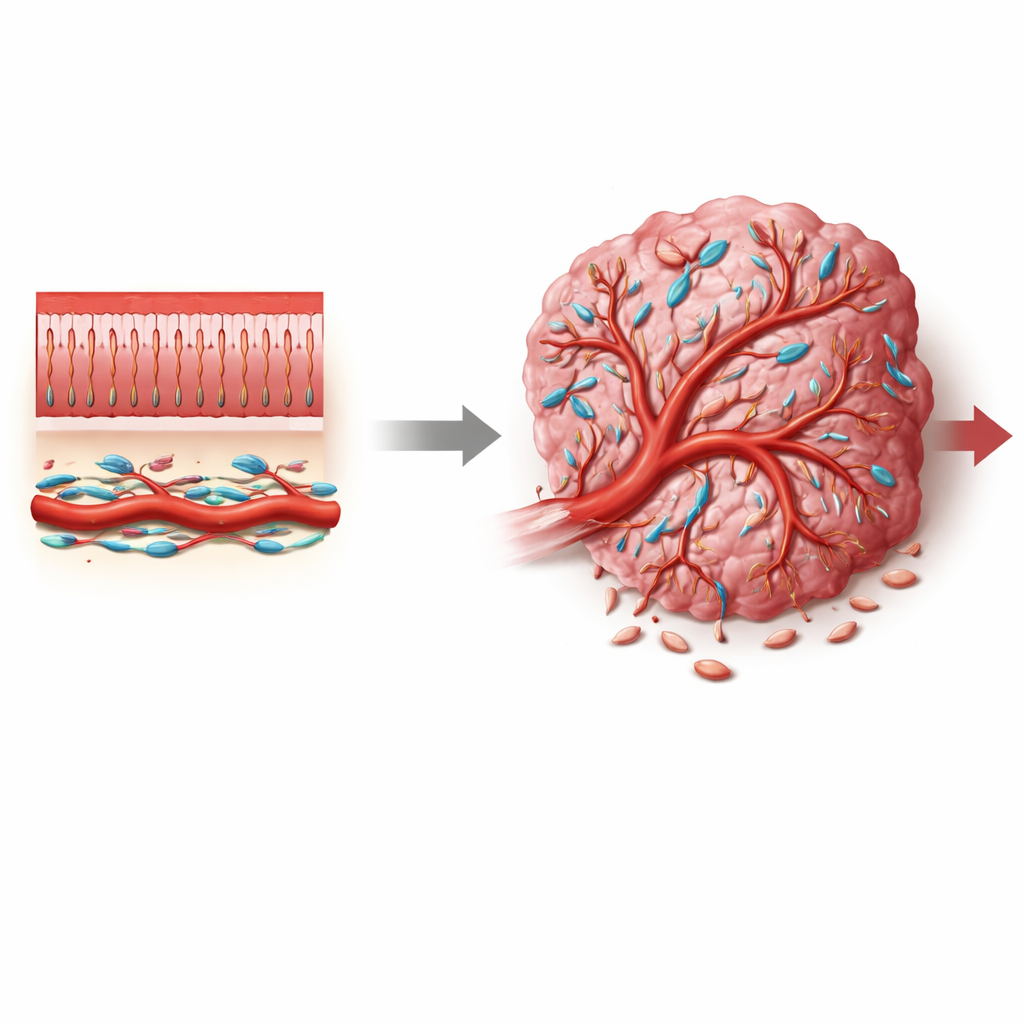
Los colaboradores ocultos alrededor de los vasos tumorales
Los vasos sanguíneos son más que tubos huecos. En tejidos sanos, los vasos pequeños están estrechamente rodeados por pericitos: células especializadas que estabilizan las paredes vasculares, controlan el flujo sanguíneo y evitan las fugas. En los tumores, sin embargo, estos pericitos con frecuencia lucen y se comportan de forma diferente: pueden desprenderse, proliferar o cambiar su identidad, contribuyendo a la vasculatura anómala y filtran que es típica de los cánceres. En los tumores colorrectales, donde el microambiente está saturado de fibroblastos, células inmunitarias y células vasculares, no estaba claro de dónde proceden los pericitos asociados al tumor, qué estados adoptan y qué señales moleculares los empujan hacia funciones que promueven el tumor.
Rastreando pericitos durante la formación de tumores
Para seguir a los pericitos a lo largo del tiempo, los investigadores utilizaron modelos murinos de cáncer colorrectal asociado a colitis en los que pudieron «marcar» genéticamente tipos celulares específicos y observar su destino. Mostraron que los pericitos encontrados en los tumores proceden en gran medida de pericitos residentes en el tejido normal que se expanden y proliferan a medida que se desarrolla el cáncer, en lugar de llegar desde fuentes distantes como la médula ósea. Mediante secuenciación de ARN de una sola célula avanzada, catalogaron decenas de miles de células del estroma de tumores de ratón y colon normal y encontraron que los pericitos están significativamente enriquecidos en el microambiente tumoral. También identificaron una expansión similar de pericitos en varios conjuntos de datos de cáncer colorrectal humano, lo que subraya que esto no es solo un fenómeno específico de los ratones.
Un interruptor molecular que cambia el comportamiento de los pericitos
El equipo preguntó luego qué señales configuran el comportamiento de los pericitos dentro de los tumores y halló que Notch3—un receptor que permite a las células comunicarse con sus vecinas—está particularmente activo en los pericitos tumorales. El análisis computacional de la comunicación célula–célula sugirió que los pericitos tanto envían como reciben señales relacionadas con Notch, sobre todo a través de socios en las células vasculares. Al activar artificialmente Notch3 en pericitos, los investigadores observaron que estas células proliferaban más pero expresaban menos proteínas contráctiles asociadas típicamente con el comportamiento estabilizador de los vasos. Los vasos sanguíneos tumorales en estos ratones se hicieron más grandes, más permeables y recubiertos por más células endoteliales en proliferación, lo que indica una vasculatura menos estable. Por el contrario, eliminar Notch3 redujo la proliferación de las células endoteliales, disminuyó el tamaño de los vasos y redujo las fugas, lo que sugiere un cambio hacia vasos más normalizados sin alterar de forma drástica el número o el tamaño inicial de los tumores. 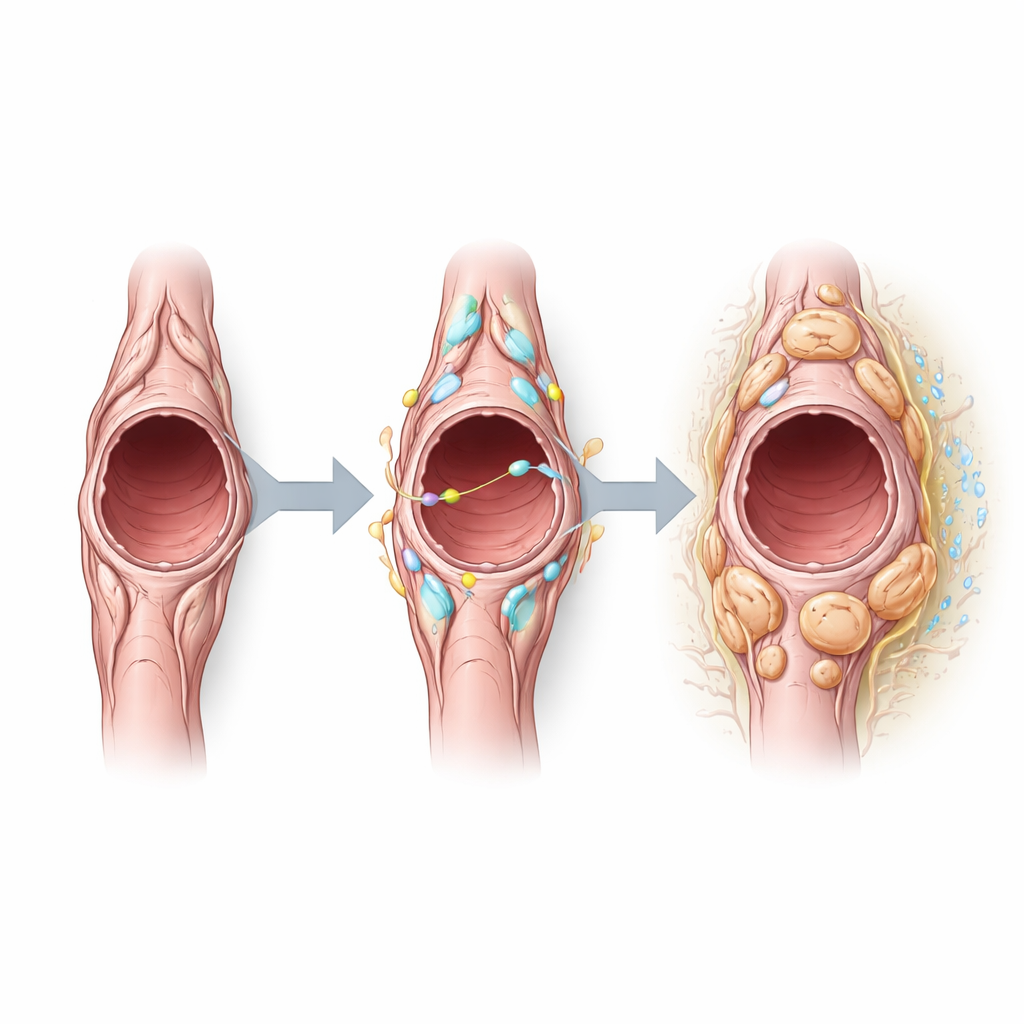
Las muchas caras de los pericitos dentro de los tumores
Más allá de cambios simples de encendido/apagado, el estudio reveló que los pericitos tumorales existen en varios estados distintos. Algunos subgrupos mostraron rasgos de células altamente contráctiles, otros produjeron grandes cantidades de matriz extracelular, algunos exhibieron características inflamatorias y un subconjunto incluso mostró firmas habitualmente vistas en células endoteliales. La actividad de Notch3 no se distribuyó de manera uniforme: se enriqueció en una población de pericitos «sintéticos» o productora de matriz y fue baja en el subconjunto más contráctil. Los análisis de trayectoria sugirieron que los pericitos pueden pasar de un estado contráctil a uno sintético y proliferativo a medida que aumenta la actividad de Notch3. Cuando los autores examinaron datos humanos de cáncer colorrectal, encontraron un espectro comparable de estados de pericitos y, nuevamente, observaron mayor actividad de un gen diana de Notch3 en pericitos asociados al tumor y en pericitos proliferantes, lo que refleja los resultados en ratones.
Convertir el caos vascular en una oportunidad terapéutica
En conjunto, el trabajo sitúa a Notch3 como un regulador clave que ajusta la identidad de los pericitos y, a través de ellos, la estructura y función de los vasos sanguíneos tumorales. Una alta actividad de Notch3 empuja a los pericitos hacia un estado proliferativo y menos contráctil vinculado a vasos agrandados y permeables que favorecen la progresión tumoral. Una baja actividad de Notch3 se asocia con pericitos más contráctiles, células endoteliales más calmadas y una vasculatura más normalizada que puede restringir el crecimiento tumoral y mejorar la entrega de fármacos. Al dirigir Notch3 específicamente en pericitos, las terapias futuras podrían orientar los vasos tumorales lejos del caos y hacia la estabilidad, ofreciendo un nuevo enfoque para tratar el cáncer colorrectal avanzado en combinación con los fármacos existentes.
Cita: Chalkidi, N., Stavropoulou, A., Arvaniti, VZ. et al. Notch3 regulates pericyte phenotypic plasticity in colorectal cancer. Commun Biol 9, 343 (2026). https://doi.org/10.1038/s42003-026-09629-4
Palabras clave: cáncer colorrectal, microambiente tumoral, pericitos, señalización Notch3, vasos sanguíneos tumorales