Clear Sky Science · es
TRIM47 endotelial regula la integridad de la barrera hematoencefálica y la cognición a través de la vía de señalización KEAP1/NRF2 en ratones
Por qué importa proteger los pequeños vasos del cerebro
La enfermedad cerebral de pequeños vasos es un problema silencioso en el cerebro. Deteriora los vasos sanguíneos más diminutos, aumenta el riesgo de ictus y erosiona lentamente la memoria y las funciones cognitivas; sin embargo, los médicos aún carecen de tratamientos que aborden sus causas biológicas fundamentales. Este estudio explora una proteína concreta, TRIM47, presente en las células que recubren los vasos sanguíneos cerebrales, para plantear una pregunta simple pero crucial: ¿ayuda a mantener intacta la barrera hematoencefálica del cerebro, y esto importa para la cognición?
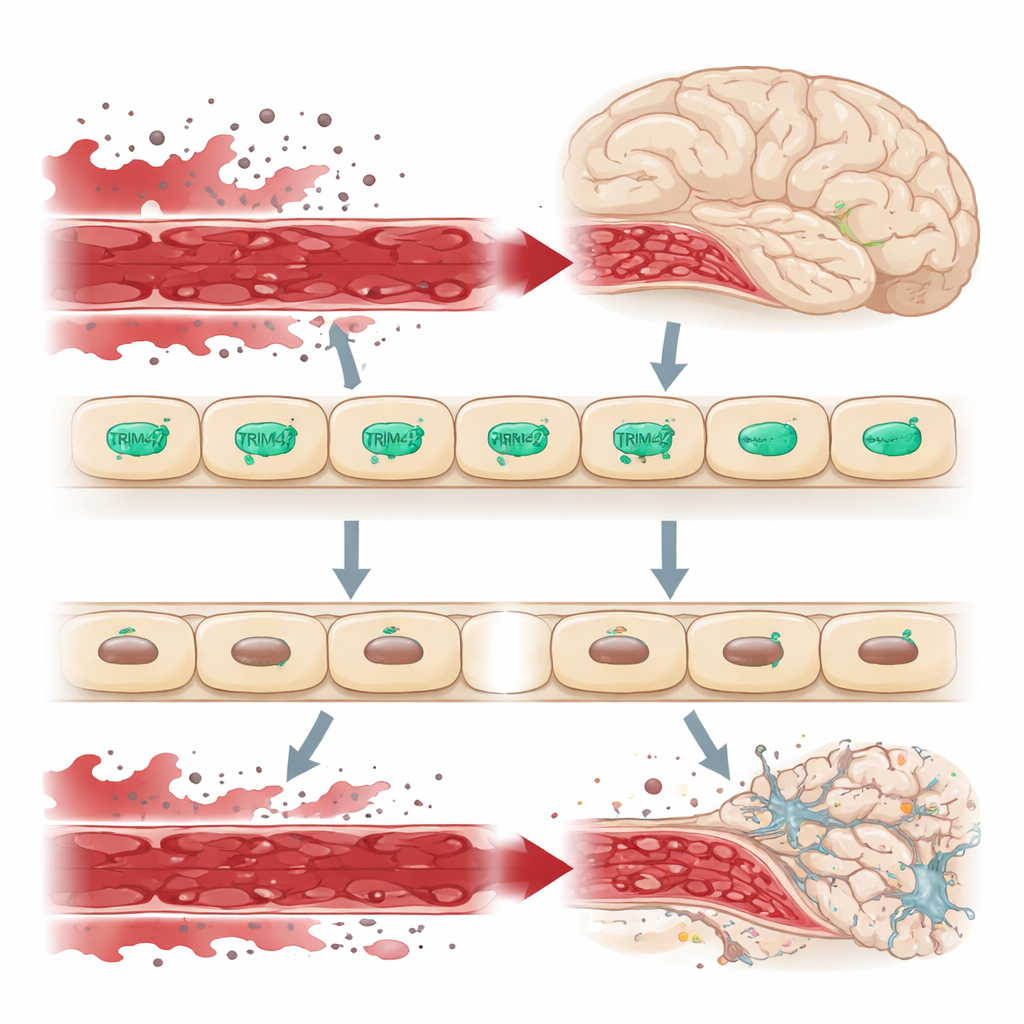
Un guardián en la frontera del cerebro
El cerebro está protegido del resto de la circulación por la barrera hematoencefálica, un revestimiento de células endoteliales fuertemente sellado que controla estrictamente lo que puede entrar en el tejido cerebral. Cuando esta barrera se filtra, moléculas nocivas de la sangre se infiltran en el cerebro, estresando a las neuronas y las células de soporte y contribuyendo a enfermedades como la demencia. Estudios genéticos en grandes poblaciones humanas habían señalado a un tramo de ADN que contiene el gen TRIM47 como una región de riesgo para la enfermedad cerebral de pequeños vasos. TRIM47 es especialmente activo en las células endoteliales cerebrales, lo que sugiere que podría ser un guardián importante de esta barrera.
Cómo TRIM47 arma a las células contra el estrés oxidativo
Los autores estudiaron primero células endoteliales humanas del cerebro cultivadas en el laboratorio y redujeron los niveles de TRIM47 mediante interferencia de ARN. Esto desencadenó cambios amplios en la actividad génica, con la red más afectada centrada en NRF2, un regulador maestro de las defensas antioxidantes celulares. En condiciones normales, NRF2 está controlado por otra proteína, KEAP1, que dirige su destrucción. El equipo mostró que TRIM47 se une a KEAP1 y ayuda a evitar que NRF2 sea degradado. Con TRIM47 presente, NRF2 puede acumularse, desplazarse al núcleo y activar genes que desintoxican las especies reactivas de oxígeno. Cuando TRIM47 se pierde, los niveles de NRF2 caen, los genes antioxidantes se muestran menos activos y las células endoteliales se vuelven más vulnerables al estrés oxidativo.
De vasos permeables a problemas de memoria en ratones
Para ver cómo se manifiesta este mecanismo en un cerebro vivo, los investigadores generaron ratones sin el gen Trim47 en todo el organismo y otra línea en la que Trim47 podía eliminarse solo en las células endoteliales. Los animales adultos de ambos modelos desarrollaron problemas claros en el aprendizaje espacial y la memoria, fallando en tareas como el laberinto en Y y el laberinto acuático de Morris a pesar de tener movilidad normal. El examen de sus cerebros reveló que la barrera hematoencefálica se había vuelto permeable: pequeños trazadores fluorescentes y proteínas sanguíneas escapaban de los vasos hacia el tejido circundante. Las proteínas clave que “sellan” las uniones estrechas y de adhesión entre las células endoteliales, especialmente Claudin-5 y Occludin, se encontraban reducidas. Los astrocitos cercanos, las células de soporte en forma de estrella que reaccionan rápidamente a la lesión, se activaron, aunque había pocas señales de inflamación generalizada o pérdida neuronal en esta etapa.
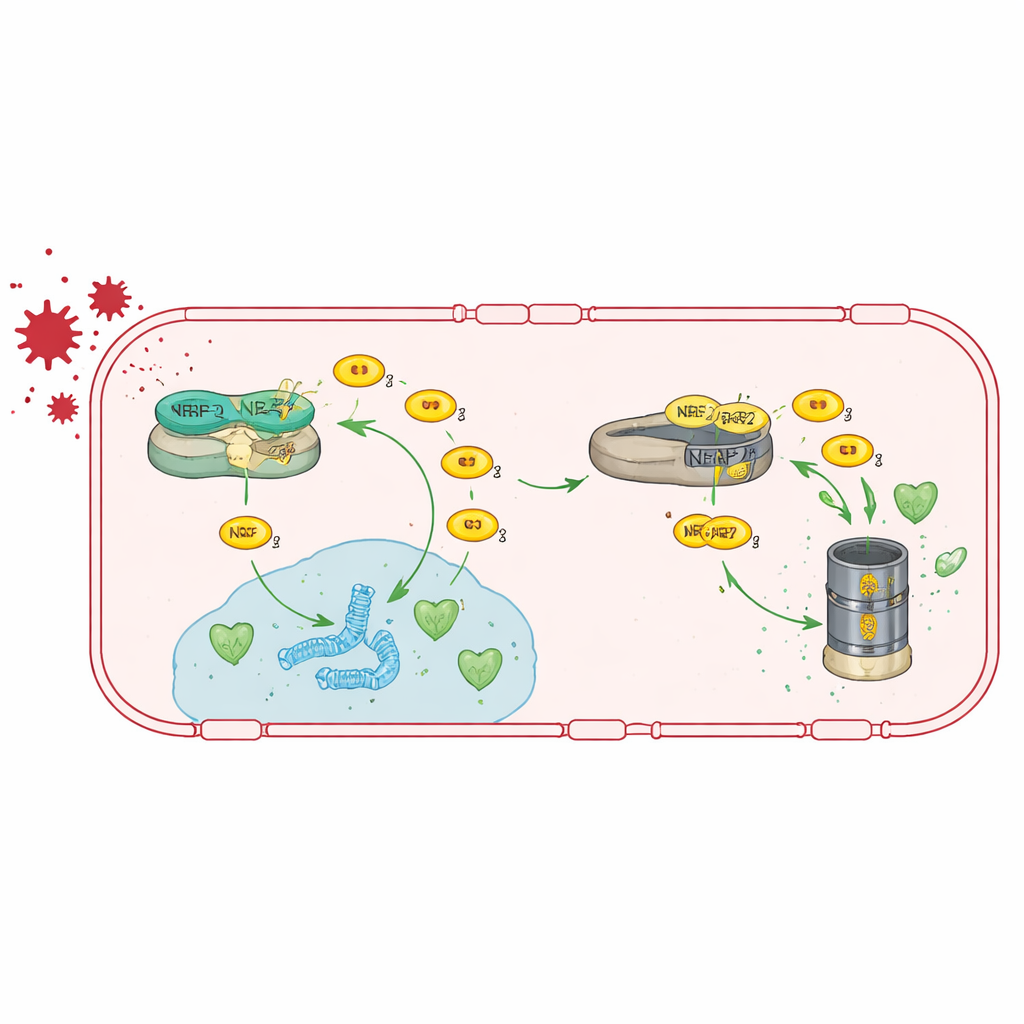
Volver a activar la vía antioxidante
Como TRIM47 actúa principalmente potenciando la actividad de NRF2, el equipo probó si podían sortear su pérdida estimulando directamente NRF2. Alimentaron a los ratones deficientes en Trim47 con una dieta que contenía terc-butilhidroquinona (tBHQ), un compuesto conocido por estabilizar NRF2 y activar sus genes diana. Este tratamiento restauró la actividad de los genes antioxidantes en las células endoteliales cerebrales, devolvió la expresión de genes de las uniones estrechas hacia la normalidad y redujo la filtración de la barrera hematoencefálica. De forma llamativa, también normalizó la activación de los astrocitos y recuperó el rendimiento de los animales en las pruebas de memoria, lo que sugiere que reforzar esta vía antioxidante puede revertir tanto los problemas vasculares como los cognitivos, al menos en ratones.
Pistas desde la sangre humana y siguientes pasos
Para vincular sus experimentos en ratones con la enfermedad humana, los investigadores analizaron proteínas relacionadas con la vía NRF2 en muestras de sangre de miles de personas que se habían sometido a resonancia magnética cerebral. Los niveles de varias proteínas reguladas por NRF2 se asociaron con marcadores de imagen de la enfermedad de pequeños vasos, como espacios perivasculares agrandados y cambios en la materia blanca. Esto respalda la idea de que la señalización TRIM47–NRF2 alterada es relevante en humanos, no solo en animales experimentales, y que estas proteínas podrían servir como biomarcadores de la gravedad o progresión de la enfermedad.
Qué significa esto para la salud cerebral
En conjunto, el trabajo retrata a TRIM47 como un guardaespaldas molecular que ayuda a los vasos sanguíneos cerebrales a resistir el daño oxidativo estabilizando el sistema antioxidante NRF2. Cuando TRIM47 falta o está perjudicado, la barrera hematoencefálica se debilita, se acumula daño cerebral sutil y la memoria comienza a fallar. Reactivar la vía NRF2 puede reparar la barrera y restaurar la cognición en ratones, lo que pone de manifiesto este eje de señalización como un objetivo terapéutico prometedor para las formas vasculares de demencia. Aunque la tBHQ en sí no es adecuada como fármaco para humanos, compuestos más seguros que aumenten NRF2 o estrategias que imiten el papel protector de TRIM47 podrían algún día ayudar a preservar la salud cerebral reforzando sus vasos más pequeños y frágiles.
Cita: Delobel, V., Grenier, C., Boulestreau, R. et al. Endothelial TRIM47 regulates blood-brain barrier integrity and cognition via the KEAP1/NRF2 signalling pathway in mice. Commun Biol 9, 399 (2026). https://doi.org/10.1038/s42003-026-09628-5
Palabras clave: enfermedad cerebral de pequeños vasos, barrera hematoencefálica, TRIM47, vía NRF2, demencia vascular