Clear Sky Science · es
Se requiere una vía inter‑subunidad para la unión entropía‑impulsada y negativamente cooperativa de nucleótidos cíclicos en el canal HCN2
Cómo los diminutos interruptores marcapasos del corazón detectan señales químicas
Cada latido y muchos ritmos cerebrales dependen de canales microscópicos que se abren y cierran en las membranas de nuestras células. Estos canales, denominados canales marcapasos HCN, están controlados no solo por el voltaje eléctrico, sino también por pequeñas moléculas mensajeras conocidas como nucleótidos cíclicos. Este estudio plantea una pregunta aparentemente simple con implicaciones profundas: ¿cómo se unen estas diminutas moléculas al canal HCN2 de manera coordinada, y cómo pueden fallos sutiles en ese proceso contribuir a trastornos como la epilepsia?
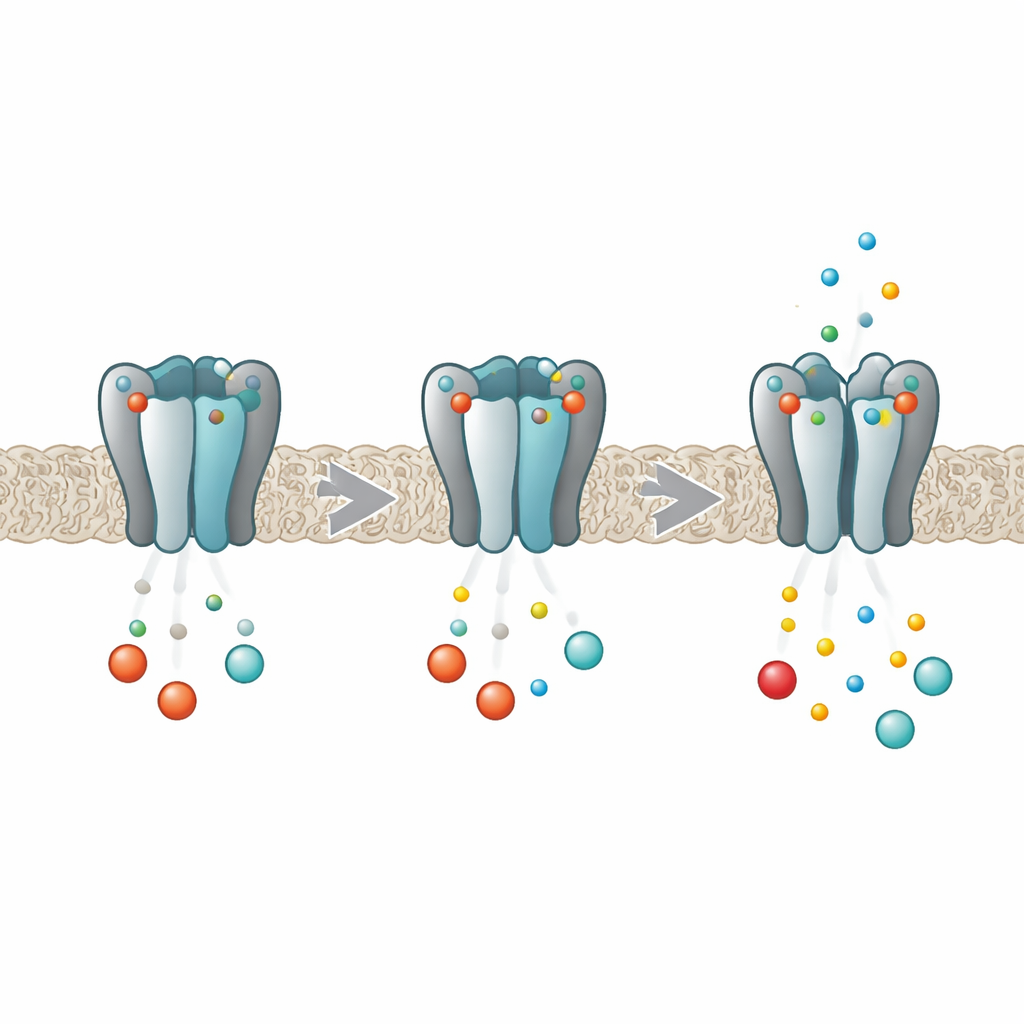
Un regulador molecular para los ritmos del cuerpo
Los canales HCN actúan como reguladores de intensidad para la actividad eléctrica en las células del corazón y del cerebro. Cada canal está formado por cuatro subunidades proteicas idénticas que juntas crean un poro central por el que fluyen iones. En lo profundo de cada subunidad hay un bolsillo capaz de captar nucleótidos cíclicos como el cAMP y el cGMP. Cuando estas moléculas se unen, facilitan la apertura del poro, aumentando la corriente marcapasos. Trabajos anteriores mostraron que en la variante HCN2 la unión no ocurre de forma independiente en cada bolsillo; en su lugar, los cuatro sitios se influyen mutuamente de modo que la primera molécula se une con más facilidad que las siguientes, un comportamiento conocido como cooperatividad negativa. El trabajo nuevo se propuso descubrir exactamente cómo las cuatro subunidades se comunican entre sí durante este proceso.
Subunidades que perciben a sus vecinas
Los investigadores combinaron simulaciones por ordenador con mediciones de laboratorio en piezas aisladas del canal HCN2. Mediante largas simulaciones de dinámica molecular observaron cómo la región terminal del canal —la parte que contiene los bolsillos de nucleótidos cíclicos y el llamado C‑linker que conecta con el poro— se flexiona y bambolea cuando están unidos distintos números de moléculas de cAMP o cGMP. Descubrieron que cuando una mensajera se fija en una subunidad, no estabiliza únicamente esa subunidad. En lugar de eso, modifica sutilmente la estabilidad de sus vecinas, a veces haciéndolas más rígidas, otras más flexibles, aunque la forma global de la proteína apenas cambia. Estas influencias entre vecinas dependían de cuántos sitios estaban ocupados y de dónde se situaban alrededor del anillo, coincidiendo con lo que se esperaría de la cooperatividad negativa.
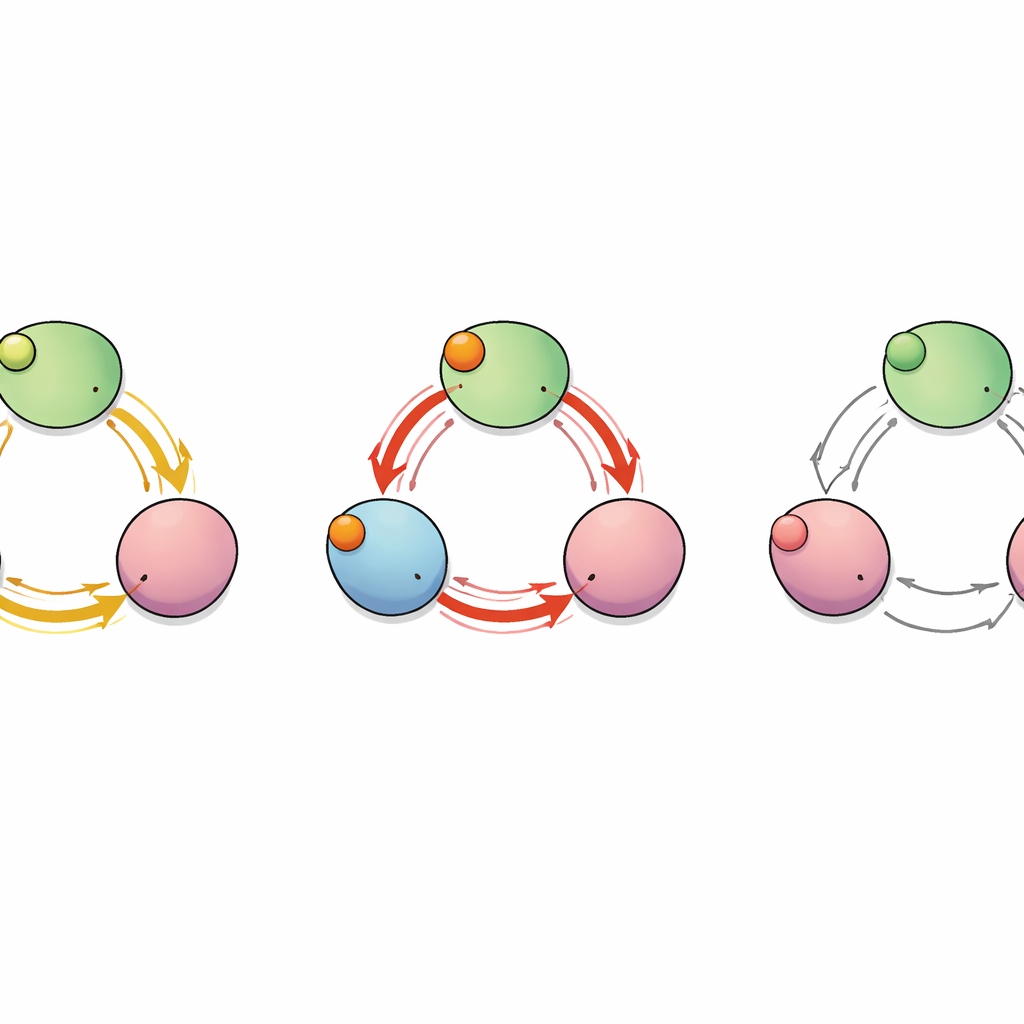
Una vía oculta entre subunidades
Para mapear cómo viaja la “señal” de la unión a través de la proteína, el equipo trató al canal como una red de aminoácidos interaccionantes. Calcularon qué residuos se movían de forma correlacionada durante las simulaciones y usaron herramientas de teoría de grafos para identificar las rutas de comunicación más cortas y eficientes desde los bolsillos de unión hasta los segmentos del C‑linker que controlan el poro. Este análisis reveló varias rutas posibles, pero dos destacaron: una que se mantiene dentro de una única subunidad y otra que salta de una subunidad a su vecina. A lo largo de esta vía inter‑subunidad, un único residuo —un glutamato en la posición 488 (E488)— actuó como un nodo crítico por el que pasaban muchas de las rutas más cortas, lo que sugiere que podría ser un punto clave de relevo para la unión cooperativa.
Mutaciones que rompen la conversación
Los autores pasaron luego a experimentos con colas purificadas del canal para probar la importancia de esta vía. Alteraron E488 y la tirosina vecina en la posición 459 (Y459), que se encuentra en la subunidad contigua donde llega la vía. Usando dispersión dinámica de luz confirmaron que las proteínas mutantes aún se ensamblaban en complejos de cuatro subunidades, pero ya no mostraban el marcado ajuste entre subunidades inducido por el ligando observado en la proteína normal. La titulación calométrica isotérmica, que rastrea los pequeños calores de unión, reveló un cambio aún mayor: el HCN2 de tipo salvaje exhibió dos eventos de unión distintos, un primer paso de alta afinidad impulsado principalmente por un aumento de entropía (mayor movimiento interno), seguido por tres pasos de menor afinidad. En contraste, las mutaciones en E488 o Y459 mostraron únicamente un modo de unión único y de afinidad modesta que carecía de ese impulso entrópico favorable y perdió la cooperatividad negativa característica.
Por qué importan los cambios sutiles de entropía
Al juntar estas piezas, el estudio dibuja la imagen del canal HCN2 como un anillo dinámico de cuatro subunidades conectadas por específicas “vías de conversación”. Cuando el primer nucleótido cíclico se une, ajusta los movimientos de partes distantes del anillo a través de E488 y Y459, haciendo que los eventos de unión posteriores sean menos favorables y modulando cómo responde el poro. Este efecto no está impulsado por grandes reordenamientos estructurales sino por cambios en la flexibilidad interna —variaciones en la entropía que son invisibles en instantáneas estáticas pero cruciales para la función. Las mutaciones que interrumpen los residuos clave a lo largo de esta vía inter‑subunidad silencian la conversación, abolieron la cooperatividad negativa y se asocian a enfermedades como la epilepsia generalizada idiopática. Para un lector no especialista, la conclusión es que los interruptores vitales del corazón y del cerebro dependen de exquisitas “susurradas” moléculas entre subunidades proteicas, y entender esos susurros ayuda a explicar tanto los ritmos normales como lo que ocurre cuando fallan.
Cita: Costa, F., Ng, L.C.T., Chow, S.S. et al. An inter-subunit path is required for entropically-driven and negatively cooperative binding of cyclic nucleotides in the HCN2 channel. Commun Biol 9, 362 (2026). https://doi.org/10.1038/s42003-026-09626-7
Palabras clave: canal iónico HCN2, unión de nucleótidos cíclicos, cooperatividad negativa, comunicación alostérica, mutación asociada a epilepsia