Clear Sky Science · es
Una pequeña molécula activa alostéricamente la secreción dependiente de SecA
Convertir el muelle de envío bacteriano en sobreaceleración
Las bacterias sobreviven exportando constantemente proteínas a través de pequeñas puertas en sus membranas. Estas exportaciones les ayudan a construir paredes celulares, secretar toxinas y adaptarse al estrés, procesos centrales en muchas infecciones. Este estudio informa sobre una pequeña molécula, denominada HSI#6, que hace algo inusual: en lugar de bloquear esta maquinaria de exportación, la transforma en un modo hiperactivo y menos selectivo. Entender cómo funciona este interruptor podría tanto revelar nuevas estrategias antibacterianas como ofrecer a la biotecnología una forma de potenciar la secreción de proteínas bajo demanda.
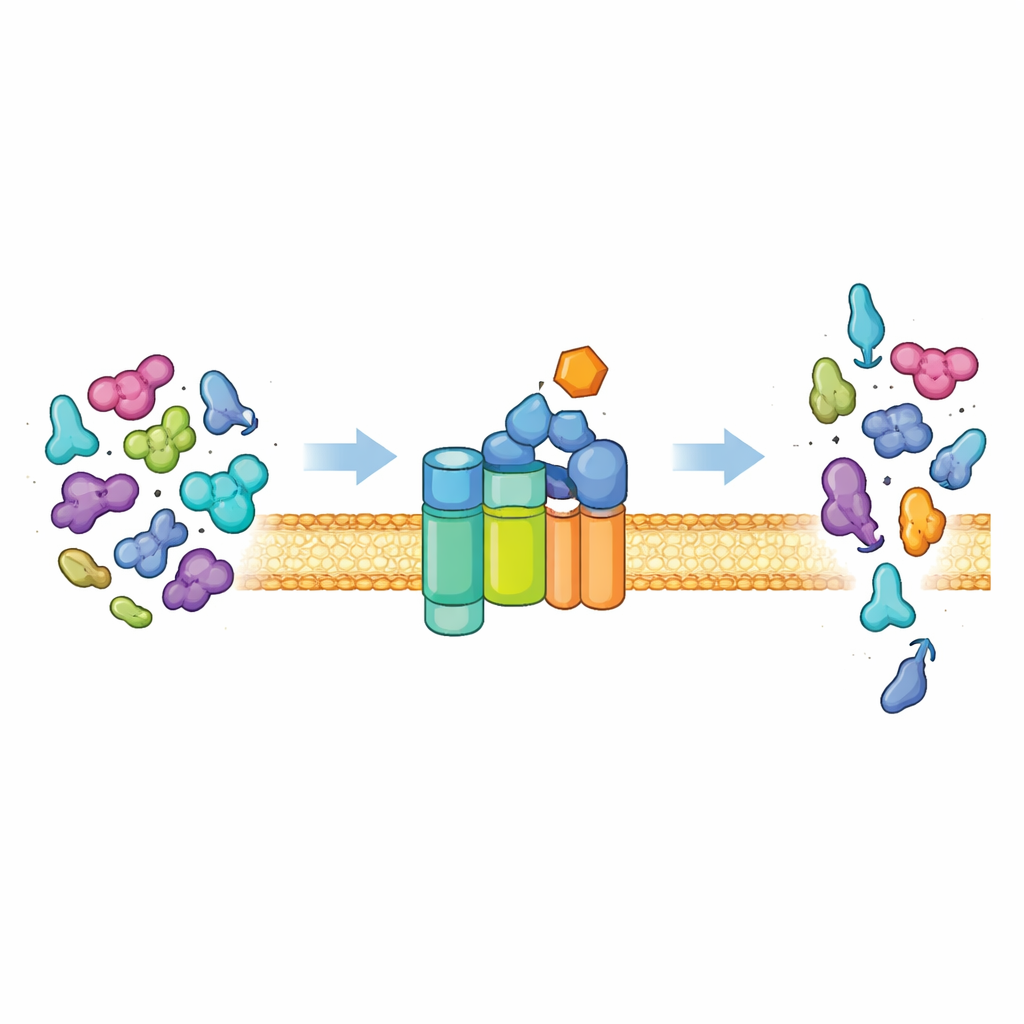
La puerta de salida de proteínas de la célula
La mayoría de las bacterias exportan proteínas fuera de la célula mediante una vía universal conocida como el sistema Sec. En su núcleo hay un canal en la membrana (SecYEG) y una proteína motora (SecA) que quema combustible celular (ATP) para impulsar cadenas proteicas no plegadas a través del canal. En condiciones normales, este sistema es exigente. Principalmente exporta “preproteínas” que llevan etiquetas de dirección especiales, conocidas como péptidos señal, además de rasgos adicionales en su dominio principal. Estas características son necesarias para cambiar a SecA de un estado silencioso y de baja actividad a un motor potente. Solo las proteínas que presentan la combinación correcta de señales pueden desbloquear la actividad completa, asegurando que la célula exporte la carga adecuada y mantenga las proteínas citoplasmáticas ordinarias de forma segura en el interior.
Una pequeña molécula que despierta el motor
Los investigadores descubrieron HSI#6 en una búsqueda de compuestos que interfieren con la secreción de proteínas bacterianas y el crecimiento. Pruebas bioquímicas mostraron que HSI#6 se une directamente a SecA con afinidad micromolar y altera la eficiencia con la que utiliza ATP. En solución, hace que SecA retenga ATP con más fuerza; cuando SecA está asociado al canal, HSI#6 mejora tanto la unión del ATP como la velocidad de su consumo. Este patrón es la marca de un activador alostérico: una molécula que se une en un sitio de una proteína pero altera la actividad en otro sitio lejano. A diferencia de los clientes proteicos naturales, HSI#6 no necesita actuar como carga para estimular el motor: simplemente ajusta la dinámica interna de SecA para que toda la translocasa quede catalíticamente preparada.
Del filtro selectivo a la nanomáquina promiscua
Una vez unido HSI#6, el sistema Sec deja de exigir las etiquetas de exportación habituales. En experimentos de tubo de ensayo, el compuesto aproximadamente duplicó la secreción de una preproteína estándar y volvió al complejo más resistente al azida de sodio, un inhibidor conocido de SecA. Más llamativo aún, HSI#6 permitió que la maquinaria normal, de tipo salvaje, translocara proteínas que carecen por completo de péptidos señal, así como proteínas que normalmente residen en el citoplasma. En células bacterianas vivas, se observó el mismo efecto usando reporteros basados en fosfatasa alcalina: cuando proteínas citoplasmáticas se fusionaron a una enzima secretada, la presencia de HSI#6 provocó un marcado aumento en la actividad secretada sin cambiar la cantidad de proteína producida. En otras palabras, HSI#6 desacopla eficazmente la exportación de las comprobaciones habituales de identidad del cliente, transformando el sistema Sec en una bomba de exportación de acción amplia para cualquier proteína suficientemente no plegada.
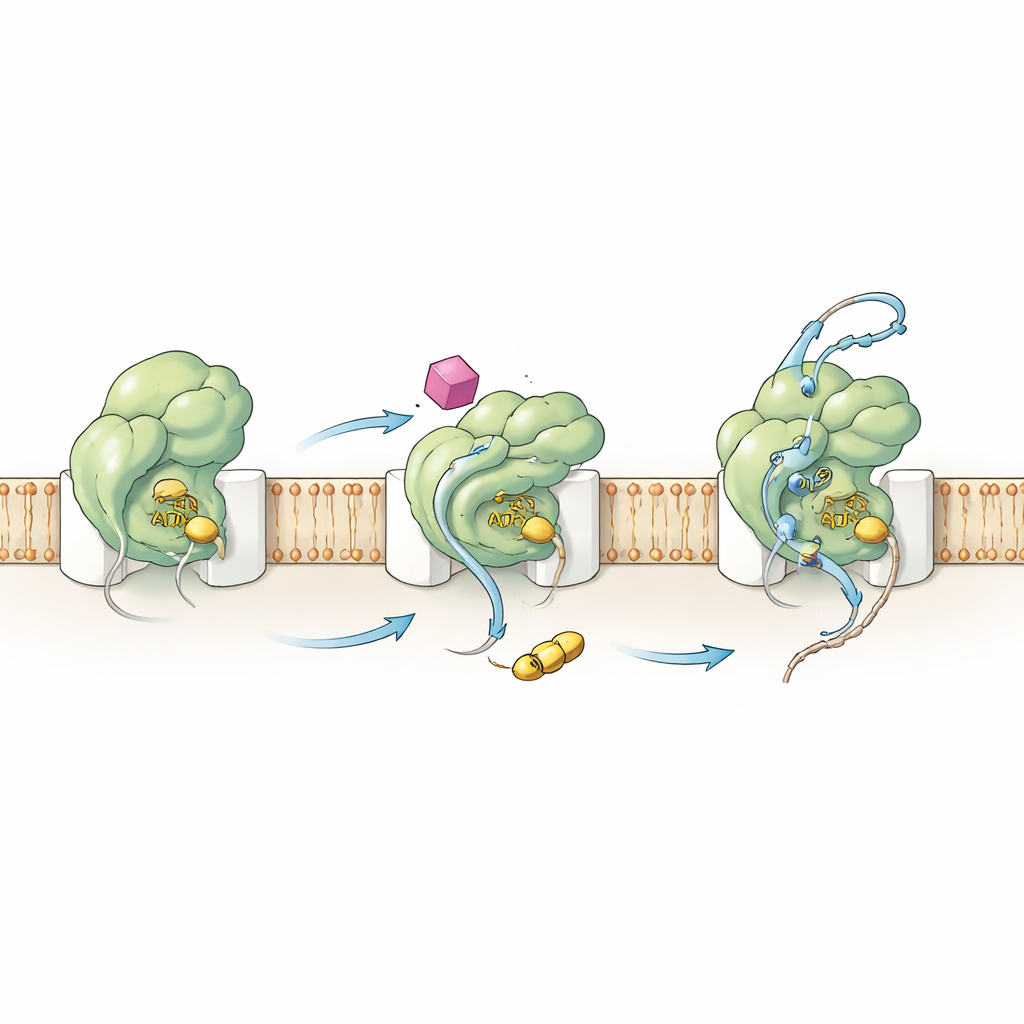
Reprogramar el motor desde dentro
Para entender cómo HSI#6 desencadena este comportamiento, el equipo examinó tanto la química como los movimientos de SecA. Mediciones cinéticas mostraron que el compuesto desplaza el paso clave de activación hacia arriba en la secuencia: el complejo SecA–canal se vuelve catalíticamente activo incluso antes de que se una un cliente proteico. HSI#6 también ayuda a SecA a liberar el combustible gastado (ADP), un paso normalmente lento y limitante, y por tanto favorece un ciclo de ATP más rápido. Usando espectrometría de masas con intercambio hidrógeno–deuterio, los autores cartografiaron cómo HSI#6 remodela la flexibilidad de distintas regiones de SecA. El compuesto afloja selectivamente partes de la proteína que detectan clientes y se conectan al canal, mientras que rigidiza una región de armazón que probablemente aloja su sitio de unión. El patrón de movimiento resultante se asemeja a un estado ya comprometido y “encendido” de la translocasa, lo que sugiere que HSI#6 estabiliza una forma activada—posiblemente incluso favoreciendo una SecA monomérica unida al canal—sin necesidad de un cliente presente.
Por qué esto importa para la medicina y la biotecnología
Al demostrar que una pequeña molécula puede activar alostéricamente a SecA y eliminar su selectividad normal de clientes, este trabajo revela una nueva manera de controlar una maquinaria bacteriana central. Para la enfermedad infecciosa, una secreción forzada y descontrolada podría debilitar a los patógenos al agotar energía y perturbar sus programas de exportación finamente afinados, lo que hace que activadores tipo HSI#6 sean puntos de partida atractivos para el diseño de antibióticos—o como guías para crear futuros inhibidores que bloqueen las mismas características regulatorias. Para la biotecnología, el mismo principio podría reutilizarse para mejorar la secreción de proteínas recombinantes útiles, sin necesidad de péptidos señal diseñados o modificaciones genéticas complejas. En esencia, el estudio demuestra que el “muelle de envío” proteico bacteriano puede reprogramarse químicamente, abriendo nuevas vías tanto para combatir microbios como para aprovecharlos como fábricas microscópicas.
Cita: Sedky, H., Hamed, M.B., Krishnamurthy, S. et al. A small molecule allosterically activates SecA dependent secretion. Commun Biol 9, 368 (2026). https://doi.org/10.1038/s42003-026-09623-w
Palabras clave: secreción de proteínas bacterianas, translocasa SecA, activación alostérica, reguladores de pequeña molécula, descubrimiento de fármacos antibacterianos