Clear Sky Science · es
LncRNA P4HA2-AS1 impulsa la fibrosis intersticial renal mediante ubiquitinación K63 mediada por TRIM32 de ULK1 y desregulación de la autofagia
Por qué importa la cicatrización renal
La enfermedad renal crónica afecta a cientos de millones de personas en todo el mundo y a menudo avanza de forma silenciosa hasta que la diálisis o un trasplante son las únicas alternativas para sobrevivir. En el centro de este deterioro está un proceso llamado cicatrización, en el que el tejido renal normal se reemplaza gradualmente por material rígido y no funcional. Este estudio plantea una pregunta simple pero crucial: ¿qué interruptores moleculares dentro de las células renales las empujan hacia esta cicatrización dañina, y se pueden volver a apagar esos interruptores?
Un interruptor ARN oculto en las células renales
Los riñones filtran la sangre mediante redes elaboradas de diminutos túbulos. Cuando estos túbulos resultan dañados por obstrucción del flujo de orina, niveles altos de glucosa o una pérdida súbita del suministro sanguíneo, pueden responder depositando tejido cicatricial entre las células. Los investigadores examinaron los riñones de ratones con varios tipos de lesión y los compararon con riñones sanos mediante secuenciación de ARN, una técnica que revela qué genes están activados. Descubrieron que una molécula poco conocida llamada P4HA2-AS1, un ARN largo no codificante que no produce proteína, estaba consistentemente elevada en riñones dañados y formadores de cicatriz y en células renales humanas estresadas en el laboratorio. Este ARN se localizaba principalmente en la parte citoplasmática de las células, lo que sugiere que podría controlar otras proteínas allí. 
Reducir el ARN para proteger el riñón
Para comprobar si P4HA2-AS1 es simplemente un marcador o un impulsor activo del daño, el equipo redujo sus niveles en ratones y en células renales humanas en cultivo. En un modelo bien establecido en el que se ligaba un uréter para causar obstrucción crónica, la disminución de este ARN mediante entrega viral dirigida alivió muchas señales de la fibrosis: los túbulos se mantuvieron más íntegros, hubo menos colágeno y otras proteínas fibróticas entre las células, y mejoraron los marcadores de función renal en sangre. En cultivos de células renales humanas, reducir P4HA2-AS1 también atenuó la respuesta a una señal profibrogénica potente, TGF-β, dando lugar a menor producción de fibronectina, colágeno y otros factores pro‑fibroticos. Estos experimentos demostraron que este ARN no es solo un marcador del daño, sino que alimenta activamente el proceso de cicatrización.
Autofagia: de limpieza a daño
Los investigadores preguntaron luego cómo causa daño este ARN. Sus datos de expresión génica e imágenes apuntaron a la autofagia, el sistema de reciclaje integrado de la célula que degrada proteínas y orgánulos envejecidos. En condiciones normales, la autofagia es un proceso de mantenimiento saludable, pero cuando se activa en exceso y durante mucho tiempo puede empujar a los riñones lesionados hacia una reparación maladaptativa y fibrosis. En células renales estresadas, P4HA2-AS1 aumentó el flujo de material a través de la autofagia, provocando acumulación de vesículas de reciclaje. Cuando el ARN fue bloqueado, este reciclaje hiperactivo volvió hacia niveles normales, tanto en células como en riñones de ratones obstruidos. Ratones carentes de ULK1, una quinasa iniciadora central de la autofagia, también estuvieron protegidos de la fibrosis, y en estos animales la sobreexpresión de P4HA2-AS1 ya no pudo agravar el daño, vinculando de forma contundente los efectos del ARN con esta vía.
Una cadena molecular de tres eslabones
Ahondando más, el equipo usó técnicas bioquímicas de captura para identificar proteínas que se unen físicamente a P4HA2-AS1. Una destacó: TRIM32, una enzima que marca otras proteínas con pequeñas “banderas” moleculares llamadas ubiquitinas. El ARN se une a TRIM32 y lo protege de la degradación, aumentando sus niveles dentro de las células renales. TRIM32 estabilizado, a su vez, añade un tipo específico de cadena de ubiquitina a ULK1. En lugar de dirigir a ULK1 hacia la destrucción, esta cadena actúa como un refuerzo, mejorando la capacidad de ULK1 para activar la autofagia. Cuando los científicos eliminaron TRIM32 en ratones o lo silenciaron en células renales, tanto la fibrosis como la autofagia excesiva se redujeron. Reintroducir TRIM32 en células donde P4HA2-AS1 había sido bloqueado restauró parcialmente la respuesta fibrótica, demostrando que esta enzima es un eslabón clave en la cadena. 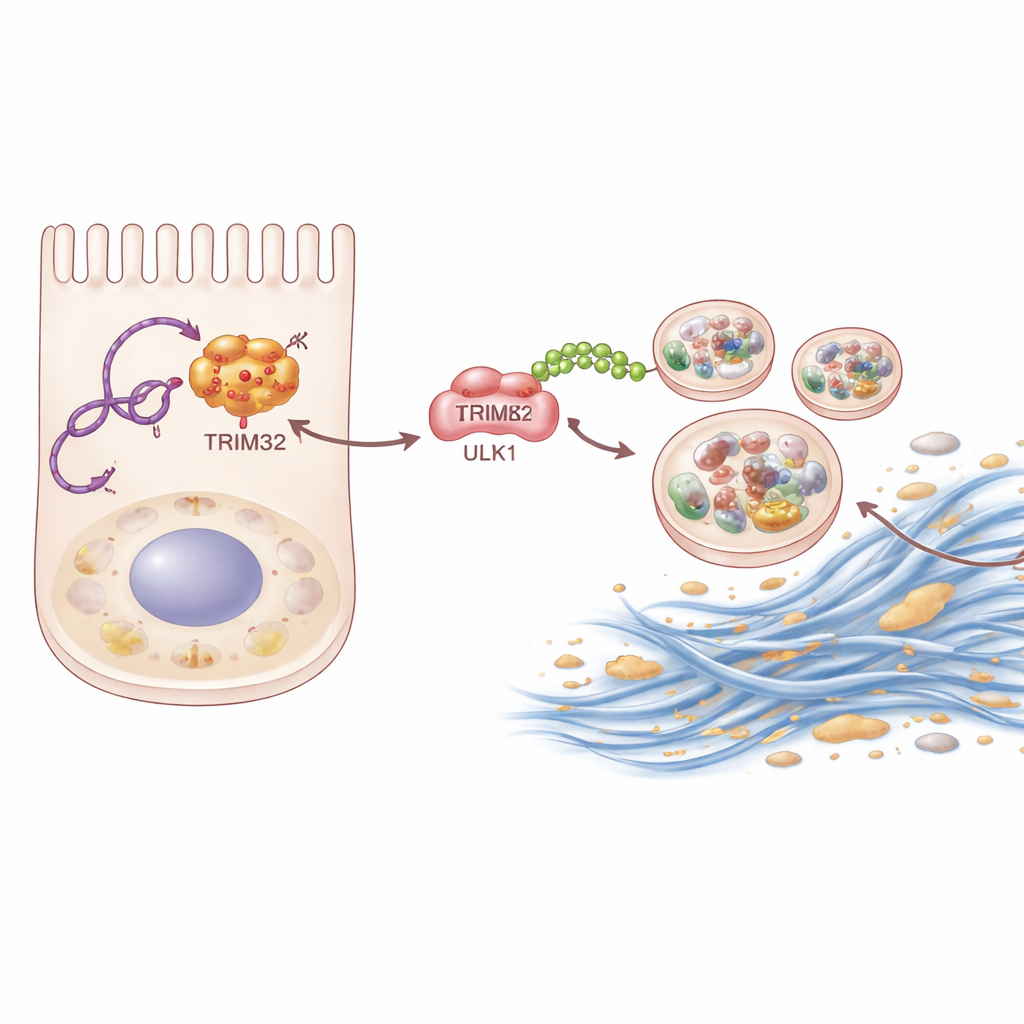
Nuevas vías hacia riñones menos rígidos
En conjunto, el trabajo revela una ruta molecular previamente desconocida que conecta ARN largo no codificante, el etiquetado proteico y el reciclaje celular con la acumulación de tejido cicatricial renal. En riñones lesionados, P4HA2-AS1 aumenta, estabiliza TRIM32, potencia ULK1 y lleva la autofagia más allá de su rango beneficioso, lo que finalmente favorece la acumulación de proteínas fibróticas y la pérdida de función. Para el público general, la conclusión es que la fibrosis renal no es una caja negra inevitable: está impulsada por interruptores identificables que podrían ser dianas terapéuticas. Apuntar al eje P4HA2-AS1–TRIM32–ULK1—reduciendo el ARN agresor, moderando TRIM32 o ajustando la actividad de ULK1—podría algún día ofrecer nuevos tratamientos para frenar o prevenir la progresión de la enfermedad renal crónica.
Cita: Pan, Z., Xiao, F., Hu, W. et al. LncRNA P4HA2-AS1 drives renal interstitial fibrosis via trim32-mediated k63 ubiquitination of ULK1 and autophagic dysregulation. Commun Biol 9, 339 (2026). https://doi.org/10.1038/s42003-026-09618-7
Palabras clave: enfermedad renal crónica, fibrosis renal, autofagia, ARN largo no codificante, túbulos renales