Clear Sky Science · es
Inhibidores de la transcriptasa inversa permiten la generación de espermátidas fértiles a partir de testículos fetales de ratón in vitro
Convertir células germinales tempranas en espermatozoides funcionales
Los tratamientos contra la infertilidad y la investigación básica dependen de entender cómo las células germinales inmaduras del testículo se transforman en espermatozoides. Este estudio demuestra que ahora es posible inducir a testículos fetales de ratón muy tempranos, tomados justo después de que se determina el sexo del embrión, a completar esta transformación íntegramente en una placa de cultivo. Ajustando con cuidado el entorno químico y el nivel de oxígeno, los investigadores no solo produjeron células maduras similares a espermatozoides, sino que además las usaron para generar descendencia sana y fértil.
Por qué es difícil reproducir el desarrollo testicular temprano
La producción de espermatozoides fuera del cuerpo ya se había logrado antes usando tejido testicular de ratones recién nacidos o mayores, pero la eficiencia era baja y los intentos con tejido fetal mucho más temprano fracasaron en gran medida. En esa etapa temprana, el testículo aún está ensamblando su arquitectura interna y las células germinales experimentan cambios profundos en cómo se empaqueta y marca su ADN. Reproducir esta compleja coreografía en cultivo resulta desafiante, y las culturas previas rara vez avanzaban más allá de los primeros pasos cuando se partía de testículos recogidos alrededor del día embrionario 12.5, poco después de fijarse el sexo del embrión.
Tomar prestados fármacos antivirales para proteger las células en desarrollo
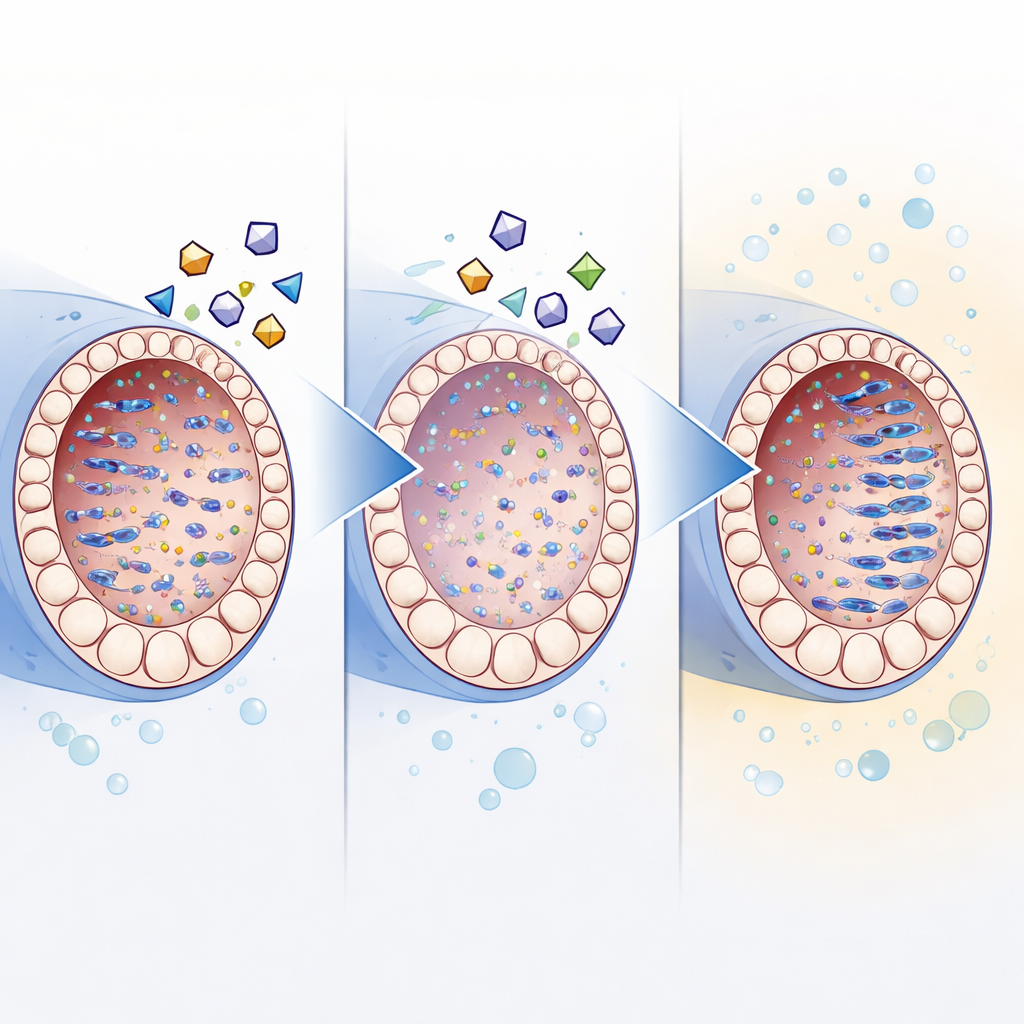
El equipo se centró en un obstáculo oculto: elementos de ADN móviles llamados retrotransposones, que pueden copiarse e insertarse en nuevas posiciones del genoma. En testículos normales in vivo, estos elementos están estrictamente controlados, especialmente en las células germinales. En cultivo, sin embargo, los autores observaron que la actividad de los retrotransposones era mucho mayor, mientras que los genes de defensa propios de la célula estaban más silenciosos. Este desequilibrio se correlacionó con un pobre desarrollo espermatogénico. Dado que los retrotransposones usan una enzima transcriptasa inversa, similar a la de algunos virus, los investigadores probaron varios fármacos diseñados originalmente como inhibidores de la transcriptasa inversa. Una mezcla específica de tres fármacos, denominada AEC, duplicó aproximadamente la fracción de células espermatogénicas y aumentó más de tres veces la proporción de células haploides similares a espermatozoides en testículos neonatales cultivados en comparación con los controles sin tratar.
De pequeños testículos fetales a espermatozoides funcionales
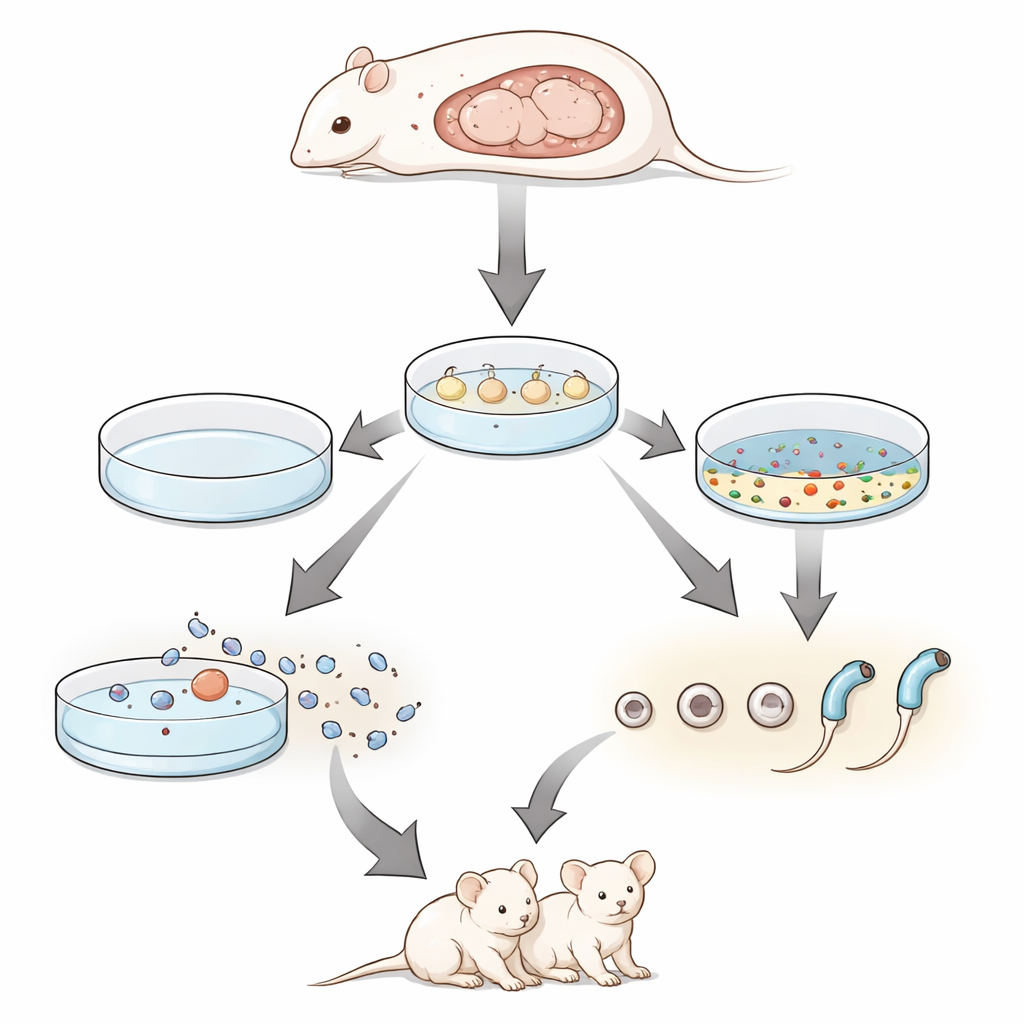
Con este cóctel farmacológico, los científicos se volcaron a los testículos fetales. En tejido tomado algo antes del nacimiento, los inhibidores aumentaron la aparición de espermátidas avanzadas. Más llamativo aún, cuando cultivaron testículos de embriones del día 12.5, una etapa que nunca antes se había mostrado capaz de completar la espermatogénesis in vitro, pudieron generar espermátidas redondas y alargadas. Las mayores mejoras se observaron al combinar la mezcla de inhibidores con una atmósfera de bajo oxígeno que imita mejor las condiciones del cuerpo en desarrollo. Bajo estas condiciones hipóxicas, alrededor de un tercio del área del tejido mostró marcadores de desarrollo germinal avanzado, y se pudieron recuperar espermatozoides con cola a partir de los cultivos.
Comprobar si las espermátidas generadas en el laboratorio funcionan de verdad
Para averiguar si estas células derivadas in vitro eran realmente funcionales, el equipo empleó una técnica llamada inyección de espermátida redonda. Aislaron espermátidas redondas de los testículos fetales cultivados e inyectaron esas células en óvulos de ratón que habían sido activados suavemente. Los embriones resultantes se transfirieron a madres nodrizas. A partir de solo dos fragmentos testiculares cultivados, el procedimiento produjo varias crías vivas, muchas de las cuales portaban un gen marcador fluorescente que confirmó su origen en cultivo. Cuando estos animales de primera generación se dejaron reproducir, dieron camadas de tamaño normal de crías sanas de segunda generación, demostrando que las espermátidas derivadas en el laboratorio podían sustentar no solo el desarrollo hasta el nacimiento, sino también la fertilidad completa.
Cómo el bloqueo del ADN móvil puede habilitar terapias futuras
Experimentos adicionales respaldaron la idea de que los inhibidores de la transcriptasa inversa ayudan principalmente manteniendo a raya el ADN móvil. En comparación con testículos de la misma edad in vivo, los testículos cultivados mostraron niveles más altos de proteínas de retrotransposones y copias extra de su ADN, junto con una expresión reducida de la maquinaria natural de silenciamiento de las células. Añadir el cóctel de inhibidores redujo esta acumulación, al tiempo que mejoraba la maduración de las células germinales. Aunque los fármacos ralentizaron ligeramente el crecimiento general del tejido, los intentos de compensar esto con aditivos basados en suero no mejoraron la producción de espermatozoides, lo que sugiere que el crecimiento y la diferenciación adecuada deben equilibrarse con cuidado.
Qué significa esto para la ciencia reproductiva
Este trabajo muestra que incluso los testículos fetales muy inmaduros ya contienen todos los ingredientes necesarios para construir una fábrica de espermatozoides funcional, siempre que el entorno proteja sus genomas e imite aspectos clave de la vida en el útero. Combinando fármacos de estilo antiviral con bajo oxígeno, los investigadores crearon un sistema de cultivo que recapitula la espermatogénesis completa a partir de una de las etapas más tempranas hasta ahora probadas y produce descendientes que crecen y se reproducen con normalidad. Aunque el estudio se realizó en ratones y está lejos del uso clínico, abre una ventana poderosa hacia los pasos más tempranos del desarrollo de las células germinales masculinas y ofrece pistas que algún día podrían ayudar a preservar o restaurar la fertilidad en pacientes cuyos gametos se dañaron tempranamente en la vida.
Cita: Nishida, M., Ono-Sunagare, Y., Kato, S. et al. Reverse transcriptase inhibitors enable the generation of fertile spermatids from fetal mouse testes in vitro. Commun Biol 9, 329 (2026). https://doi.org/10.1038/s42003-026-09613-y
Palabras clave: espermatogénesis in vitro, cultivo de testículo fetal, inhibidores de la transcriptasa inversa, retrotransposones, fertilidad masculina