Clear Sky Science · es
La obesidad altera la espermatogénesis mediante ferroptosis de células de Leydig inducida por miR-122-5p exosomal derivado del hígado
Por qué el peso y la fertilidad están relacionados
La obesidad suele tratarse en relación con las enfermedades cardíacas y la diabetes, pero también puede socavar silenciosamente la fertilidad masculina. Este estudio en ratones descubre una vía sorprendente por la que una dieta rica en grasas puede reducir la testosterona y dañar la producción de esperma: el hígado envía pequeñas “burbujas mensajeras” a la sangre que desencadenan un tipo especial de muerte celular en las células productoras de hormonas del testículo. Comprender esta comunicación oculta hígado–testículo puede ayudar a explicar por qué los hombres con sobrepeso con frecuencia presentan testosterona baja e infertilidad, y señalar posibles dianas terapéuticas.
Correo oculto entre órganos
Nuestros órganos se comunican constantemente mediante hormonas y otros mensajeros químicos. Una forma de esta comunicación usa exosomas: burbujas de tamaño nanométrico liberadas por las células que transportan lípidos, proteínas y material genético. Los investigadores empezaron con ratones alimentados con una dieta normal o con una dieta alta en grasas que provocó obesidad, resistencia a la insulina y mal control glucémico. Los ratones obesos tenían testículos más pequeños y menos activos: sus recuentos de esperma, niveles de testosterona y el tamaño y número de túbulos productores de espermatozoides estaban reducidos. Al examinar marcadores celulares clave en los testículos, hallaron menos células de Leydig productoras de testosterona y menos células espermáticas en estadios tempranos y tardíos, lo que confirma que toda la cadena de producción de esperma estaba afectada. 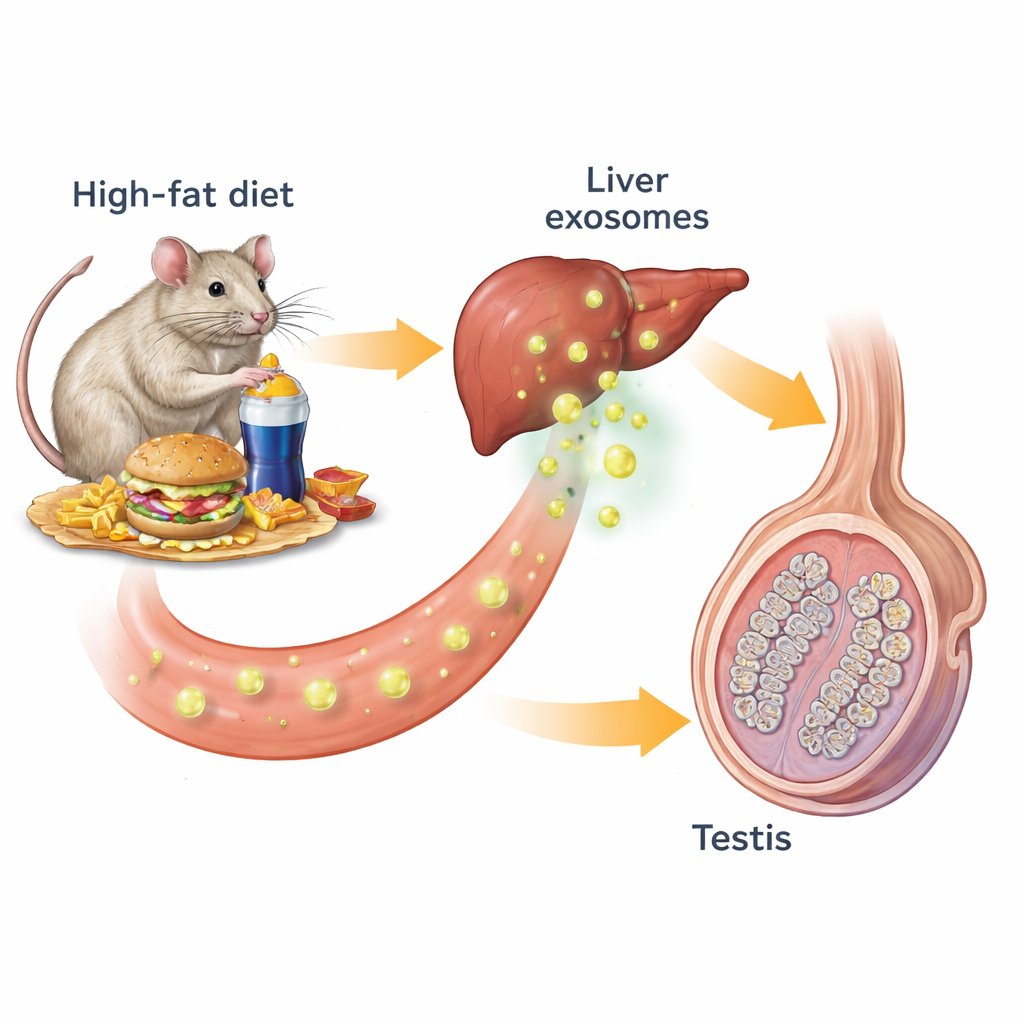
Los exosomas propagan el daño
Para comprobar si los exosomas circulantes contribuyen a este daño, los científicos purificaron exosomas de la sangre de ratones obesos y delgados. Inyectar exosomas procedentes de ratones obesos en ratones sanos y delgados fue suficiente para reproducir muchos de los problemas: los receptores desarrollaron signos de alteración metabólica, sus niveles de testosterona cayeron y empeoraron sus recuentos de esperma y la estructura testicular. Bloquear la liberación de exosomas en ratones obesos con un fármaco llamado GW4869 revirtió en gran medida estos cambios, restaurando los recuentos de esperma, la testosterona y la arquitectura testicular normal. Estos resultados muestran que los exosomas en el torrente sanguíneo no son meros espectadores; transportan activamente señales dañinas desde la obesidad hacia el sistema reproductor.
Una forma tóxica de muerte celular
El equipo investigó entonces qué estaban haciendo exactamente los exosomas a las células de Leydig. Se centraron en la ferroptosis, una forma de muerte celular impulsada por hierro, caracterizada por acumulación de hierro, daño oxidativo a los lípidos y lesiones mitocondriales —las centrales energéticas de la célula—. En ratones obesos y en ratones sanos a los que se les administraron exosomas procedentes de obesos, los testículos mostraron niveles elevados de hierro y malondialdehído, un subproducto del daño lipídico, así como lesión mitocondrial evidente al microscopio electrónico. Tratar a ratones obesos con un compuesto inhibidor de la ferroptosis, Ferrostatina-1, preservó las células de Leydig, aumentó la testosterona y los recuentos de esperma, y mejoró la salud mitocondrial. En cultivo celular, el mismo fármaco protegió a las células de Leydig aisladas frente a la muerte y al estrés oxidativo inducidos por exosomas de animales obesos. En conjunto, estos experimentos revelan la ferroptosis como un vínculo clave entre la obesidad y el fallo en la producción de testosterona.
El mensaje del hígado y el interruptor SCD2
Para localizar el mensaje dentro de los exosomas, los investigadores secuenciaron su carga de ARN pequeño y hallaron que un microARN particular, miR-122-5p, estaba fuertemente aumentado en los exosomas de ratones obesos. Este microARN era especialmente abundante en el hígado y en exosomas derivados del hígado, y se pudo rastrear cómo esos exosomas hepáticos viajaban hasta los testículos. Cuando los niveles de miR-122-5p se redujeron experimentalmente en los exosomas, las células de Leydig fueron menos propensas a la ferroptosis y mejoró la producción de testosterona, aunque los animales siguieron metabólicamente enfermos. Pruebas adicionales mostraron que miR-122-5p inhibe directamente un gen llamado Scd2, que ayuda a convertir ciertas grasas en formas que protegen a las células del daño oxidativo. Reducir Scd2 en las células de Leydig las hizo más vulnerables a la ferroptosis y disminuyó la testosterona, mientras que aumentar Scd2 en ratones obesos restauró parcialmente los niveles hormonales, la producción de esperma y la estructura mitocondrial. 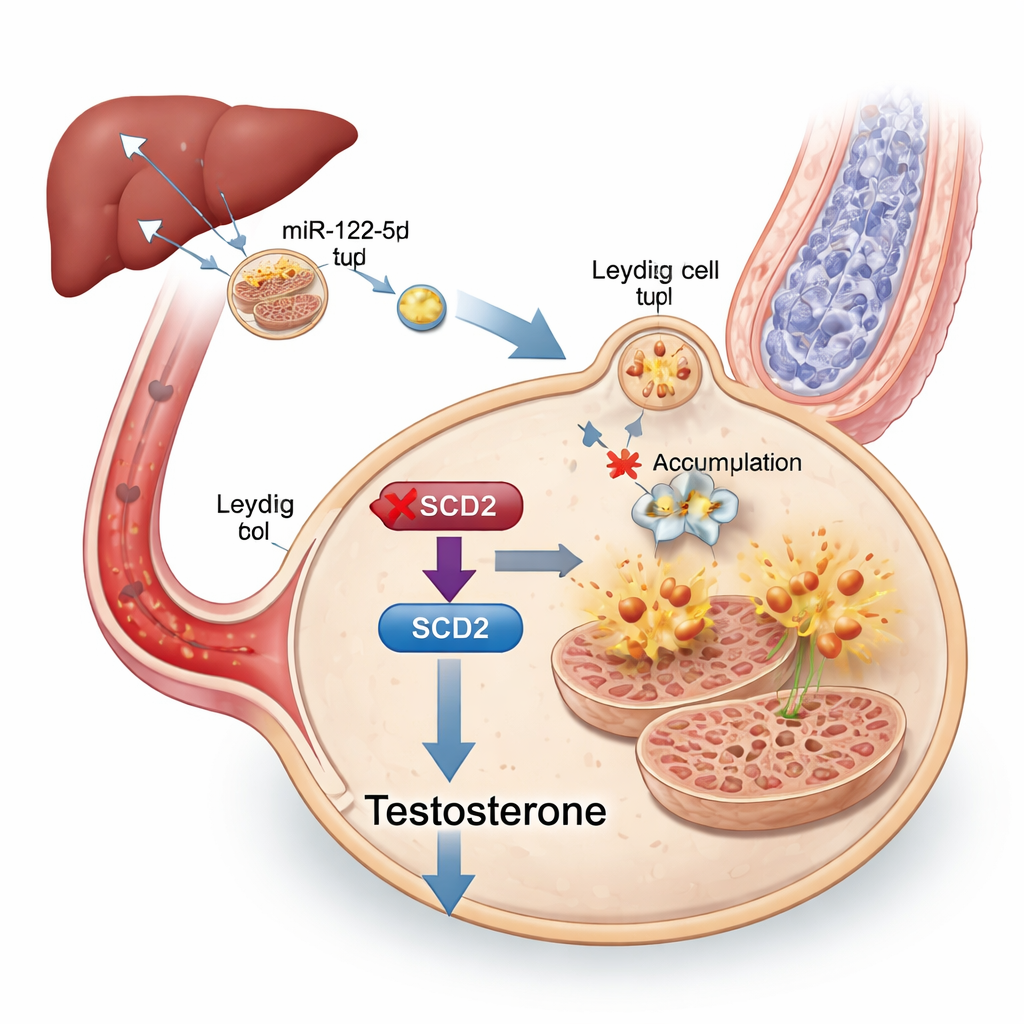
Qué significa esto para la salud humana
En términos sencillos, este trabajo muestra que una dieta alta en grasas puede hacer que el hígado cargue exosomas con una sobreabundancia de miR-122-5p. Estos exosomas viajan por la sangre hasta los testículos, donde el microARN apaga el “interruptor” Scd2 de manejo de grasas en las células de Leydig. Sin Scd2, estas células acumulan daño oxidativo impulsado por hierro, sufren ferroptosis, producen menos testosterona y, en última instancia, sostienen menos espermatozoides sanos. Aunque esta investigación se realizó en ratones y aún necesita confirmación en humanos, identifica a los exosomas derivados del hígado, miR-122-5p, la ferroptosis y Scd2 como posibles biomarcadores y dianas farmacológicas prometedoras para tratar la infertilidad masculina relacionada con la obesidad —y subraya otra razón más por la cual las dietas altas en grasas a largo plazo pueden erosionar silenciosamente la salud reproductiva.
Cita: Wang, N., Zhang, B., Chen, T. et al. Obesity impairs spermatogenesis via Leydig cell ferroptosis induced by liver-derived exosomal miR-122-5p. Commun Biol 9, 318 (2026). https://doi.org/10.1038/s42003-026-09612-z
Palabras clave: obesidad y fertilidad masculina, testosterona, exosomas, células de Leydig, ferroptosis