Clear Sky Science · es
Etiqueta proteica doble permite la expresión soluble y la purificación dependiente del calcio de fragmentos de anticuerpos de cadena única
Facilitar la fabricación de anticuerpos potentes
Los medicamentos modernos dependen cada vez más de fragmentos de anticuerpos: “misiles guiados” pequeños y precisos que pueden localizar células cancerosas, tejidos inflamados o moléculas causantes de enfermedad. Sin embargo, estos prometedores fármacos son sorprendentemente difíciles de fabricar: en fábricas bacterianas tienden a agregarse, plegarse erróneamente y resistir los métodos de purificación estándar. Este estudio describe un nuevo aditamento proteico, llamado etiqueta CSQ, que aborda ambos problemas a la vez, haciendo que estos fragmentos sean más fáciles de producir y purificar de forma sencilla y económica.
Por qué importan los anticuerpos reducidos
Los anticuerpos de tamaño completo han transformado el tratamiento del cáncer, las enfermedades autoinmunes y los trastornos oculares, pero su gran tamaño y estructura compleja tienen desventajas. Pueden eliminarse lentamente del organismo, no penetrar eficazmente en tumores o tejidos y son costosos de producir. Los fragmentos variables de cadena única, o scFv, conservan solo la parte funcional de un anticuerpo —la porción que reconoce el objetivo— enlazada en una sola cadena. Estas moléculas compactas penetran tejidos con mayor facilidad y pueden diseñarse para terapias y diagnósticos sofisticados. Sin embargo, cuando se producen en bacterias comunes como Escherichia coli, muchos scFv se acumulan en agregados insolubles llamados cuerpos de inclusión, y no existe una forma universal y sencilla de purificarlos.
Una etiqueta auxiliar dos en uno
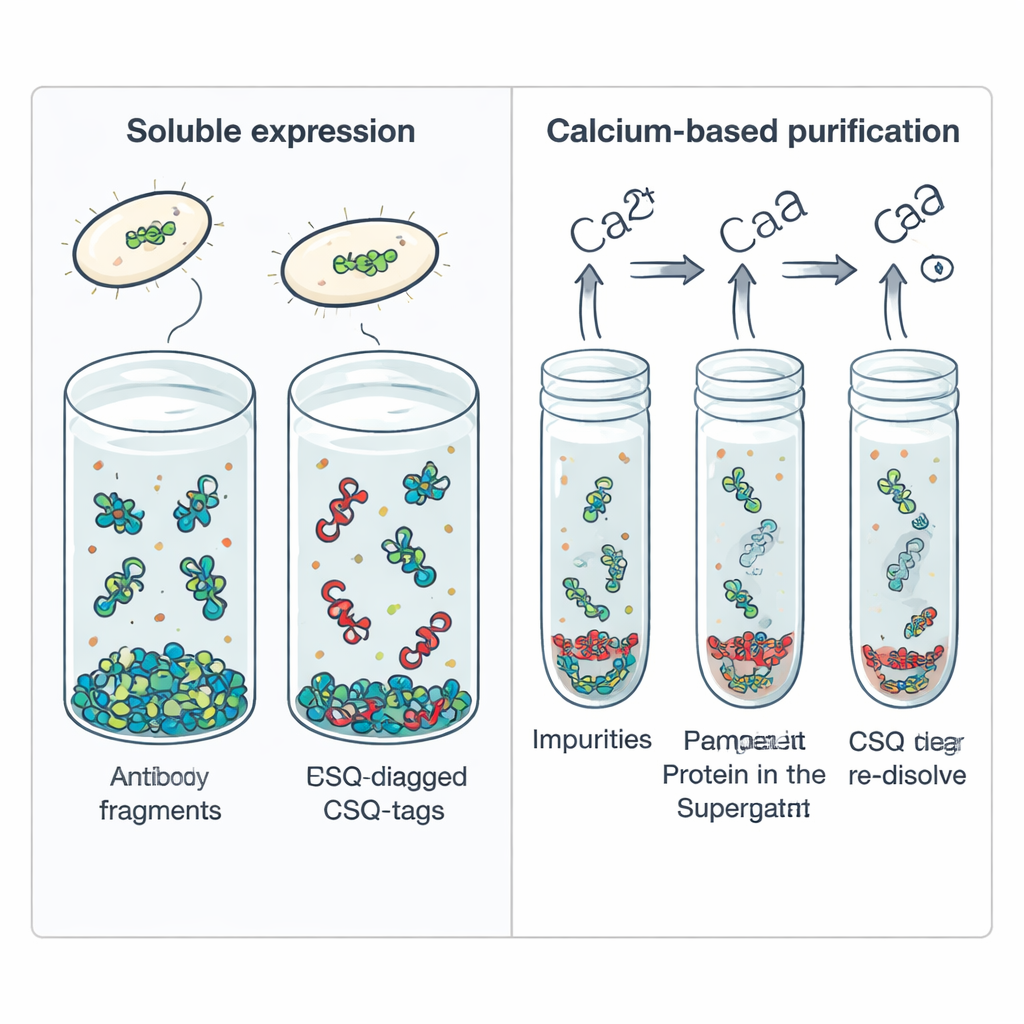
Los investigadores recurrieron a la calsequestrina, una proteína natural almacenadora de calcio en células musculares, para diseñar una etiqueta auxiliar que denominan etiqueta CSQ. Esta etiqueta es inusualmente ácida y muy flexible, con largas regiones desordenadas que actúan como “cerdas entrópicas” que barren el espacio alrededor de la proteína adjunta. Al fusionarla a cuatro scFv terapéuticos diferentes que normalmente se agregan, la etiqueta CSQ aumentó dramáticamente la cantidad que permanecía disuelta dentro de células E. coli estándar. Mientras que las mismas scFv con solo una simple etiqueta His eran casi totalmente insolubles, las versiones con CSQ alcanzaron una solubilidad media de alrededor del 84 por ciento, incluso en una cepa bacteriana que normalmente ofrece un entorno químicamente desafiante para el plegamiento correcto.
Superando tecnologías de etiquetas establecidas
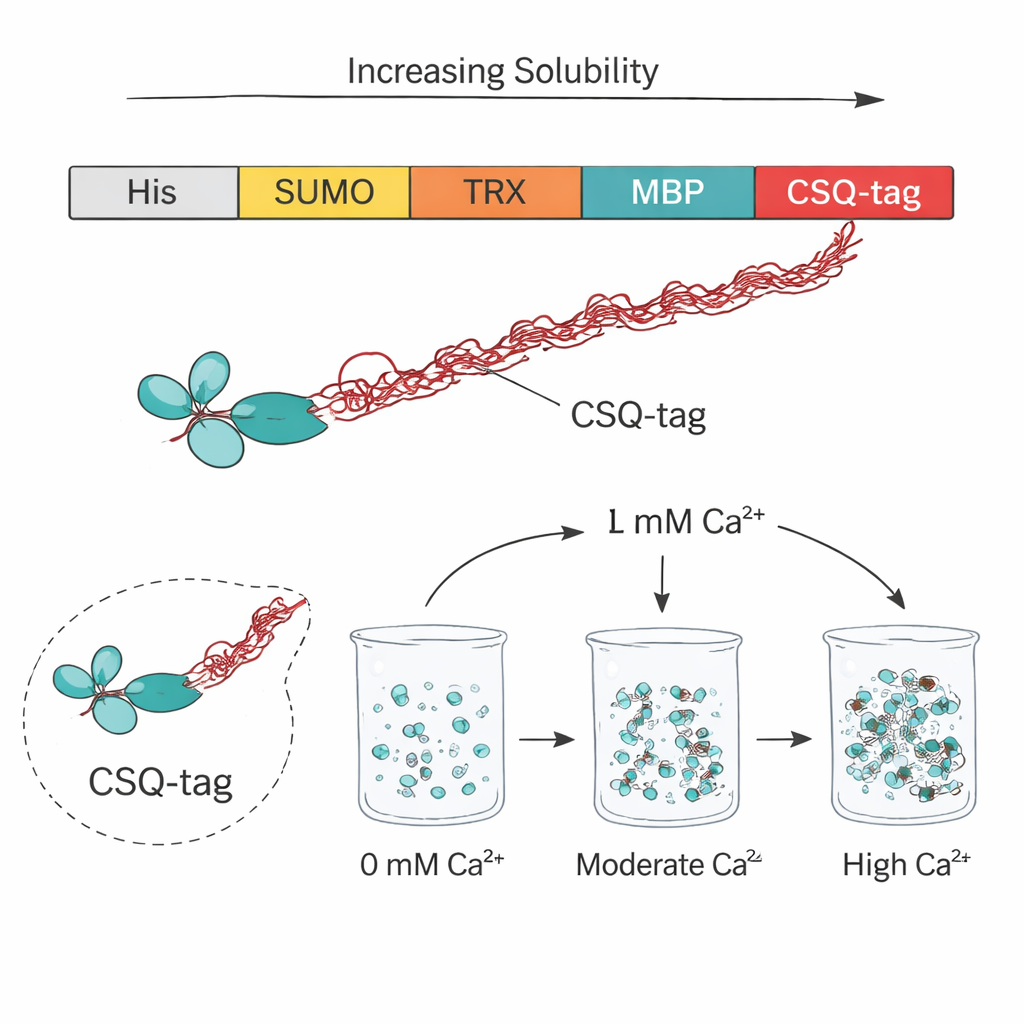
Para evaluar cómo se comparaba la etiqueta CSQ con etiquetas proteicas populares, el equipo la comparó con SUMO, tiorredoxina, GST y MBP, que se usan ampliamente para inducir la solubilidad de proteínas problemáticas. En esta prueba directa con un fragmento scFv anti-VEGF (la base del fármaco ocular brolucizumab), solo MBP y CSQ mejoraron notablemente la solubilidad, y CSQ resultó claramente superior. En cuatro scFv diferentes, CSQ aumentó la producción soluble aproximadamente 1,8 veces más que MBP, considerado durante mucho tiempo una de las mejores opciones. Experimentos adicionales mostraron que la porción más ácida y desordenada de la calsequestrina, conocida como dominio 3, era crucial para este efecto: eliminarla redujo bruscamente la solubilidad, subrayando cómo la carga negativa y la laxitud estructural de la etiqueta ayudan a evitar que las proteínas asociadas se peguen entre sí.
Usar el calcio como un interruptor simple de purificación
Más allá de ayudar a disolver los scFv, la etiqueta CSQ ofrece un truco de purificación incorporado. La calsequestrina se agrega naturalmente cuando se une al calcio y se desensambla cuando se elimina el calcio. Los autores aprovecharon este comportamiento añadiendo calcio a un extracto celular que contenía scFv con etiqueta CSQ, lo que provocó que las proteínas de fusión etiquetadas se agregaran mientras la mayoría de los contaminantes bacterianos permanecían en solución. Una rotación rápida en centrífuga sedimentó la proteína etiquetada con CSQ; la adición del quelante de calcio EDTA la redispersó de nuevo con alta pureza, por encima del 95 por ciento, sin resinas de cromatografía costosas. Esta transición de fase impulsada por calcio se pudo repetir sin dañar la proteína, lo que la hace atractiva para la producción a gran escala.
Mantener la potencia del medicamento
Para cualquier terapéutico, aumentar la producción solo importa si el producto final sigue funcionando. Tras usar una enzima estándar para cortar la etiqueta CSQ y un paso final de pulido, el equipo probó el scFv anti-VEGF libre. Se unió a su objetivo con una afinidad esencialmente idéntica a la del fármaco aprobado brolucizumab, y ensayos químicos detallados confirmaron enlaces internos correctos y la ausencia de agregados dañinos. Un segundo scFv especialmente problemático dirigido al receptor CD3 mostró una conservación de la actividad similar. Los rendimientos totales del proceso con CSQ fueron varias veces mayores que los informados para métodos tradicionales de replegado, usando equipos más sencillos y reactivos más baratos.
Qué podría significar esto para tratamientos futuros
Al combinar una mejor solubilidad y una palanca de purificación sencilla en una sola etiqueta, el sistema CSQ aborda dos cuellos de botella históricos en la producción de fragmentos de anticuerpos. Permite a los desarrolladores de fármacos usar cepas de E. coli de crecimiento rápido y económicas y, aun así, obtener scFv de alta calidad que conservan su capacidad de unión. Aunque todavía se necesita cierta optimización, especialmente para reducir pérdidas tras la eliminación de la etiqueta, esta etiqueta afinable por calcio podría simplificar la fabricación no solo de fragmentos de anticuerpos sino también de otras proteínas terapéuticas sensibles. Para los pacientes, eso podría traducirse eventualmente en una gama más amplia de fármacos biológicos dirigidos producidos de forma más eficiente y a menor coste.
Cita: Lee, J., Park, H., Jeong, S. et al. Two-in-one protein tag enables the soluble expression and calcium-dependent purification of single-chain antibody fragments. Commun Biol 9, 326 (2026). https://doi.org/10.1038/s42003-026-09611-0
Palabras clave: fragmentos de anticuerpos de cadena única, expresión de proteínas, etiqueta de calsequestrina, purificación dependiente del calcio, anticuerpos terapéuticos