Clear Sky Science · es
El reconocimiento y la unión de glicolípidos por Siglec-6 depende de interacciones con la membrana celular
Cómo nuestras células distinguen amigo de enemigo
El sistema inmunitario escudriña constantemente nuestras propias células, decidiendo cuándo permanecer en calma y cuándo atacar. Una parte clave de esta vigilancia implica reconocer estructuras azucaradas en las superficies celulares. Este estudio revela que un receptor inmunitario humano llamado Siglec-6 utiliza no solo esos azúcares, sino también la propia membrana celular circundante para tomar decisiones de unión con especial precisión. Esa estrategia inusual podría ayudar a explicar cómo el organismo afina las señales inmunitarias y abrir nuevas vías para terapias dirigidas.
Un guardián sensor de azúcares en las células inmunitarias
Las Siglecs son una familia de receptores situados en células inmunitarias que reconocen azúcares que contienen ácido siálico, ayudando al sistema inmune a distinguir lo “propio” de lo “ajeno”. La mayoría de las Siglecs dependen de un único y muy conservado elemento —un residuo de arginina— para sujetarse a estos azúcares. Si se elimina esa arginina, la unión generalmente falla. Sin embargo, Siglec-6 es un caso atípico: trabajos previos mostraron que puede seguir uniéndose a algunos lípidos portadores de azúcares incluso cuando esa arginina clave está mutada. El nuevo estudio se propuso descubrir cómo Siglec-6 puede eludir esta aparente regla y qué implica esto para su papel en mastocitos, células B de memoria y células placentarias humanas.
Los lípidos especiales que busca Siglec-6
En las superficies celulares, los azúcares relevantes pueden presentarse tanto en proteínas como en lípidos. Este trabajo se centra en un grupo de lípidos portadores de azúcar llamados gangliósidos, especialmente tres estrechamente relacionados: GM1, GM2 y GM3. Los tres exponen una única “cabeza” rematada por ácido siálico fuera de la membrana. Experimentos anteriores mostraron que Siglec-6 se une fuertemente a GM1 cuando forma parte de una membrana, pero casi no se une a GM2 o GM3, pese a que sus cabezas azucaradas son muy parecidas. Mediante simulaciones computacionales detalladas de membranas realistas, los autores confirmaron que el ácido siálico en GM1 y GM3 está igualmente expuesto y accesible. Dicho de otro modo, el acceso físico simple no es lo que confiere el estatus especial a GM1. En cambio, una azúcar adicional en la punta de GM1 —la galactosa terminal— emergió como un elemento crítico que ayuda a posicionar a Siglec-6 correctamente frente a la membrana.
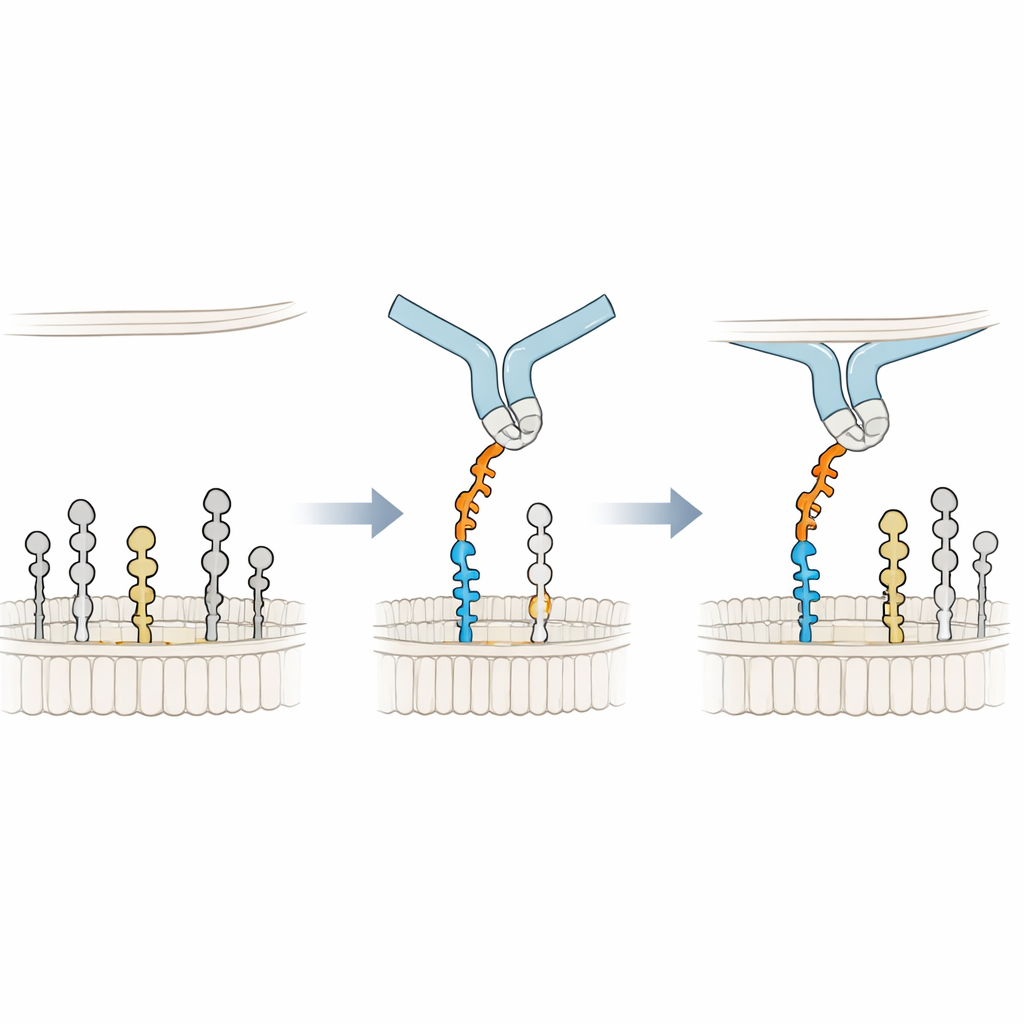
Apoyándose en la membrana para un agarre más firme
Para entender el mecanismo de unión a nivel atómico, los investigadores construyeron modelos 3D de Siglec-6 interactuando con GM1 en una membrana y realizaron largas simulaciones de dinámica molecular. Encontraron que Siglec-6 sigue usando su arginina canónica (Arg122) para contactar el ácido siálico, pero ese contacto parpadea con el tiempo. Lo que mantiene estable el complejo es algo nuevo: un triptófano cercano (Trp127) se hunde en la parte grasa de la membrana, mientras que una lisina adyacente (Lys126) interactúa con los grupos cabeza cargados de los lípidos circundantes. Esta “cuña” en la membrana complementa la interacción habitual azúcar–arginina, tomando efectivamente energía de unión del entorno lipídico. Cuando se elimina la galactosa terminal de GM1 para imitar GM2, un bucle flexible de Siglec-6 se desplaza hacia el espacio vacante, tira del receptor fuera de la membrana y perturba este agarre asistido por la membrana, lo que explica la pérdida de unión estable.
Experimentos que ponen a prueba el mecanismo
El equipo comprobó luego estas ideas computacionales en ensayos celulares y bioquímicos. Diseñaron células que expresaban Siglec-6 normal o mutado y midieron cuánto se unían estas células a liposomas fluorescentes y a pequeños discos lipídicos que contenían GM1. Mutar la arginina canónica solo redujo modestamente la unión cuando GM1 estaba en una membrana, confirmando que Siglec-6 no depende únicamente de este residuo en ese contexto. En contraste, mutar Trp127 abolió casi por completo la unión a liposomas que contenían GM1, y mutar tanto Trp127 como Lys126 prácticamente eliminó la unión por completo. Sin embargo, los mismos mutantes se unieron con normalidad a azúcares tipo GM1 presentados fuera de una membrana, lo que indica que la estructura básica de Siglec-6 permanecía intacta. Experimentos de espectrometría de masas nativa revelaron además que Siglec-6 puede unirse no solo a GM1 sino también a fosfolípidos ordinarios, y que esta interacción lipídica desaparece cuando se elimina Trp127. De forma notable, Siglec-6 incluso se adhiere a liposomas “desnudos” carentes de GM1, de nuevo de manera dependiente de Trp127, lo que sugiere que primero puede muestrear la membrana y luego fijarse al encontrar GM1.
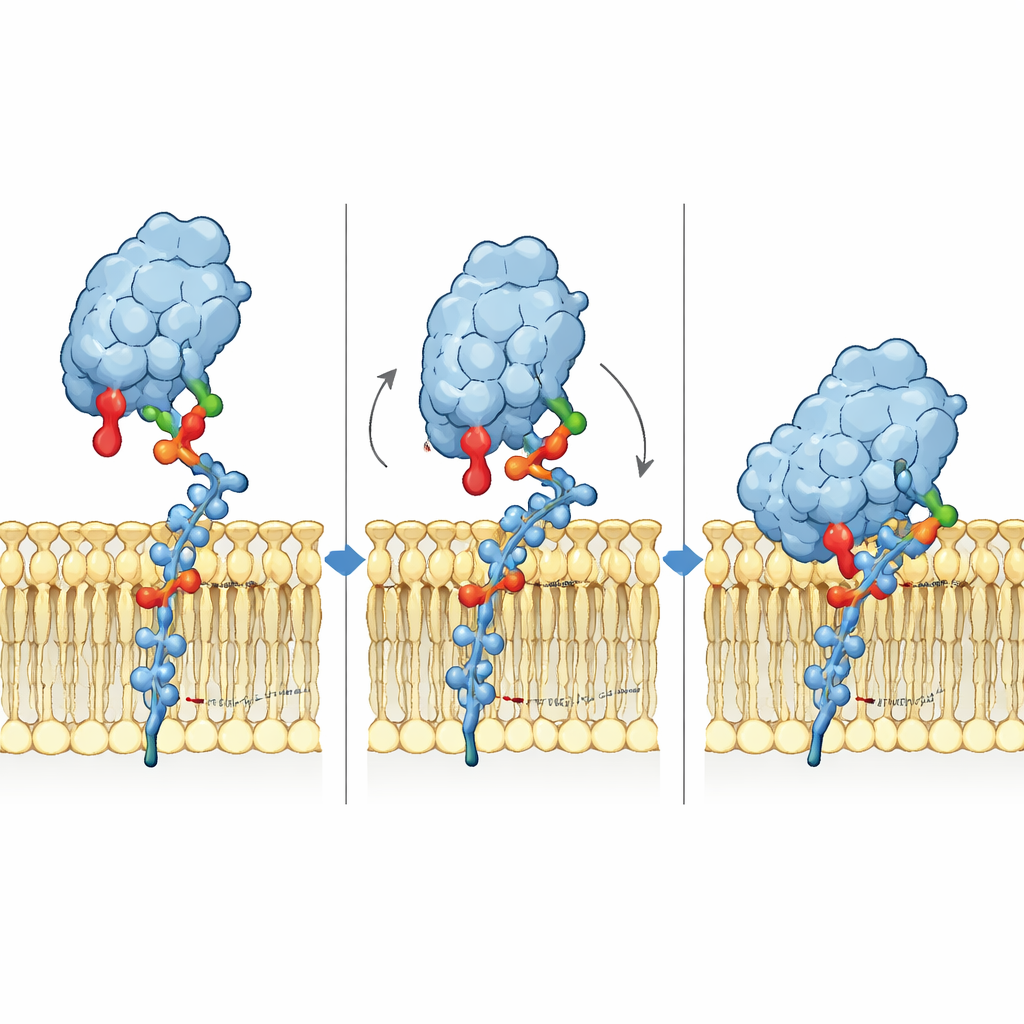
Los azúcares libres cuentan otra historia
Cuando los mismos tres gangliósidos se probaron como fragmentos azucarados libres en solución en lugar de formar parte de una membrana, Siglec-6 se comportó más como sus homólogos. En solución, se unió a GM1, GM2 y GM3 con afinidad débil y similar, y en ese contexto la arginina canónica era esencial: mutar Arg122 redujo drásticamente la unión, mientras que mutar Trp127 tuvo poco efecto. Este contraste muestra que Siglec-6 cambia efectivamente de mecanismo dependiendo de si encuentra azúcares en una membrana o en forma libre. En membranas, depende de una asociación cooperativa entre la cabeza azucarada, la galactosa terminal de GM1 y el contacto directo con la membrana; en solución, vuelve al motivo clásico de reconocimiento centrado en la arginina.
Por qué esto importa para el control inmunitario
En conjunto, el estudio revela a Siglec-6 como un sensor finamente ajustado que utiliza el contexto físico de la membrana para afinar su especificidad. Al anclarse parcialmente en los lípidos circundantes, puede reconocer selectivamente GM1 entre gangliósidos muy semejantes, convirtiendo en la práctica a un lector general de ácido siálico en un detector de alta precisión de un patrón superficial concreto. Esta estrategia asistida por la membrana parece única entre las Siglecs estudiadas hasta ahora y puede ayudar a que Siglec-6 explore las superficies celulares en busca de firmas glicolipídicas específicas que regulen respuestas inmunitarias o marquen tejidos particulares, como la placenta humana. Comprender este modo dual de reconocimiento podría facilitar el diseño de terapias y herramientas diagnósticas que exploten la inusual combinación de detección de azúcares y membrana de Siglec-6.
Cita: D’Andrea, S., Schmidt, E.N., Bui, D. et al. Glycolipid recognition and binding by Siglec-6 hinges on interactions with the cell membrane. Commun Biol 9, 333 (2026). https://doi.org/10.1038/s42003-026-09609-8
Palabras clave: Siglec-6, gangliósidos, membrana celular, reconocimiento de glicolípidos, regulación inmunitaria