Clear Sky Science · es
La desestabilización de la envoltura por la sobreexpresión de AcrAB2NodT vincula la resistencia a antibióticos con la sensibilidad a metales en Caulobacter vibrioides
Cuando luchar contra los antibióticos tiene un precio oculto
A medida que la resistencia a los antibióticos se propaga, solemos imaginar que las bacterias se vuelven simplemente más duras y difíciles de matar. Este estudio revela un giro sorprendente: en una bacteria de agua dulce común, una forma de resistencia a fármacos en realidad hace que las células sean más vulnerables a ciertos metales como el cobre y el zinc. Entender esta compensación oculta puede abrir nuevas vías para inclinar la balanza a nuestro favor combinando antibióticos con otros estreses que exploten las debilidades bacterianas.
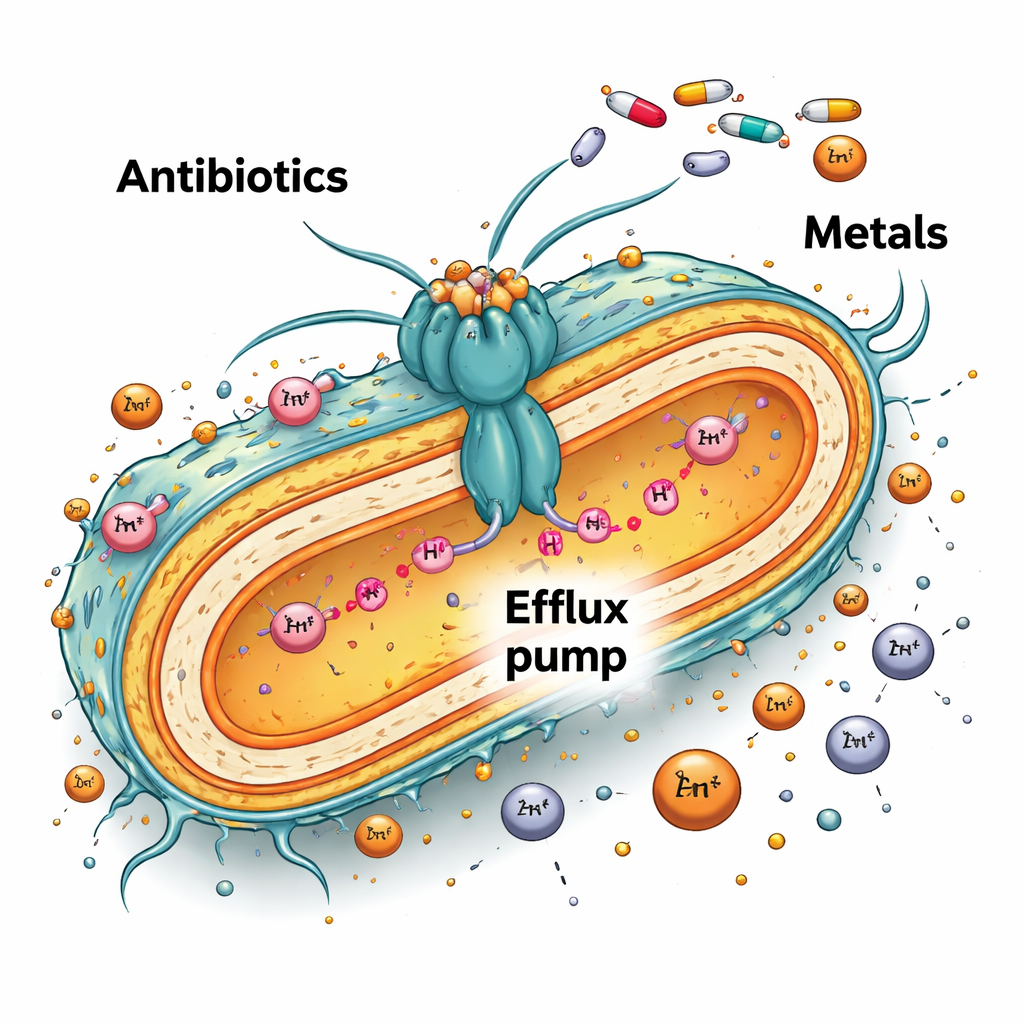
Una bomba bacteriana con doble papel
Muchas bacterias se defienden usando potentes bombas moleculares que se sitúan en sus capas externas y expulsan compuestos dañinos, incluidos los antibióticos. En Caulobacter vibrioides, un microbio de vida libre que prospera en lagos y ríos pobres en nutrientes, una de esas bombas se llama AcrAB2NodT. Atraviesa las membranas interna y externa de la célula y normalmente está controlada por una proteína reguladora llamada TipR. Cuando TipR está presente, la bomba solo se produce cuando es necesaria. Los investigadores examinaron qué ocurre cuando se elimina tipR, creando un mutante que mantiene esta bomba a pleno rendimiento todo el tiempo.
Ganar contra los fármacos, perder frente a los metales
El mutante carente de tipR fue en efecto mejor para soportar ciertos antibióticos beta-lactámicos, lo que confirma que la bomba sobreactivada ayuda a las células a expulsar los fármacos. Pero cuando el equipo expuso estas células al cobre y a otros metales, incluidos zinc, níquel y cadmio, la situación se invirtió: el mutante se volvió mucho más sensible que las células normales. Mediciones cuidadosas mostraron que esta sensibilidad no se debía a que las células almacenaran cobre extra ni a una mayor producción de especies reactivas de oxígeno. En cambio, el contenido total de metal dentro del mutante se mantuvo similar al de las células normales y los indicadores habituales de estrés oxidativo no aumentaron. Esto significaba que la vulnerabilidad debía provenir de cambios en la estructura celular o en la fisiología básica, más que de una simple sobrecarga metálica.
Una piel frágil y una barrera con fugas
Al observar más de cerca la superficie celular, los científicos utilizaron microscopía electrónica y análisis proteómicos y revelaron que la sobreexpresión de AcrAB2NodT trastorna la "piel" bacteriana, conocida como envoltura celular. Las células mutantes mostraron abultamientos, formas anormales y un espacio ondulado y desigual entre sus membranas interna y externa. Las proteínas implicadas en la construcción y remodelación de la envoltura eran más abundantes, lo que indica que las células mantenían un esfuerzo de reparación constante. Pruebas adicionales revelaron que la envoltura del mutante era más permeable, permitiendo que colorantes entraran con mayor facilidad una vez que la capacidad de la bomba para expulsarlos se desactivaba experimentalmente. Cuando los investigadores desactivaron por completo la bomba —ya sea eliminando sus genes o introduciendo mutaciones sutiles que la dejaban presente pero mayormente inactiva— tanto las formas celulares extrañas como la sensibilidad a metales desaparecieron en gran medida, aunque algunos componentes de la bomba seguían presentes.
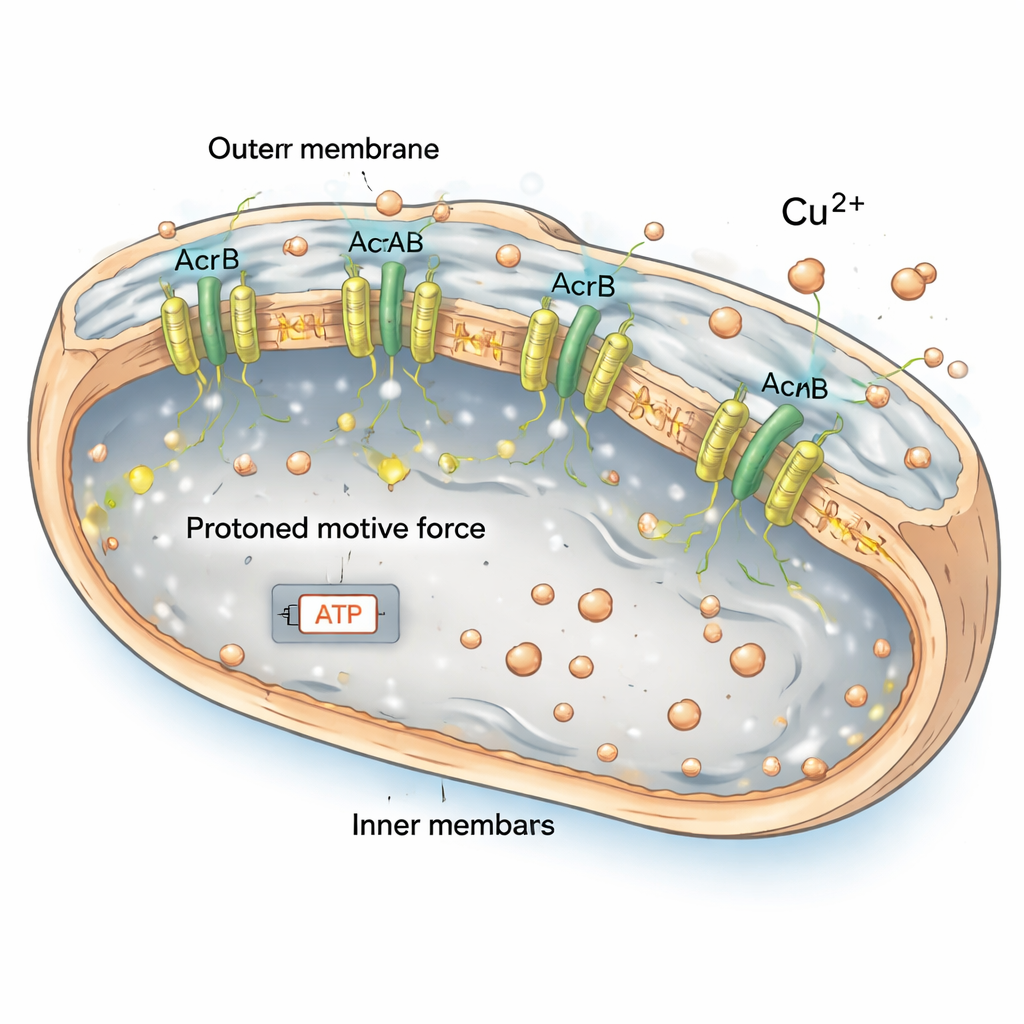
Baterías descargadas y tensión energética
Bombas de expulsión como AcrAB2NodT se alimentan de la fuerza motriz protónica, una especie de pequeña batería formada por partículas cargadas a través de la membrana interna. En el mutante que hace funcionar la bomba sin parar, esta batería estaba parcialmente agotada: un colorante que informa sobre el voltaje de la membrana mostró una señal más débil y las células presentaban niveles más bajos de ATP, su principal moneda energética. Las bacterias intentaron compensar aumentando las vías que producen energía, como las implicadas en la degradación de ácidos grasos, pero esto no fue suficiente para evitar una escasez energética global. Cuando los investigadores colapsaron químicamente el gradiente protónico en células normales, esas células empezaron a asemejarse al mutante en su pobre manejo del cobre. Esto sugiere firmemente que la combinación de una envoltura debilitada y una energía crónicamente baja hace que las bacterias con sobreproducción de la bomba sean objetivos especialmente vulnerables al estrés por metales.
Convertir una debilidad en una estrategia terapéutica
Para el público general, el mensaje clave es que la resistencia a antibióticos puede traer aparejado un coste: las bacterias pueden sobrevivir mejor a los fármacos pero volverse más frágiles en otros aspectos. En Caulobacter, mantener en funcionamiento continuo una bomba potente de expulsión somete a tensión las capas externas y el suministro energético de la célula, dejándola menos capaz de afrontar metales como el cobre. Esta compensación sugiere nuevas ideas terapéuticas. Si debilidades similares existen en bacterias patógenas, los médicos podrían potenciar la eficacia de los antibióticos combinándolos con metales u otros agentes que exploten la carga energética y estructural de los mecanismos de resistencia, llevando a los microbios resistentes más allá de su punto de ruptura.
Cita: Ote, M., Lardinois, L., Hendrickx, E. et al. Envelope destabilization by AcrAB2NodT overexpression links antibiotic resistance to metal sensitivity in Caulobacter vibrioides. Commun Biol 9, 313 (2026). https://doi.org/10.1038/s42003-026-09606-x
Palabras clave: resistencia a antibióticos, bombas de expulsión, sensibilidad al cobre, envoltura bacteriana, metabolismo energético