Clear Sky Science · es
Análisis integrado de GWAS y molQTLs revela variantes genéticas específicas de tipo celular en el sistema inmunitario porcino
Por qué la inmunidad porcina nos importa a todos
Los cerdos ayudan a alimentar a gran parte del mundo y también sirven como modelos importantes de los humanos en investigación médica. Sin embargo, las enfermedades infecciosas en cerdos cuestan a los ganaderos miles de millones de dólares cada año y fomentan un uso intensivo de antibióticos. Este estudio plantea una pregunta sencilla pero poderosa: ¿cómo influyen pequeñas diferencias en el ADN en el funcionamiento de las células inmunitarias porcinas, y podemos seguir esos efectos hasta el comportamiento de tipos celulares individuales en la sangre? Entender esa cadena de causa y efecto podría orientar la cría de piaras más sanas y ofrecer pistas sobre nuestros propios sistemas inmunitarios.
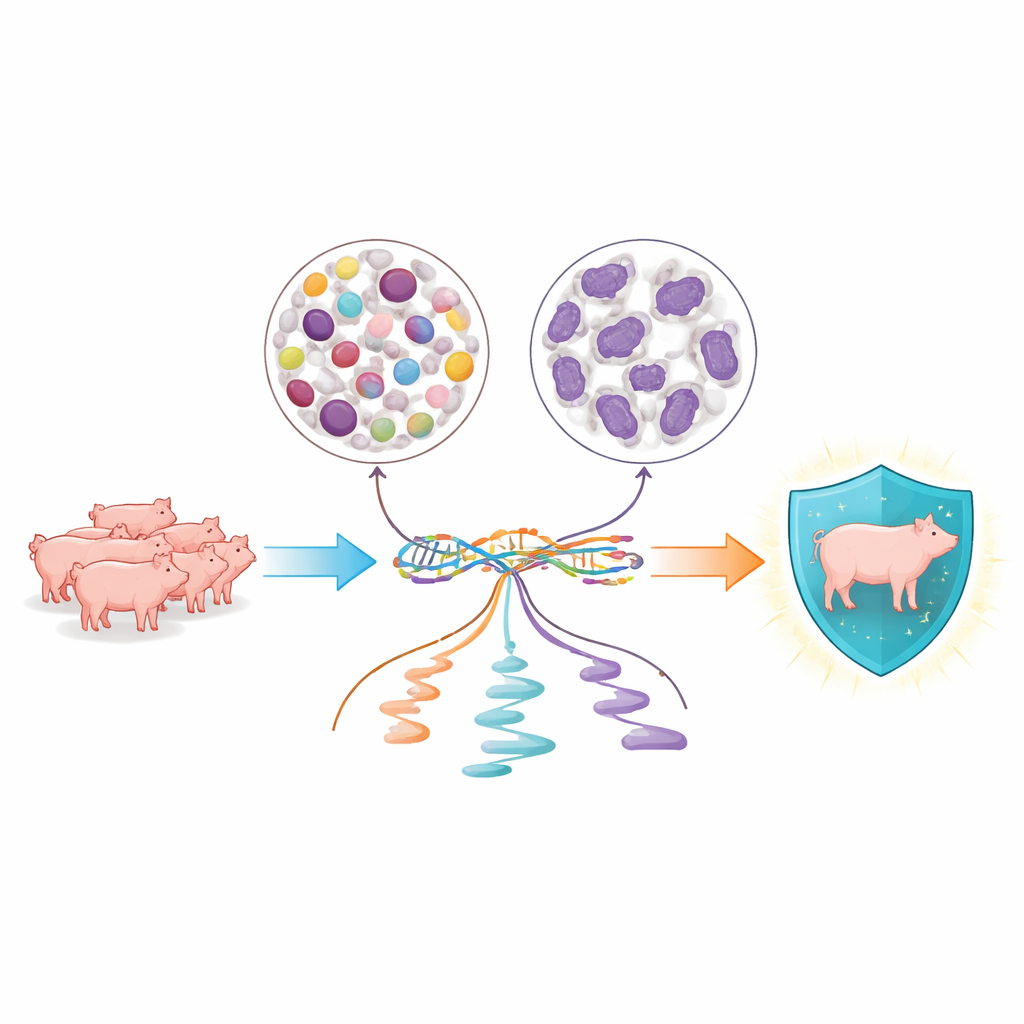
Observando de cerca dos familias clave de células sanguíneas
Los investigadores se centraron en dos grandes grupos de glóbulos blancos que patrullan constantemente la sangre porcina: las células mononucleares periféricas, que incluyen linfocitos y monocitos implicados en defensas más lentas y específicas, y los neutrófilos, que realizan ataques rápidos de primera línea contra microbios. A partir de 134 lechones Yorkshire jóvenes, purificaron cada tipo celular por separado y obtuvieron tanto datos genómicos completos como instantáneas detalladas del ARN, las moléculas que llevan las instrucciones genéticas dentro de las células. Esto les permitió ver no solo qué genes estaban activos, sino también cómo la célula cortaba y procesaba esos mensajes antes de utilizarlos.
Conectando variantes de ADN con interruptores moleculares
En lugar de observar solo qué variantes de ADN se asocian con el riesgo de enfermedad, el equipo mapeó cómo las variantes influyen en tres tipos de características moleculares dentro de cada tipo celular. Algunas variantes alteraban la cantidad de ARN que producía un gen. Otras cambiaban cómo se empalmaba el ARN, recortando o reorganizando fragmentos. Una tercera clase modificaba cómo se terminaba el ARN en su extremo final, un proceso llamado poliadenilación que puede afectar la estabilidad del mensaje. A estos pares variante–efecto se les denomina loci cuantitativos moleculares, o molQTLs. Los mapas revelaron miles de sitios de este tipo en cada tipo celular y, de forma llamativa, más de cuatro de cada cinco eran específicos de las células mononucleares mixtas o de los neutrófilos, lo que subraya cuán diferente puede leerse el mismo genoma en distintas células inmunitarias.
Encontrando redes que enlazan genes con rasgos inmunitarios reales
Para ver cómo estos interruptores moleculares se relacionan con la inmunidad del animal entero, los científicos combinaron los mapas de molQTL con análisis sanguíneos estándar y mediciones de proteínas señalizadoras inmunitarias. Construyeron redes de coexpresión—grupos de genes que tienden a subir y bajar juntos—y examinaron cuáles se correlacionaban con rasgos como la proporción de neutrófilos o linfocitos, el recuento de glóbulos blancos o los niveles de interferones y factor de necrosis tumoral. Los módulos ligados a rasgos de linfocitos estaban enriquecidos en vías de la inmunidad adaptativa, mientras que los asociados a rasgos de neutrófilos destacaban las defensas innatas rápidas y la señalización inflamatoria. Muchos genes clave en estos módulos estaban regulados directamente por molQTLs específicos de tipo celular, lo que sugiere rutas claras desde la variante del ADN hasta la alteración de la composición o función celular.
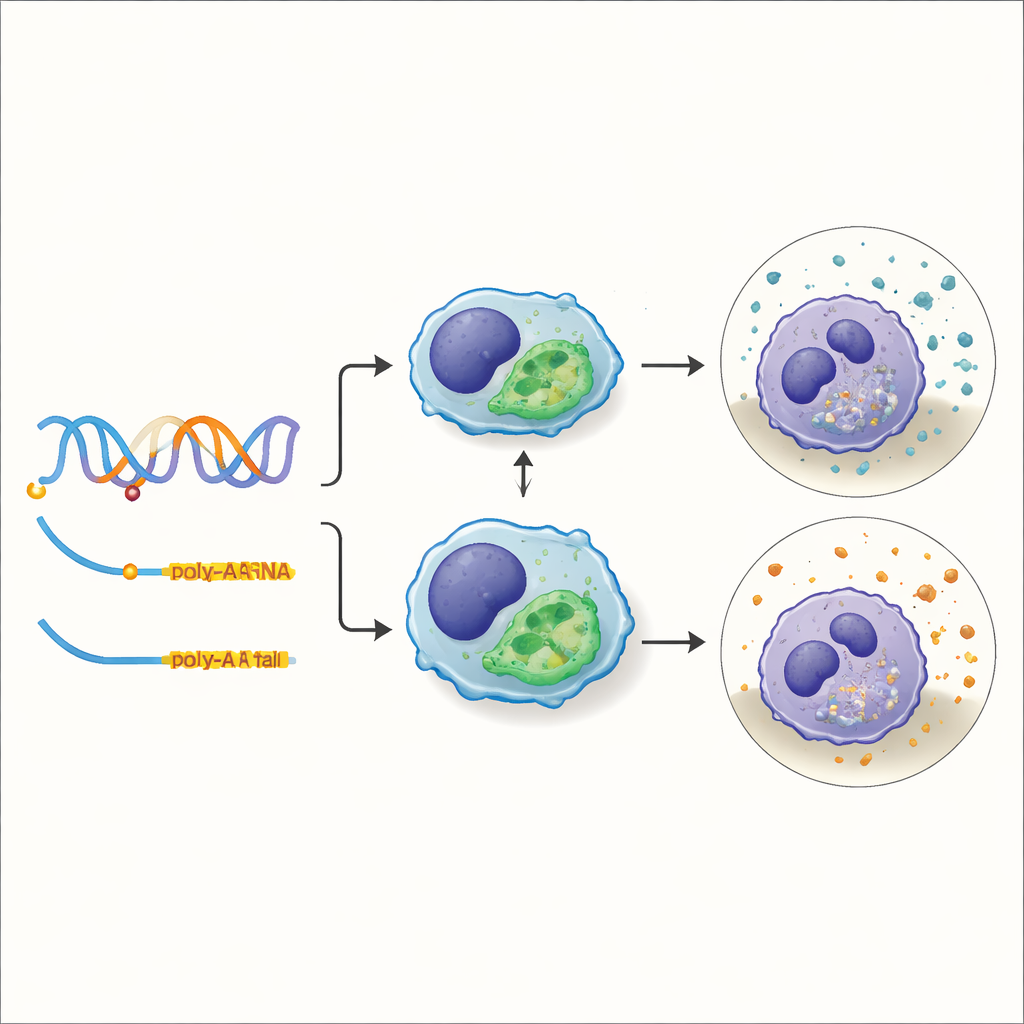
Detallando una variante que ajusta la capacidad de "limpieza" celular
Uno de los rasgos más prácticos que examinó el equipo fue la capacidad fagocítica—la habilidad de las células inmunitarias para engullir y eliminar desechos o patógenos. Al superponer sus molQTLs con los resultados de estudios de asociación a todo el genoma previos sobre fagocitosis, identificaron 588 regiones donde el mismo cambio en el ADN probablemente impulsa tanto un cambio molecular como una variación en el rendimiento de limpieza celular. Un ejemplo destacado fue una variante dentro de un gen llamado TXNDC15. Este cambio no simplemente activó o desactivó el gen; en su lugar, alteró qué sitio de poliadenilación elegía la célula para el ARN del gen. Los cerdos portadores de una versión de la variante privilegiaban una cola más corta en el ARN, que resultó ser más estable y se acumuló en niveles mayores, y estos animales mostraron una actividad fagocítica más fuerte en sus células inmunitarias.
Qué significa esto para cerdos más sanos y más allá
En términos sencillos, este trabajo muestra cómo pequeñas diferencias en el ADN pueden reconfigurar las "instrucciones" dentro de tipos celulares inmunitarios específicos y, a través de ello, influir en cuántas de esas células hay y qué tan bien realizan sus funciones. Al separar cuidadosamente los tipos celulares y rastrear no solo la actividad génica sino también cómo se cortan y se terminan los mensajes, el estudio descubre puntos de control ocultos que los estudios en tejidos mezclados no detectan. El mapa genético resultante proporciona una base para criar cerdos naturalmente más resistentes a las enfermedades, lo que podría reducir la necesidad de antibióticos. Al mismo tiempo, dado que la inmunidad porcina se parece mucho a la humana, estos hallazgos también pueden ayudar a los científicos a entender cómo operan mecanismos similares en la salud y la enfermedad humanas.
Cita: Yang, J., Chen, S., Tang, Y. et al. Integrated analysis of GWAS and molQTLs reveals cell-specific genetic variants in the porcine immune system. Commun Biol 9, 408 (2026). https://doi.org/10.1038/s42003-026-09605-y
Palabras clave: inmunidad porcina, variantes genéticas, células inmunitarias, fagocitosis, QTLs moleculares