Clear Sky Science · es
La inhibición de ATM mejora la eficiencia de knock-in suprimiendo la activación de vías apoptóticas inducidas por AAV
Hacer que la edición genética funcione mejor
La edición genética con CRISPR promete tratamientos para enfermedades genéticas, cultivos más resistentes y potentes herramientas de investigación. Pero uno de sus trucos más valiosos —insertar con precisión ADN nuevo en un lugar elegido del genoma, conocido como “knock-in”— sigue siendo ineficiente. Este estudio explora por qué algunas células aceptan ADN nuevo con más facilidad que otras y revela una forma de inducir a las células a realizar ediciones precisas con mayor frecuencia, especialmente al usar adenovirus adenoasociado (AAV), un vehículo líder para la terapia génica.
Observando la reparación del ADN en tiempo real
Para entender qué favorece o dificulta la inserción precisa de genes, los investigadores construyeron un intrincado “panel de control” dentro de células madre embrionarias de ratón. Este sistema triple de reporteros usa tres marcadores fluorescentes para seguir, en las mismas células, si CRISPR ha cortado el ADN, si se ha producido un knock-in preciso y si la célula, en cambio, ha integrado el ADN donante mediante un método de reparación más tosco. Leyendo las diferentes combinaciones de colores con citometría de flujo, pudieron separar las ediciones limpias basadas en plantilla de las inserciones propensas a errores y de las células no editadas. Este seguimiento paralelo les permitió cartografiar cómo distintas vías de reparación del ADN contribuyen a cada resultado con mucha más resolución que las pruebas antiguas basadas en PCR.
Dos ayudas del ADN, dos respuestas muy distintas
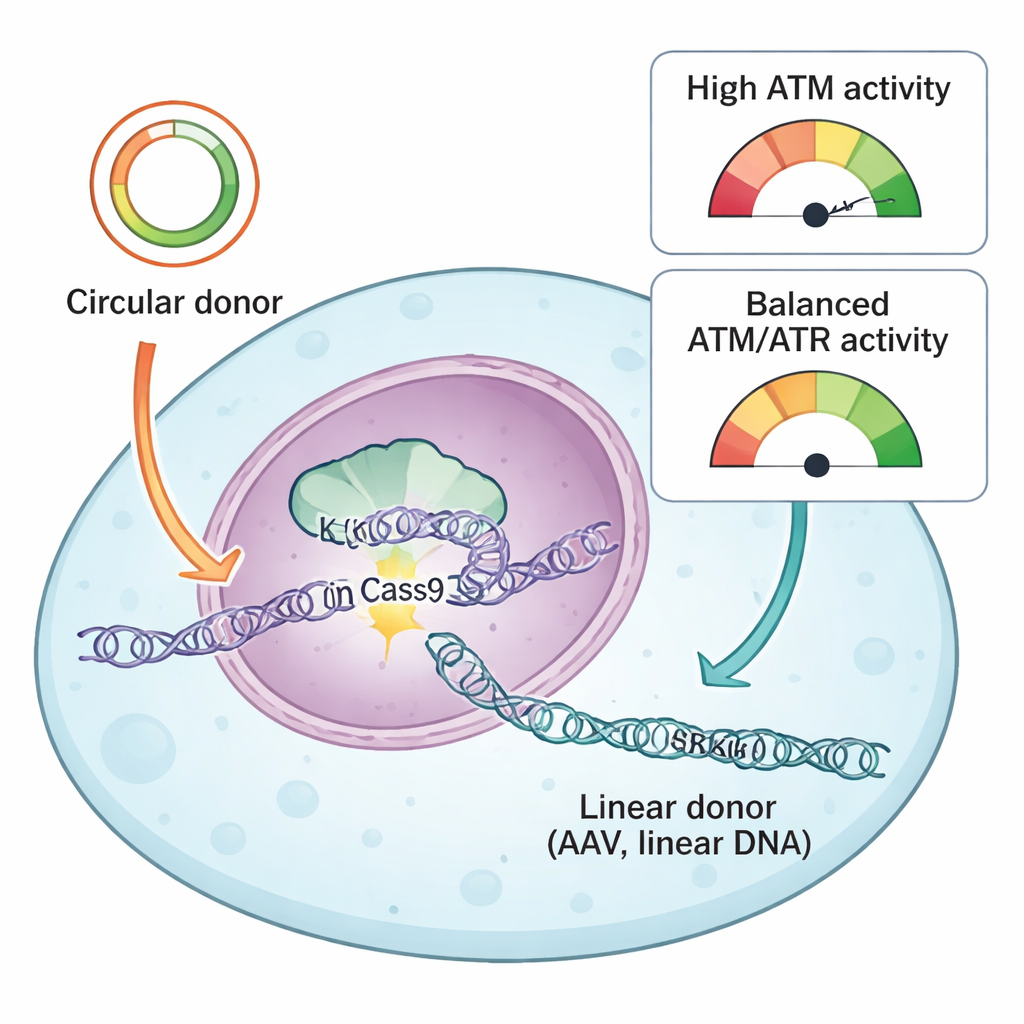
El equipo comparó dos tipos comunes de ADN donante usados para guiar las reparaciones CRISPR: plasmidios circulares y ADN lineal derivado de AAV. Ambos llevan “brazos de homología” coincidentes que le indican a la célula dónde insertar la nueva secuencia, pero entran en la célula en formas físicas diferentes. Los plasmidios circulares son bucles cerrados de ADN bicatenario, mientras que los donantes AAV suelen llegar como moléculas lineales simples. Usando su sistema de reporteros y una biblioteca de fármacos que apuntan a proteínas de la respuesta al daño del ADN, los autores encontraron que una proteína clave, ATR, era uniformemente esencial para knock-ins exitosos con ambos tipos de donante. La inhibición de ATR redujo drásticamente la inserción precisa, mientras que una estimulación moderada de la actividad de ATR a través de la vía KEAP1–NRF2 hizo que los knock-ins fueran más eficientes, especialmente con donantes AAV.
Cuando la protección del ADN resulta contraproducente
Un sensor distinto del daño del ADN, ATM, resultó comportarse de manera llamativamente dependiente del tipo de donante. Con donantes plasmidiales circulares, bloquear ATM redujo tanto el knock-in preciso como las inserciones mediadas por unión de extremos, acorde con su papel clásico en ayudar a las células a reparar roturas de doble cadena. Pero con ADN lineal —ya fuera de AAV, AAV autocontenible o plasmidios cortados en fragmentos rectos— la inhibición de ATM produjo lo contrario: aumentó la eficiencia del knock-in. Los investigadores trazaron este efecto a la forma en que las células interpretan las oleadas de ADN lineal. Dosis altas de AAV activaron fuertemente ATM, que a su vez activó p53 y caspasa 3, actores centrales de la muerte celular programada. Las células que habían tomado muchas copias del ADN donante, y por lo tanto tenían la mayor probabilidad de un knock-in exitoso, eran también las más propensas a ser eliminadas por este sistema de alarma.
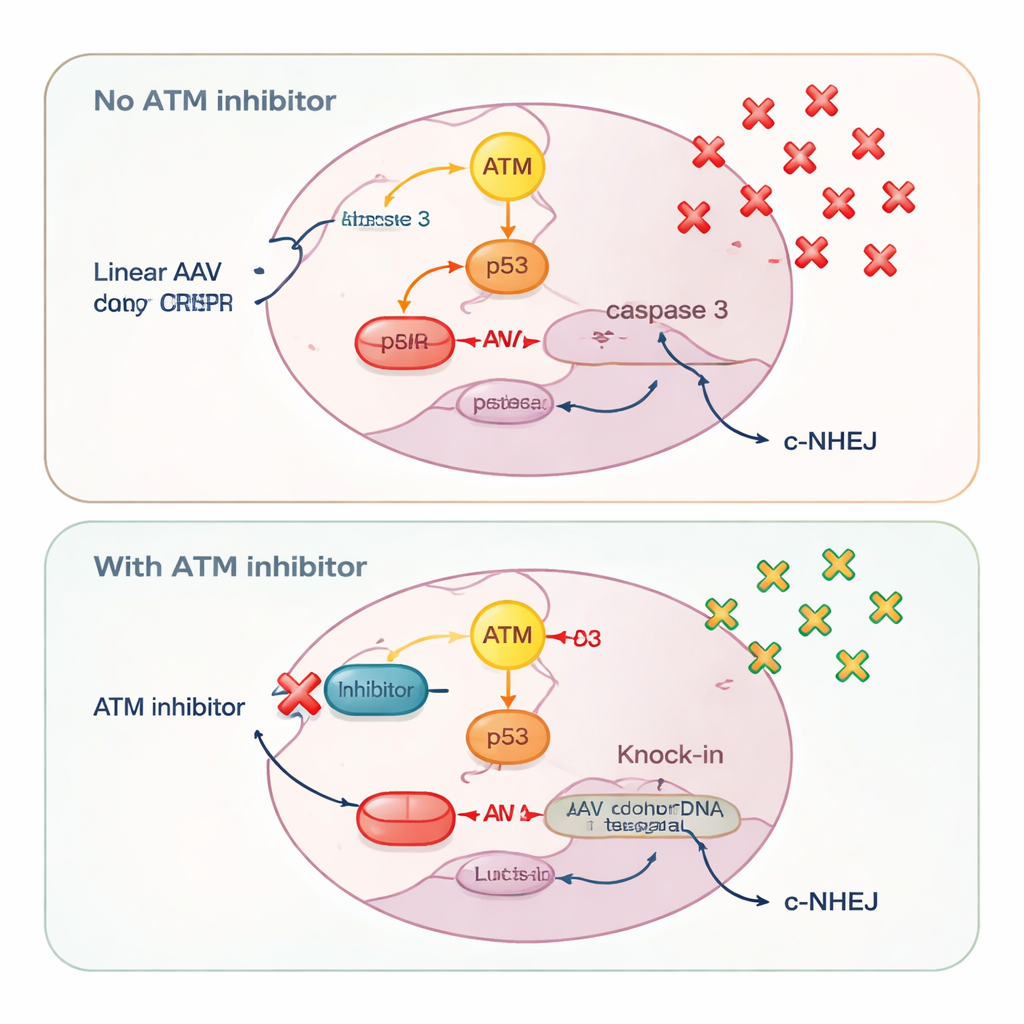
Salvar a las células mejor equipadas
Al añadir inhibidores de ATM, los científicos silenciaron la vía de muerte ATM–p53–caspasa 3. Esto preservó a las células que llevaban altas cantidades de ADN donante, permitiendo que más de ellas sobrevivieran el tiempo suficiente para completar un knock-in preciso. Mediciones de copias del genoma viral confirmaron que la inhibición de ATM aumentó el número de moléculas de AAV retenidas dentro de las células. Al mismo tiempo, el bloqueo de ATM atenuó ligeramente una vía de reparación rápida y contundente llamada unión por extremos no homóloga clásica, como lo mostró la reducción en la activación de DNA-PK, una enzima central en esa vía. Debilitar esta opción de reparación competidora orientó más cortes de CRISPR hacia el knock-in basado en homología en lugar de parches rápidos que ignoran la plantilla donante.
Qué significa esto para futuras terapias génicas
Para no especialistas, la conclusión es que las mismas salvaguardas celulares que nos protegen del daño del ADN pueden sabotear involuntariamente la edición genética precisa, especialmente cuando se usan grandes cantidades de ADN donante viral. Este trabajo muestra que modular con cuidado esas salvaguardas —mantener a ATR activo pero restringir temporalmente a ATM cuando hay donantes lineales como AAV— puede hacer que los knock-ins con CRISPR sean más fiables y eficientes. Dicha estrategia podría mejorar las terapias génicas, la ingeniería celular y los modelos de enfermedad al ayudar a más células a aceptar el cambio previsto mientras se evita la pérdida celular innecesaria.
Cita: Natsagdorj, ME., Hara, H., Uosaki, H. et al. ATM Inhibition Enhances Knock-in Efficiency by Suppressing AAV-Induced Activation of Apoptotic Pathways. Commun Biol 9, 177 (2026). https://doi.org/10.1038/s42003-026-09604-z
Palabras clave: knock-in con CRISPR, edición génica con AAV, respuesta al daño del ADN, inhibición de ATM, ingeniería del genoma