Clear Sky Science · es
STING controla la glucólisis y la lactilación de histonas para impulsar la reprogramación metabólica de macrófagos en el íleo postoperatorio
Cuando la cirugía pone el intestino en pausa
Tras una cirugía abdominal, muchos pacientes descubren que sus intestinos simplemente se niegan a reactivarse. Esta ralentización, denominada íleo postoperatorio, puede suponer días de náuseas, distensión y recuperación demorada. El estudio resumido aquí plantea una pregunta aparentemente simple: ¿por qué ciertas células inmunitarias del intestino mantienen el tránsito intestinal detenido, y podría la atenuación de un único interruptor molecular ayudar a que el intestino vuelva a funcionar?
Cómo una operación de rutina desencadena inflamación intestinal
La cirugía abdominal altera inevitablemente los intestinos. En ratones, la manipulación suave del intestino fue suficiente para provocar hinchazón, acumulación de líquido y obstrucción del contenido en el intestino delgado. Cuando los investigadores siguieron hasta qué punto avanzaba un tinte fluorescente inocuo a través del tracto digestivo, observaron que la cirugía ralentizaba bruscamente su progresión, señal de la motilidad deteriorada. El examen microscópico de la pared intestinal mostró que la capa muscular —el tejido que realmente se contrae para empujar el alimento— se inflamó y quedó abarrotada de células inmunitarias entrantes, en especial macrófagos y neutrófilos. Estos hallazgos sugieren que la propia capa muscular del intestino se convierte en un campo de batalla inflamado tras la cirugía, y que esta inflamación local está estrechamente ligada a la parálisis intestinal.
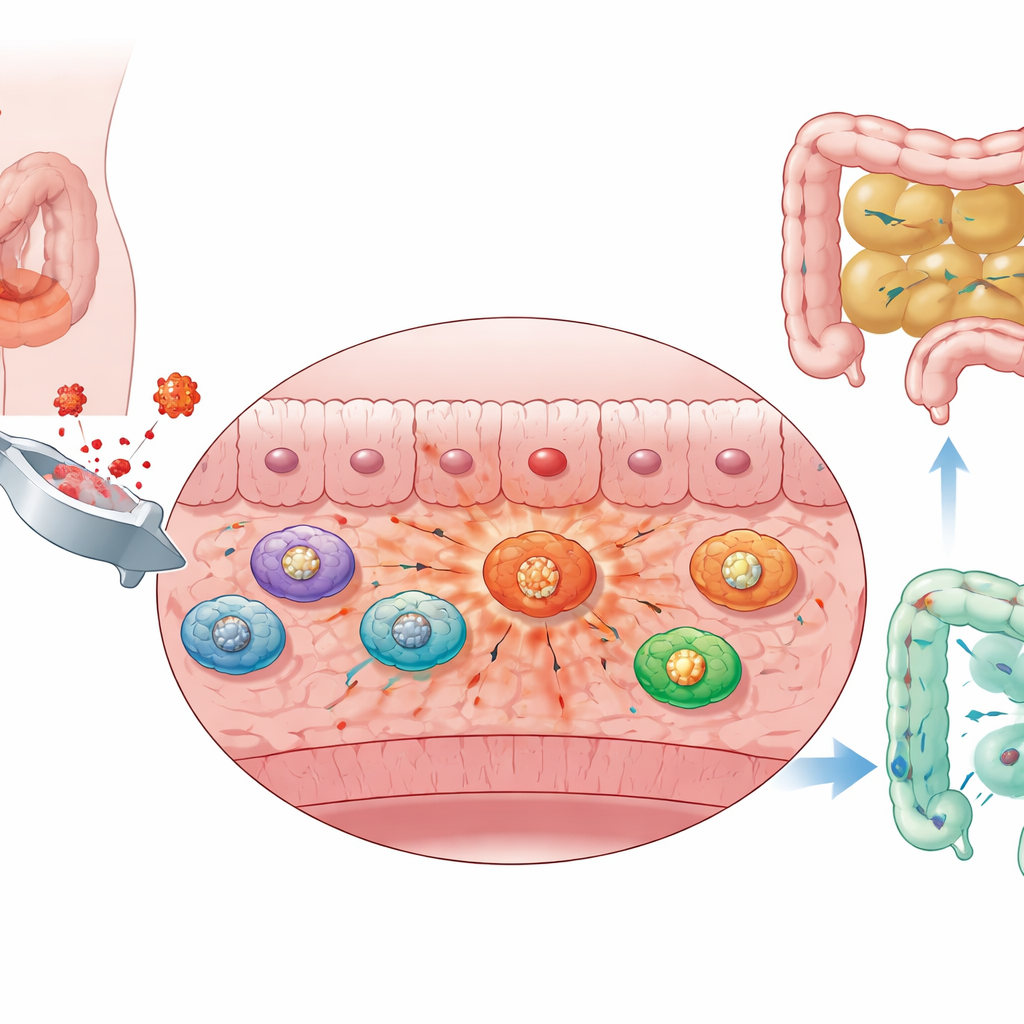
Los macrófagos cambian su combustible y avivan la inflamación
Para entender qué estaban haciendo estos macrófagos infiltrantes, el equipo analizó datos masivos de ARN y secuenciación unicelular del estrato muscular intestinal. Encontraron que los macrófagos en animales operados aumentaron con fuerza una vía rápida de quema de azúcar conocida como glucólisis. En comparación con otras células inmunitarias del mismo tejido, los macrófagos infiltrantes mostraron las puntuaciones de glucólisis más altas y expresaron niveles elevados de enzimas glucolíticas clave. Un subconjunto distinto de estas células dependía en gran medida de la glucólisis, presentaba fuertes firmas inflamatorias y respondía vigorosamente a componentes bacterianos como el lipopolisacárido. En esencia, los macrófagos habían activado un modo de alta utilización de azúcar y alta inflamación que parece agravar la inflamación de la capa muscular y mantener al intestino inmóvil.
Un interruptor molecular que conecta la detección de peligro con la quema de azúcar
Los investigadores se centraron entonces en STING, una proteína conocida como sistema de alarma para ADN extranjero pero cada vez más reconocida como reguladora metabólica. En la musculatura intestinal inflamada, el subconjunto de macrófagos altamente glucolíticos mostró niveles de STING notablemente más altos, un patrón confirmado por tinción tisular. En cultivo celular, exponer macrófagos al lipopolisacárido bacteriano aumentó tanto la actividad de STING como las enzimas glucolíticas que convierten la glucosa en energía y lactato. Cuando los científicos eliminaron el gen STING, este estallido de quema de azúcar colapsó: los intermedios glucolíticos disminuyeron, la acidificación del medio de cultivo se redujo y se produjeron menos especies reactivas de oxígeno. Estas células sin STING también generaron menos lactato, lo que implica que la vía de alarma y el motor metabólico están estrechamente acoplados.
Del residuo azucarado a la memoria epigenética
El lactato suele considerarse un producto de desecho metabólico, pero aquí desempeña un papel más sutil. El equipo demostró que, en macrófagos normales, la avalancha de lactato se utiliza para modificar químicamente las histonas —las proteínas que empaquetan el ADN— mediante un proceso llamado lactilación. Esta modificación fue especialmente prominente en un sitio llamado H4K8 en histonas próximas al gen de HK2, una enzima glucolítica de control. En células carentes de STING, la lactilación de histonas y la accesibilidad de la cromatina en el promotor de HK2 se redujeron, y métodos especializados de secuenciación confirmaron que estos cambios frenaban la activación de HK2. Al mismo tiempo, se observó que un factor de transcripción aguas abajo, IRF3, se unía directamente al promotor de HK2 con más facilidad cuando estaba presente esta marca de lactilación de histonas. Juntos, estos pasos crean un bucle autorreforzante: STING estabiliza factores que incrementan la glucólisis, la glucólisis produce lactato, el lactato marca histonas para abrir el gen HK2, e IRF3 aumenta la expresión de HK2, alimentando aún más la glucólisis y la inflamación.
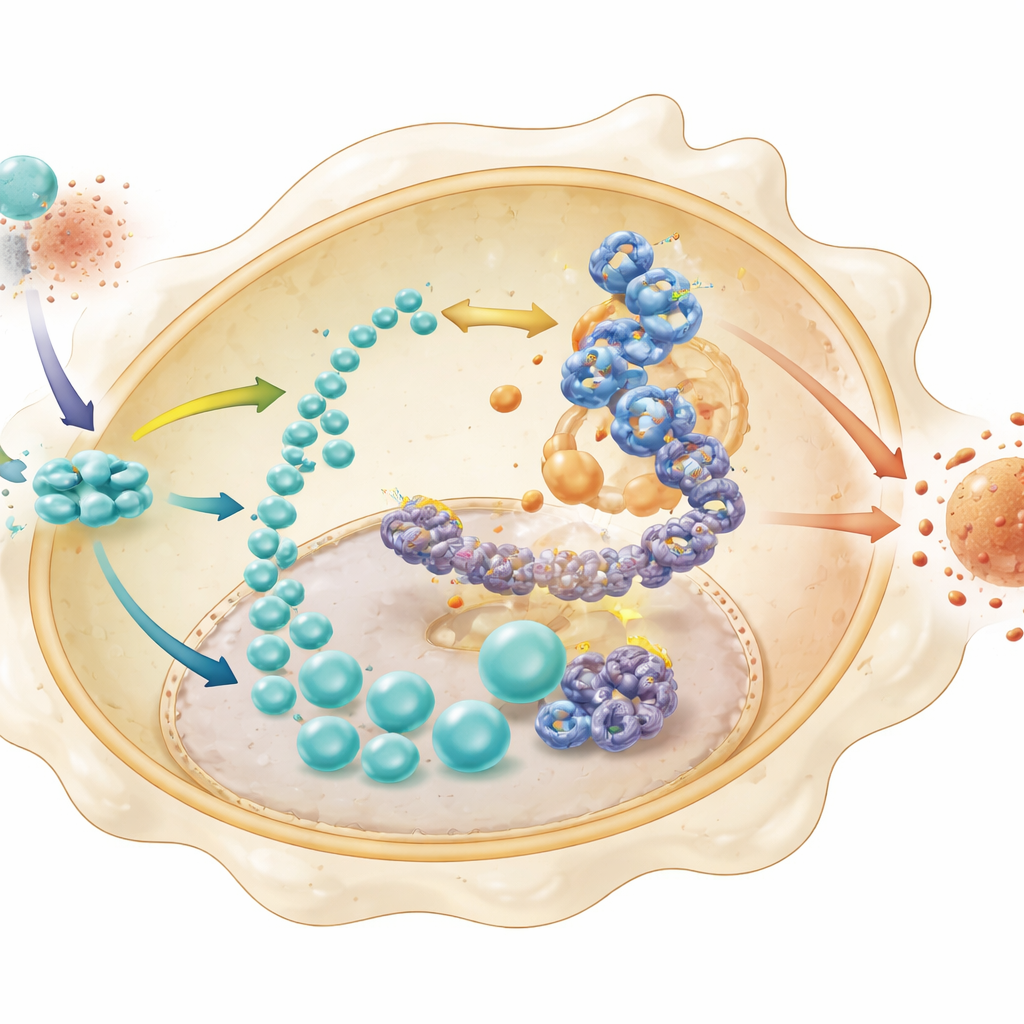
Romper el bucle para permitir la recuperación intestinal
Finalmente, el equipo se preguntó si romper este bucle podría ayudar realmente a los animales a recuperarse del íleo postoperatorio. En ratones sin STING, el tejido muscular intestinal expresó menos enzimas glucolíticas, contenía menos macrófagos inflamatorios y mostró un cambio desde un estado macrófago agresivo y proinflamatorio hacia un perfil más resolutivo. La infiltración de neutrófilos fue menor y el tránsito intestinal mejoró. El bloqueo farmacológico de STING en ratones normales produjo beneficios similares, mientras que reactivar la enzima HK2 en animales deficientes en STING restauró parcialmente la inflamación y los problemas de motilidad. Para un lector no especializado, el mensaje es claro: un único interruptor sensor de peligro en los macrófagos intestinales puede reconfigurar su metabolismo de un modo que deja al intestino en una pausa prolongada tras la cirugía. Apuntar a STING —o al bucle de retroalimentación que controla entre la quema de azúcar y la marca de lactato en histonas— ofrece una vía prometedora para acelerar la recuperación y aliviar una de las complicaciones más persistentes de las intervenciones abdominales.
Cita: Chen, K., Li, G., Cheng, Y. et al. STING controls glycolysis and histone lactylation to drive macrophage metabolic reprogramming in postoperative ileus. Commun Biol 9, 358 (2026). https://doi.org/10.1038/s42003-026-09602-1
Palabras clave: íleo postoperatorio, metabolismo de macrófagos, vía STING, glucólisis, inflamación intestinal