Clear Sky Science · es
Caracterización de la desarrollabilidad de nanocuerpos para mejorar el diseño terapéutico mediante el Therapeutic Nanobody Profiler
Por qué importan los parientes diminutos de los anticuerpos para los medicamentos del futuro
Muchos de los fármacos de gran éxito actuales son anticuerpos: proteínas que se adhieren a dianas de enfermedad con gran precisión. Una clase más reciente de ligandos todavía más pequeños, llamados nanocuerpos, puede colarse en huecos de difícil acceso en virus, tumores y otras moléculas. Pero la capacidad de unirse a una diana no es suficiente: un candidato a fármaco también debe ser fácil de producir, estable en un vial y seguro en el organismo. Este artículo presenta el Therapeutic Nanobody Profiler, una herramienta computacional diseñada para ayudar a los científicos a evaluar, de forma temprana y solo a partir de la secuencia, qué nanocuerpos tienen más probabilidades de convertirse en medicamentos prácticos.
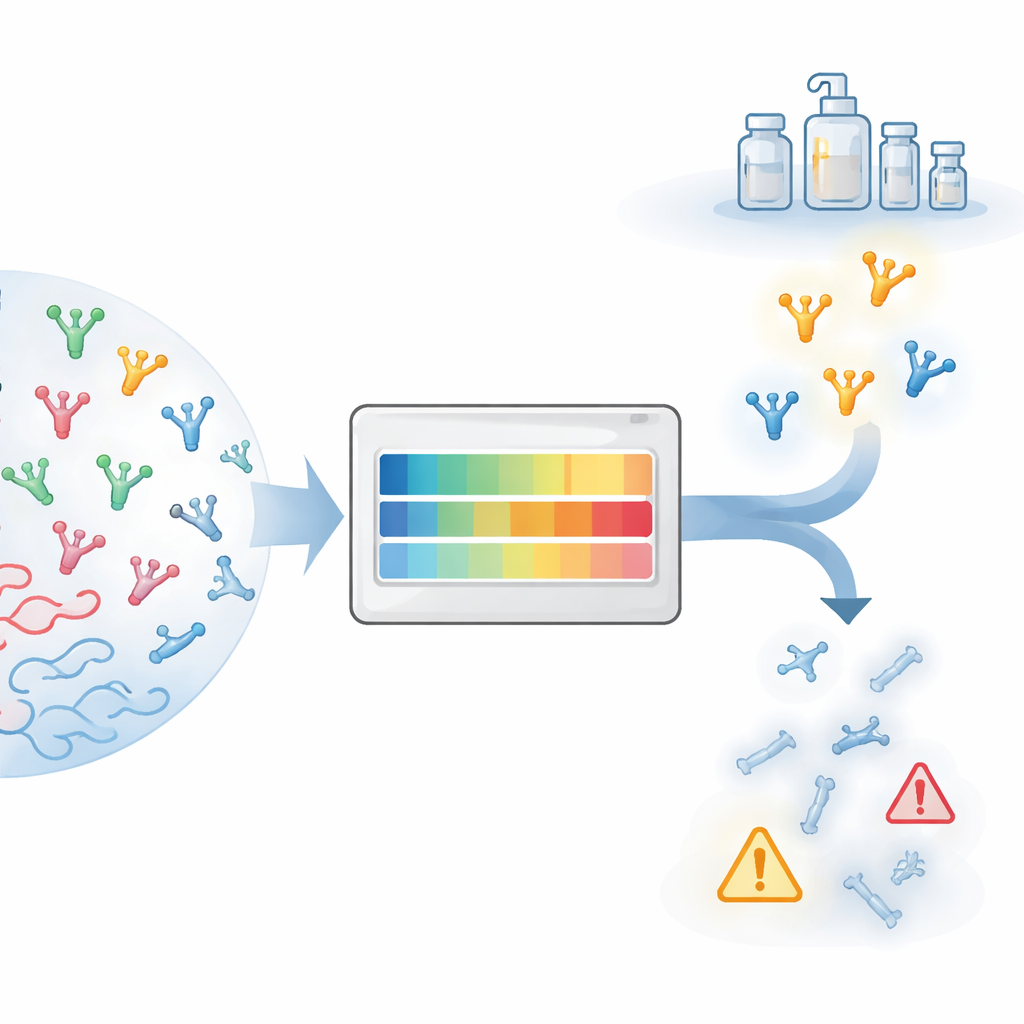
De una idea prometedora a un fármaco práctico
Convertir una proteína en una terapia real implica una serie de obstáculos prácticos agrupados bajo el término «desarrollabilidad». Las proteínas deben producirse en grandes cantidades, mantenerse solubles, evitar agregarse y conservar su estabilidad durante el transporte y el almacenamiento. En la última década, los investigadores han aprendido a predecir muchas de estas características para anticuerpos monoclonales de tamaño completo, apoyados por abundantes datos clínicos y pruebas de laboratorio especializadas. Sin embargo, los nanocuerpos son estructuralmente diferentes: constan de un solo dominio en lugar de un par de cadenas, con frecuencia tienen bucles de unión más largos y exponen regiones de superficie que están enterradas en los anticuerpos convencionales. Como resultado, los métodos ajustados a anticuerpos regulares pueden dar respuestas engañosas cuando se aplican a nanocuerpos.
Un profiler diseñado para las particularidades de los nanocuerpos
Para abordar esta discrepancia, los autores diseñaron el Therapeutic Nanobody Profiler (TNP), inspirado en una herramienta anterior para anticuerpos estándar pero reingenierizado en torno a la biología de los nanocuerpos. Compilaron secuencias de nanocuerpos de muchas fuentes: ensayos clínicos, repertorios inmunes naturales, patentes, artículos científicos y estructuras cristalográficas conocidas. Usando predictores de estructura basados en aprendizaje profundo adaptados a anticuerpos de dominio único, generaron modelos 3D para esas secuencias. A partir de cada modelo midieron la longitud de los bucles de unión, hasta qué punto un bucle clave se extiende desde el cuerpo de la proteína y cómo se disponen en la superficie los grupos de residuos hidrofóbicos y cargados: rasgos que influyen de forma importante en la solubilidad, la agregación y la adhesión inespecífica.
Dos sabores estructurales, ambos viables
Uno de los hallazgos más llamativos concierne al bucle de unión principal, conocido como CDR3. Cuando el equipo cuantificó cuán «compacto» es este bucle —comparando su longitud con la distancia a la que se proyecta desde la proteína— encontró una división clara en dos estilos estructurales. En un subtipo, el bucle es más largo y se pliega sobre el lateral de la proteína, formando numerosos contactos estabilizadores con un conjunto de residuos característicos. En el otro, el bucle sobresale más, como en un fragmento de anticuerpo convencional. Los nanocuerpos en fase clínica ocupan ambos subtipos y, cuando los investigadores compararon docenas de medidas experimentales prácticas —como agregación, autoasociación y estabilidad térmica— no observaron una penalización sistemática para ninguno de los estilos. Esto significa que los diseñadores de fármacos no necesitan favorecer una forma de bucle sobre la otra, siempre que el resto de las propiedades sea aceptable.
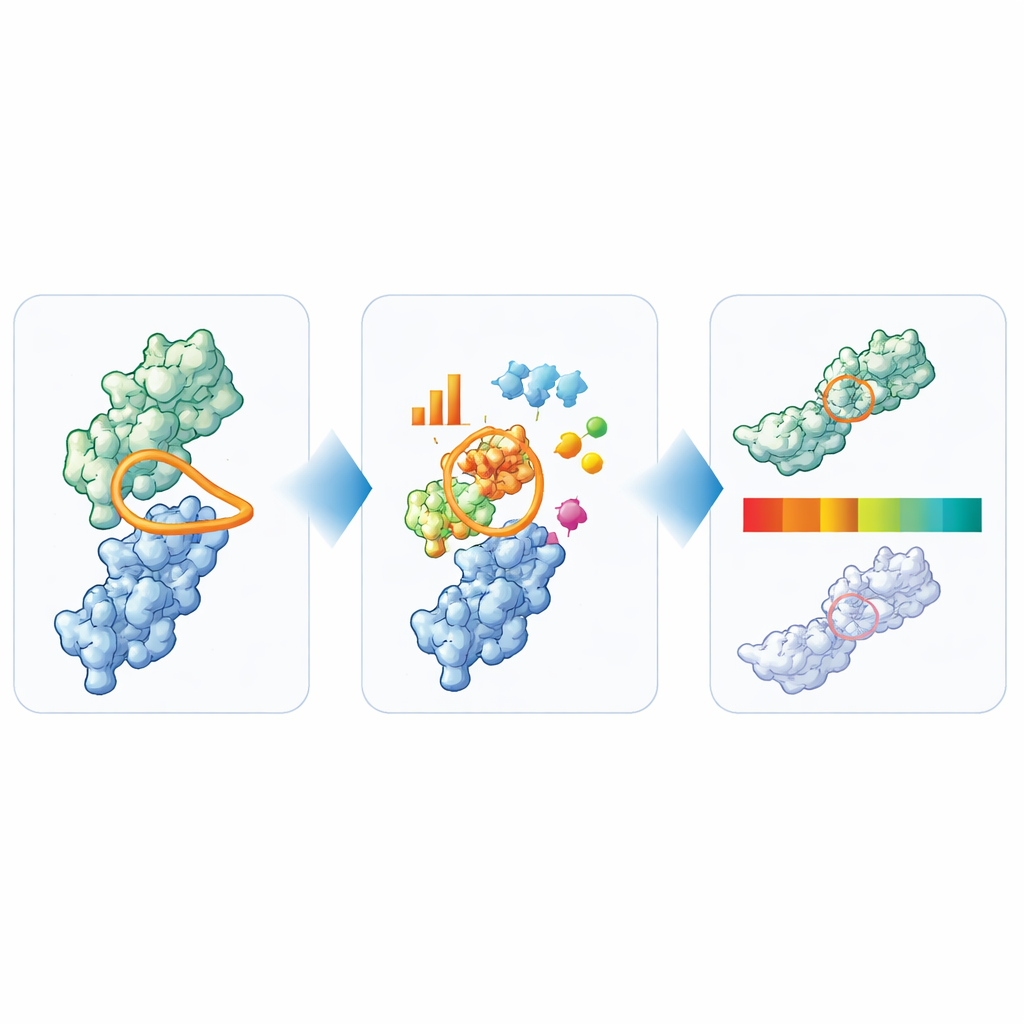
Convertir la estructura en semáforos sencillos
A partir de su análisis amplio, los autores destilaron seis características clave que en conjunto capturan las principales preocupaciones de desarrollabilidad para nanocuerpos: longitud total de los bucles, la longitud y compactación específicas del CDR3 y el tamaño de los parches superficiales hidrofóbicos, con carga positiva y con carga negativa alrededor del sitio de unión. A continuación utilizaron los 36 nanocuerpos que han llegado a ensayos clínicos para establecer límites prácticos para cada medida. Los valores en la región central, bien poblada, se etiquetan como «verde», los límites como «ámbar» y los valores claramente atípicos como «rojo». Para probar cuán informativas son estas señales, aplicaron TNP a 72 nanocuerpos propietarios adicionales y compararon las alertas con un extenso panel de ensayos de laboratorio. Los nanocuerpos que TNP marcó como atípicos claros normalmente también mostraron múltiples señales de advertencia experimentales, mientras que los que parecían limpios computacionalmente con mayor frecuencia se comportaron bien en el laboratorio.
Qué significa esto para los tratamientos del mañana
Para los no especialistas, el mensaje central es que la forma y el patrón de superficie de un nanocuerpo pueden ahora convertirse en un perfil de desarrollabilidad claro antes de comenzar trabajos de laboratorio costosos. El Therapeutic Nanobody Profiler no reemplaza los experimentos, y todavía se producen desajustes entre predicciones y ensayos, especialmente porque las pruebas de laboratorio se realizaron en nanocuerpos fusionados a fragmentos de anticuerpos más grandes. Pero al señalar rápidamente candidatos con bucles inusualmente largos o muy plegados o con parches superficiales problemáticos, TNP ayuda a orientar la atención hacia nanocuerpos con más probabilidades de convertirse en fármacos fiables. A medida que más nanocuerpos entren en ensayos clínicos y amplíen el conjunto de referencia, esta herramienta debería volverse aún más precisa, acelerando el diseño de medicamentos pequeños y robustos similares a anticuerpos para una amplia gama de enfermedades.
Cita: Gordon, G.L., Gervasio, J., Souders, C. et al. Characterising nanobody developability to improve therapeutic design using the Therapeutic Nanobody Profiler. Commun Biol 9, 344 (2026). https://doi.org/10.1038/s42003-026-09594-y
Palabras clave: nanocuerpos, desarrollabilidad de fármacos biológicos, perfilado computacional, ingeniería de anticuerpos, estabilidad de proteínas