Clear Sky Science · es
La degradación mediada por DTX1 de TUBB3 en células de Kupffer mitiga la progresión del carcinoma hepatocelular al regular la polarización M1/M2
Por qué importan los “vecinos” inmunitarios del hígado
La mayoría de la gente piensa en el cáncer como una enfermedad de células rebeldes que crecen fuera de control. Pero los tumores viven en un vecindario bullicioso de células inmunitarias, vasos sanguíneos y tejido de soporte que puede tanto combatir el cáncer como ayudarlo a crecer silenciosamente. Este estudio se centra en el cáncer de hígado —específicamente el carcinoma hepatocelular— y revela cómo una proteína dentro de células inmunitarias especializadas del hígado puede inclinar la balanza entre una respuesta antitumoral y un entorno que favorece al tumor. Comprender este interruptor de control oculto podría abrir nuevas vías para mejorar las inmunoterapias actuales.
Un cáncer de hígado impulsado por su entorno
El hígado es rico en células inmunitarias, incluida una población residente llamada células de Kupffer que normalmente ayudan a mantener el órgano sano. En el cáncer hepático, muchas de estas células se transforman en macrófagos asociados a tumores que pueden atacar el cáncer (un estado tipo M1) o protegerlo (un estado tipo M2). Los pacientes cuyos tumores están llenos de macrófagos de tipo M2 suelen tener peor pronóstico y a menudo responden mal a fármacos que desbloquean las defensas inmunitarias, como los inhibidores de PD-1. Los autores comenzaron examinando bases de datos públicas de genes y muestras de pacientes para buscar moléculas vinculadas tanto al cáncer de hígado como a estos macrófagos, y se centraron en una proteína estructural llamada TUBB3, que resultó estar inesperadamente abundante en tejido tumoral.
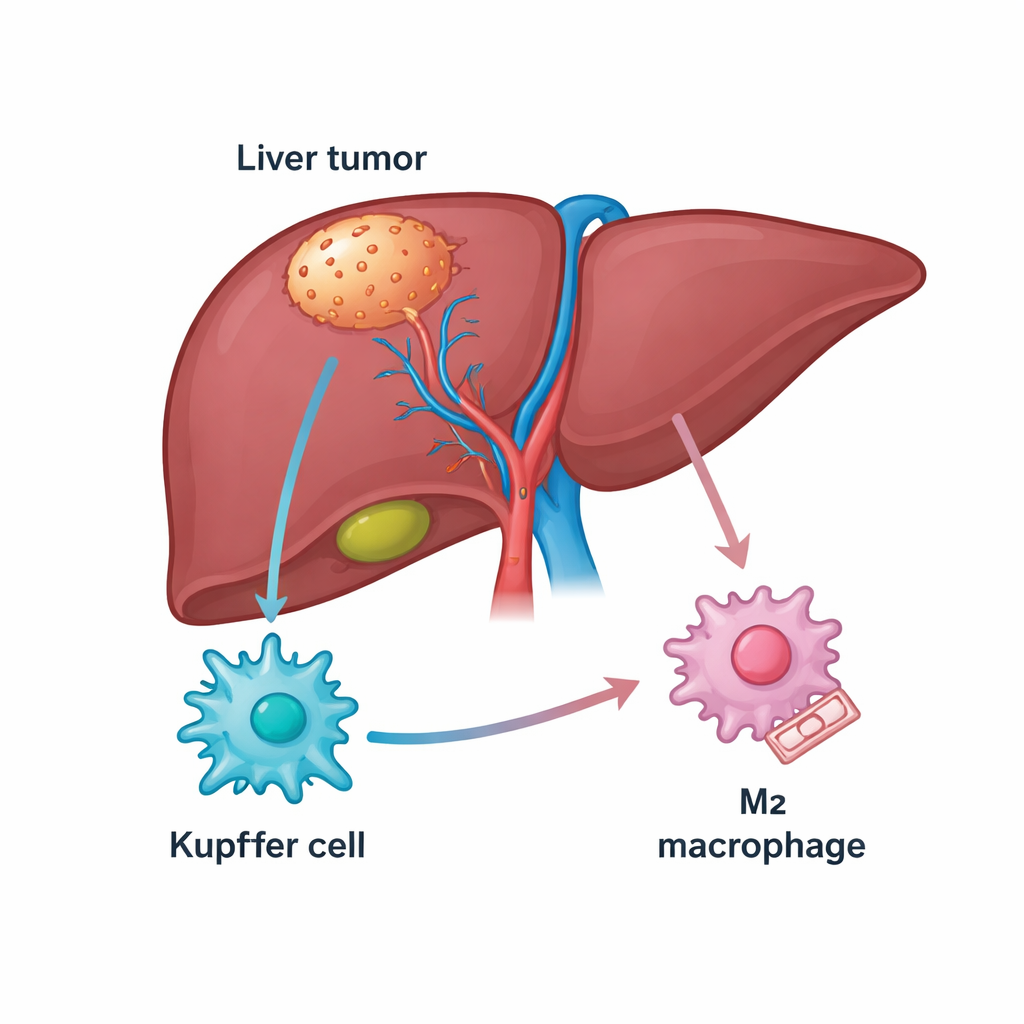
Una proteína sorprendente que empuja a las células inmunitarias a ayudar al tumor
TUBB3 es más conocida como un componente de los “rieles” microscópicos dentro de las células, pero también se ha relacionado con comportamiento agresivo y resistencia a fármacos en varios cánceres. Aquí, los investigadores hallaron que los niveles de TUBB3 eran mucho más altos en los tumores hepáticos que en el tejido sano adyacente, y que los pacientes con más TUBB3 tendían a tener una supervivencia más corta. Mediante técnicas de tinción, mostraron que TUBB3 se enriquecía especialmente en las células de Kupffer dentro de los tumores, y su presencia se correlacionaba fuertemente con marcadores del estado M2, que favorece al tumor. En otras palabras, las células de Kupffer cargadas de TUBB3 tenían más probabilidad de comportarse de forma que amortigua el ataque inmunitario y respalda el crecimiento tumoral.
Reprogramar macrófagos para frenar tumores hepáticos
Para probar causalidad, el equipo redujo los niveles de TUBB3 en células de Kupffer en experimentos de laboratorio. Cuando TUBB3 se redujo, estas células produjeron menos señales tipo M2, más señales tipo M1 y secretaron menos moléculas que normalmente suprimen la actividad inmunitaria. Las células de carcinoma hepático expuestas a estos macrófagos reprogramados crecieron más despacio, se dividieron menos y tuvieron menor capacidad de migrar e invadir. En ratones, mezclar células de cáncer hepático con células de Kupffer deficientes en TUBB3 condujo a tumores más pequeños, mayor muerte de células cancerosas y una mayor afluencia de células CD8 citotóxicas cargadas de proteínas destructivas. Si los macrófagos se eliminaban por completo de los animales, el beneficio de bloquear TUBB3 desaparecía en gran medida, lo que subraya que el efecto se transmite a través de estas células inmunitarias y no solo de las células tumorales.
Descubriendo un freno interno sobre una vía señalizadora clave
El estudio también investigó cómo TUBB3 ejerce esta influencia. Los autores se centraron en una vía bien conocida de crecimiento y supervivencia controlada por las proteínas PTEN y AKT, que también determina si los macrófagos adoptan una identidad M1 o M2. Encontraron que disminuir TUBB3 aumentaba PTEN, lo que a su vez reducía las “etiquetas fosfato” activadoras en AKT, empujando a los macrófagos hacia el estado que combate el tumor. Cuando reactivaron artificialmente AKT, los macrófagos volvieron al patrón M2 y las células cancerosas recuperaron su comportamiento agresivo, incluso en ausencia de TUBB3. Esto sitúa a TUBB3 río arriba de PTEN y AKT como una especie de dial interno para el comportamiento de los macrófagos.
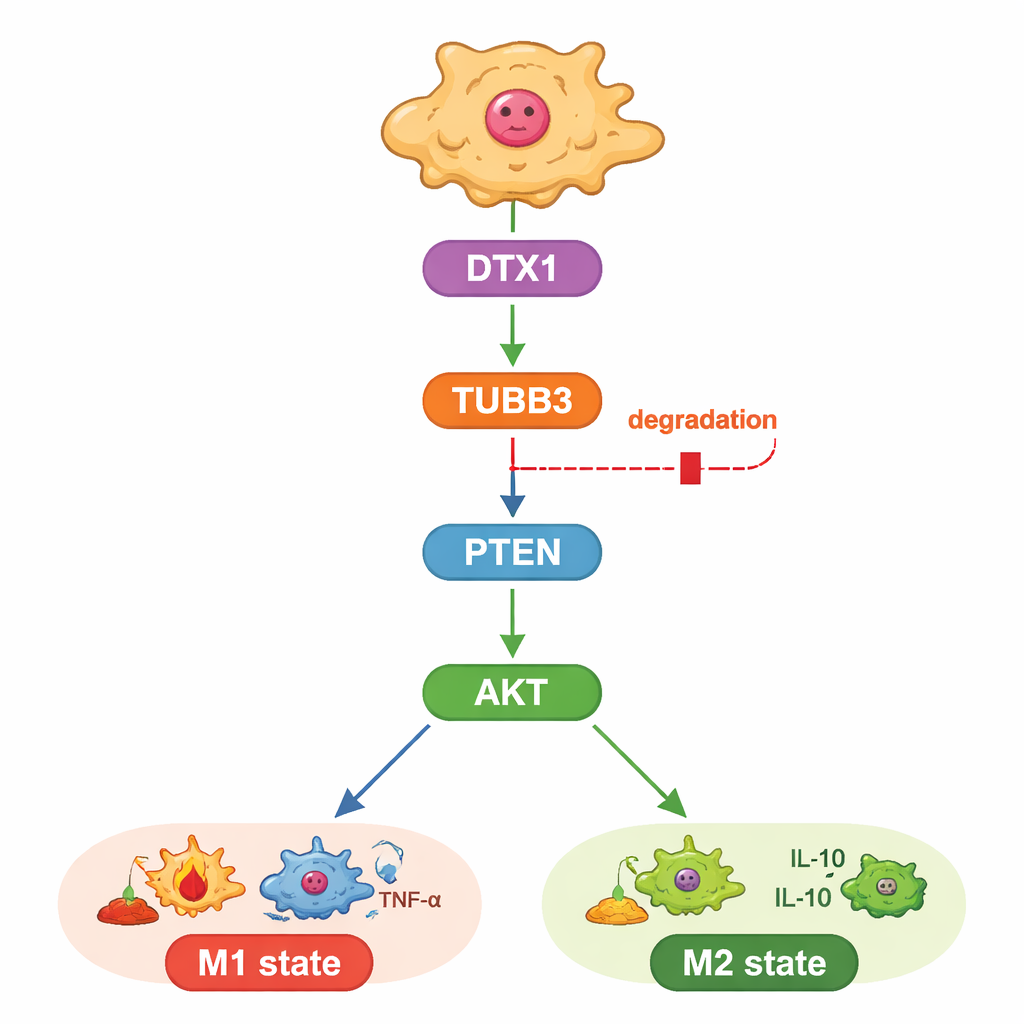
Una etiqueta de basura integrada que podría reactivarse
Finalmente, los investigadores se preguntaron por qué TUBB3 es tan abundante en los tumores hepáticos. Combinando predicciones bioinformáticas con datos de expresión, identificaron a una enzima llamada DTX1, parte de una familia que etiqueta proteínas para su eliminación, como regulador probable. Los niveles de DTX1 eran más bajos en tumores hepáticos que en tejido sano y se asociaban con mejores resultados en pacientes y con una mayor presencia de macrófagos tipo M1. En células, aumentar DTX1 aceleró la degradación de TUBB3, atenuó la actividad de AKT y empujó a los macrófagos hacia el estado antitumoral, frenando el crecimiento de las células cancerosas. Revertir esto reintroduciendo TUBB3 adicional borró los beneficios de DTX1, tanto en cultivos como en tumores de ratón. En conjunto, estos resultados trazan una línea clara desde DTX1 a través de TUBB3 y PTEN/AKT hacia el tono inmunitario del tumor.
Qué significa esto para el tratamiento futuro del cáncer de hígado
Para los no especialistas, el mensaje clave es que este trabajo identifica un sistema de control previamente oculto dentro de las células inmunitarias residentes del hígado que decide si ayudan o dificultan al cáncer. Cuando la enzima etiquetadora DTX1 es baja, TUBB3 se acumula, se activa una vía de crecimiento y las células de Kupffer se deslizan hacia un modo que apoya al tumor y atenúa el efecto de la inmunoterapia. Restaurar esta vía —reduciendo TUBB3, aumentando DTX1 o ajustando con cuidado la señal PTEN/AKT— podría reavivar las defensas inmunitarias locales y hacer que tratamientos como los inhibidores de PD-1 sean más efectivos. Aunque tales estrategias aún están en fase experimental, ponen de relieve la promesa de tratar no solo las células tumorales, sino también a los “vecinos” inmunitarios que influyen de forma decisiva en el comportamiento del cáncer de hígado.
Cita: Sun, J., Sun, T., Zhang, Y. et al. DTX1-mediated degradation of TUBB3 in Kupffer cells mitigates hepatocellular carcinoma progression by regulating M1/M2 polarization. Commun Biol 9, 311 (2026). https://doi.org/10.1038/s42003-026-09593-z
Palabras clave: carcinoma hepatocelular, macrófagos asociados a tumores, células de Kupffer, inmunoterapia, señalización AKT