Clear Sky Science · es
Esparsificación y descarrelación de la actividad de las células granulares en el giro dentado por la noradrenalina
Por qué un pico de activación puede afinar los recuerdos
Momentos que nos sacuden—un susto en el tráfico, un comentario inesperado, un giro sorprendente en una película—suelen permanecer en la memoria mucho mejor que un día corriente. Este estudio explora una razón clave: un químico cerebral relacionado con la activación, la noradrenalina, remodela discretamente cómo una puerta de entrada crítica de la memoria en el hipocampo filtra y separa experiencias, ayudando a que sucesos parecidos sean más fáciles de distinguir después.
El portero cerebral para experiencias similares
Dentro del hipocampo se encuentra el giro dentado, una región que actúa como portero de los recuerdos nuevos. Recibe información rica desde la corteza entorrinal—señales sobre dónde estamos y qué sucede a nuestro alrededor—y las convierte en patrones de actividad en las células granulares, sus neuronas principales. La teoría y los experimentos sugieren que estos patrones deben ser “esparsos” (solo unas pocas células activas a la vez) y “descorrelacionados” (experiencias diferentes activan conjuntos distintos de células) para que los recuerdos no se mezclen. Sin embargo, cómo ocurre esta transformación a nivel de células y circuitos concretos ha permanecido poco claro.
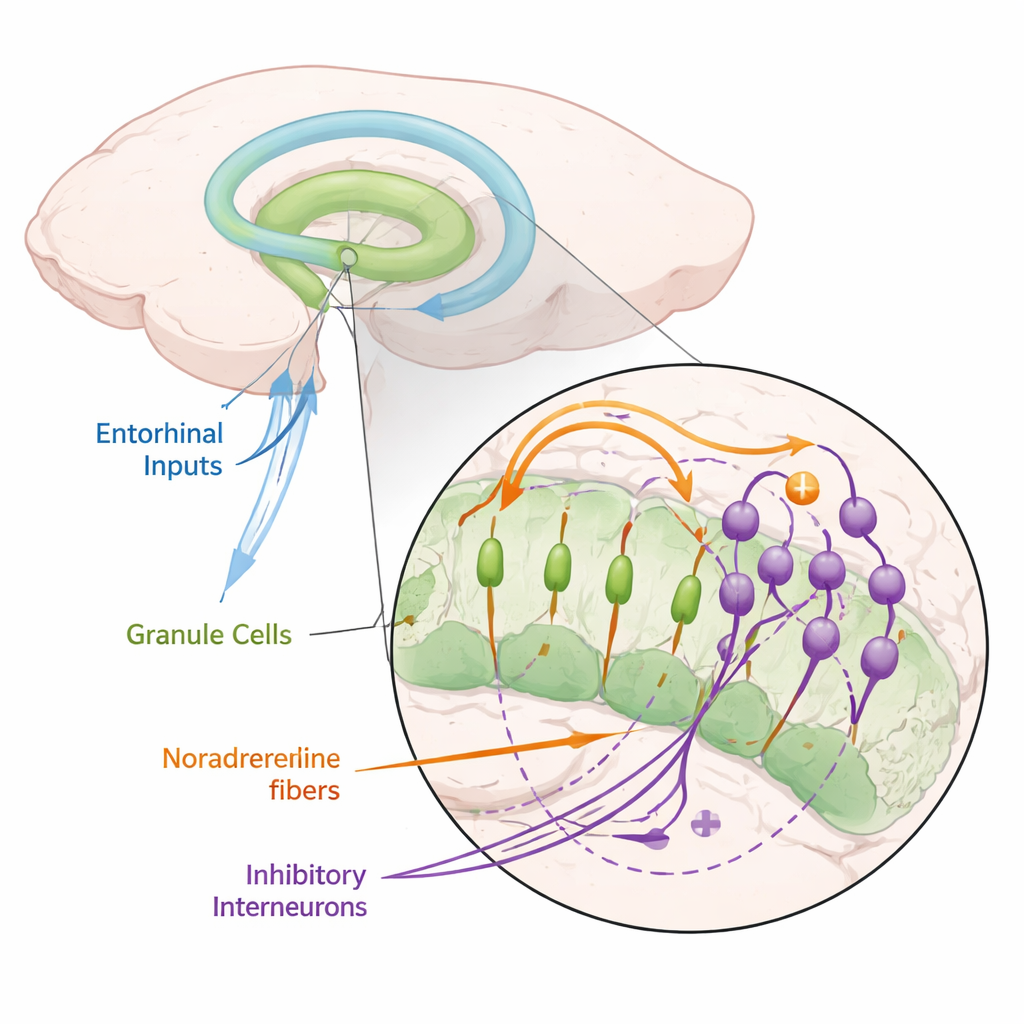
Un químico de la activación que calla células clave de la memoria
Los autores se centraron en la noradrenalina, un neuromodulador liberado por neuronas en una pequeña región del tronco encefálico llamada locus coeruleus, que se activa durante la atención, la novedad y el estrés. En ratones, expresaron proteínas sensibles a la luz en estas neuronas noradrenérgicas, lo que les permitió liberar noradrenalina a demanda con destellos de luz. Cuando estimularon la vía de entrada principal al giro dentado y registraron de las células granulares, descubrieron que la liberación de noradrenalina reducía fuertemente la tendencia de estas células a disparar. Esta supresión se observó tanto a nivel de neuronas individuales como en señales poblacionales, y se reprodujo simplemente bañando cortes cerebrales en noradrenalina. Bloquear los receptores de noradrenalina eliminó el efecto, mostrando que dependía realmente de este mensajero químico.
No menos excitación, sino frenos más potentes
Para entender cómo la noradrenalina silenciaba las células granulares, el equipo comprobó las posibilidades obvias. No cambió de forma significativa el voltaje de reposo ni la resistencia de entrada de las células granulares, lo que indica que su excitabilidad básica se mantenía aproximadamente igual. Tampoco debilitó las corrientes excitatorias que estas células reciben desde la corteza entorrinal. En cambio, cuando bloquearon los receptores GABAA, que median la inhibición, la noradrenalina ya no pudo suprimir el disparo de las células granulares. Mediciones detalladas de corrientes mostraron que la noradrenalina potenció selectivamente una forma rápida de inhibición de tipo feedforward: las señales excitatorias entrantes primero activaban un conjunto de interneuronas, que luego inhibían rápidamente a las células granulares antes de que estas pudieran disparar. Los análisis temporales revelaron que esta corriente inhibitoria sensible a la noradrenalina llegaba justo después de la excitación directa, pero antes de que la población principal de células granulares disparase, una marca distintiva de los frenos feedforward.
Interneuronas especializadas que imponen el tiempo
¿Qué interneuronas proporcionaban esta inhibición crucial? Sorprendentemente, las células que expresan parvalbúmina, pensadas durante mucho tiempo como dominantes en el control feedforward rápido, no eran las responsables—la noradrenalina en realidad las hacía menos activas. En su lugar, las protagonistas fueron interneuronas que expresan colecistoquinina (células CCK). Estas células reciben entrada directa de las mismas fibras corticales que excitan las células granulares y disparan justo antes que las células granulares, lo que indica un papel feedforward. La noradrenalina despolarizó las células CCK, haciéndolas más fáciles de reclutar, y aumentó la probabilidad de que las señales de entrada las activaran, sin cambiar la fuerza de cada conexión inhibidora individual. Cuando los investigadores bloquearon farmacológicamente la salida de las células CCK, la noradrenalina ya no pudo suprimir la actividad de las células granulares. En efecto, la noradrenalina activa un circuito de interneuronas CCK que impone una ventana temporal muy estrecha durante la cual los impulsos excitatorios entrantes pueden activar con éxito a las células granulares.
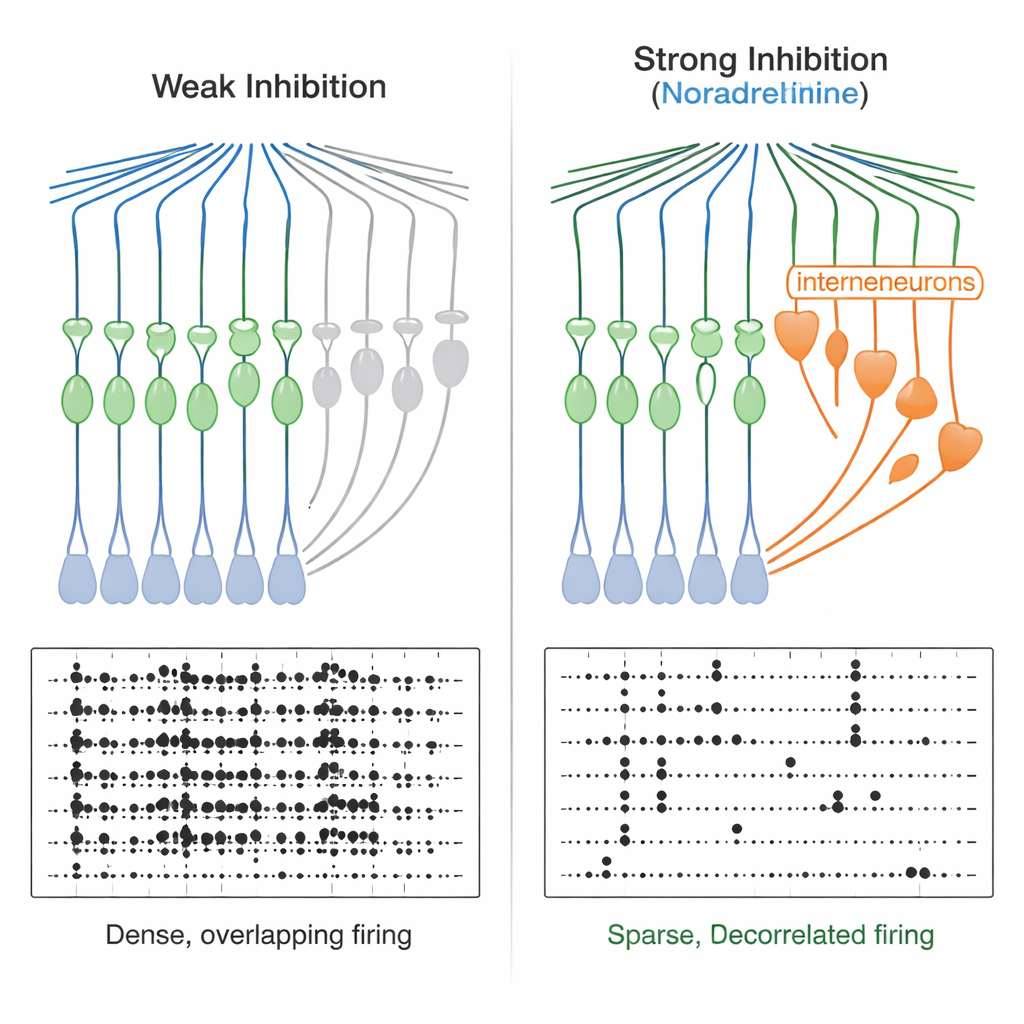
De ventanas estrechas a códigos de memoria más limpios
Este afinamiento temporal tiene consecuencias poderosas. Cuando el equipo entregó pares de entradas excitatorias breves, encontró que en condiciones normales las células granulares podían integrar entradas espaciadas por decenas de milisegundos en un disparo. Con noradrenalina presente, la ventana se redujo a solo unos pocos milisegundos—las células granulares pasaron a responder casi exclusivamente a entradas altamente sincronizadas. Modelos computacionales de red confirmaron que fortalecer y acelerar la inhibición feedforward producía una salida más esparsa y reducía las superposiciones entre patrones de actividad, mejorando la “descorrelación”. Experimentalmente, cuando los investigadores enviaron dos patrones de entrada similares, pero no idénticos, al giro dentado, las células granulares respondieron con patrones de disparo más distintos en presencia de noradrenalina, tanto en registros de células individuales como en imágenes de calcio a través de muchas células. Al mismo tiempo, la actividad global de las células granulares se volvió más esparsa.
Cómo la activación puede ayudarnos a separar recuerdos parecidos
Para el lector general, la conclusión es que la noradrenalina, liberada cuando estamos alerta o emocionalmente comprometidos, ayuda a que un filtro de memoria clave en el hipocampo sea más selectivo. Al energizar una clase específica de interneuronas inhibitorias, estrecha la ventana temporal durante la cual las entradas pueden activar las células granulares, de modo que solo las señales estrechamente sincronizadas y significativas atraviesan. Esto reduce el disparo global, hace que los patrones de actividad se solapen menos y ayuda al cerebro a almacenar experiencias similares—como dos aulas o dos conversaciones—como recuerdos separados en lugar de una mancha indistinta. El trabajo revela un mecanismo de circuito concreto que vincula la activación momentánea con recuerdos más precisos y menos confusos.
Cita: Glovaci, I., Mihály, A., Vervaeke, K. et al. Sparsification and decorrelation of granule cell activity in the dentate gyrus by noradrenaline. Commun Biol 9, 323 (2026). https://doi.org/10.1038/s42003-026-09592-0
Palabras clave: noradrenalina, giro dentado, interneuronas inhibitorias, separación de patrones, memoria episódica