Clear Sky Science · es
Información estructural sobre la helicasa WRN revela estados conformacionales y oportunidades para el descubrimiento de fármacos contra cáncer MSI‑H
Por qué importa para el tratamiento del cáncer
Ciertos cánceres tienen una debilidad intrínseca: su capacidad para reparar errores en el ADN está comprometida. Una proteína llamada helicasa WRN actúa como una herramienta molecular de reparación que mantiene con vida a estos tumores frágiles. Este estudio revela, con detalle atómico, cómo WRN se desplaza a lo largo del ADN y cómo fármacos experimentales pueden bloquear su movimiento, ofreciendo una hoja de ruta para nuevos tratamientos que eliminen selectivamente estas células cancerosas vulnerables mientras preservan el tejido sano.
El manitas del ADN bajo el microscopio
La helicasa WRN forma parte del equipo de mantenimiento de la célula, ayudando a desenrollar el ADN para que los daños puedan detectarse y repararse. Las personas que nacen sin WRN funcional desarrollan el síndrome de Werner, un trastorno raro caracterizado por envejecimiento prematuro, lo que muestra lo crucial que es esta proteína para el mantenimiento del genoma. Los tumores con “inestabilidad de microsatélites alta” (MSI‑H), una alteración frecuente en el cáncer colorrectal y en otros tipos, resultan especialmente dependientes de WRN. Cuando WRN se inactiva en estas células, su ADN ya frágil se desintegra con rapidez y las células cancerosas mueren. Eso convierte a WRN en un objetivo atractivo para fármacos, pero hasta ahora los científicos carecían de una visión clara de cómo cambia la forma de la proteína mientras capta ADN, consume su combustible químico y se desplaza a lo largo del material genético.
Observando a WRN flexionar y respirar
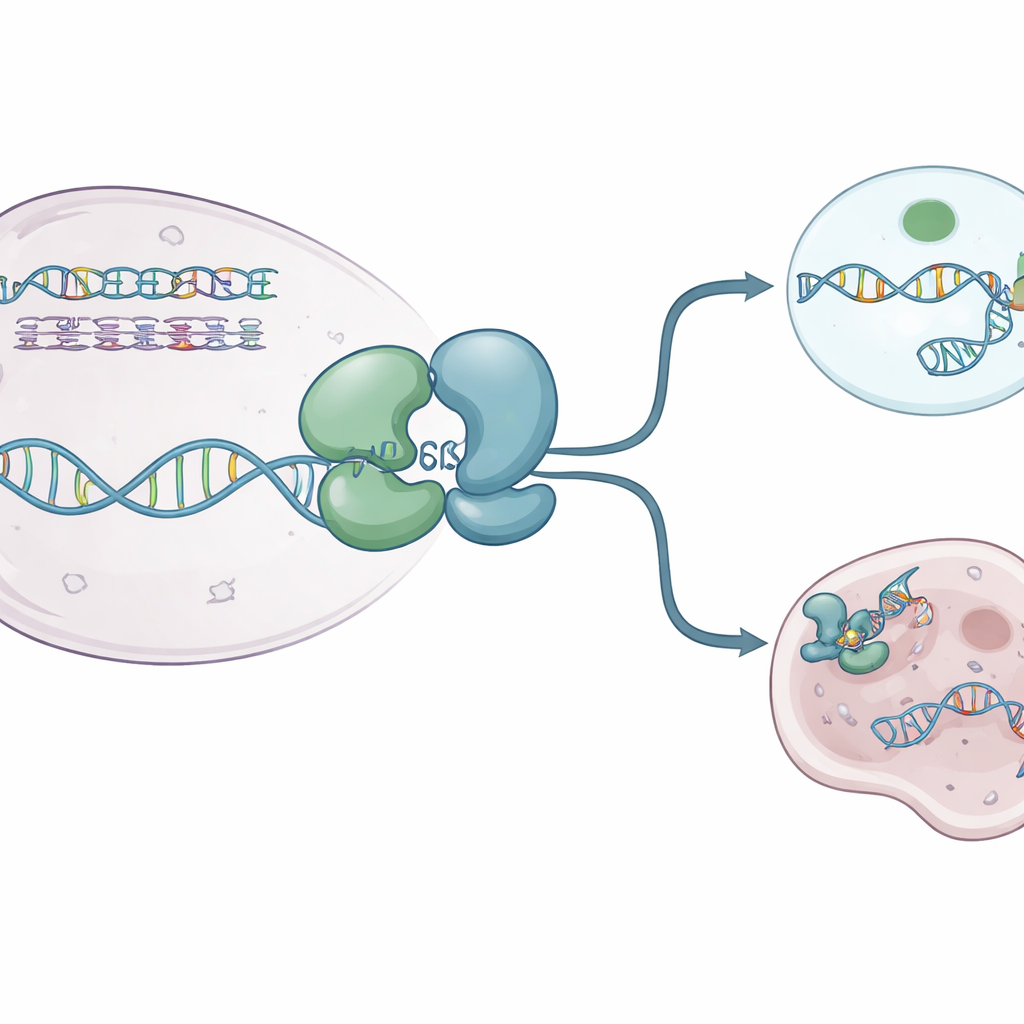
Los autores utilizaron cristalografía de rayos X para capturar varias “instantáneas” de alta resolución del núcleo helicasa humano WRN. Resolviendo estructuras de WRN sola y de WRN unida a ADN monocatenario y a una molécula de combustible similar al ATP pero no hidrolizable, mostraron que la proteína está construida por dos lóbulos principales conectados por una bisagra flexible que se comporta como una articulación que respira. En su estado de reposo, sin combustible, WRN adopta una forma compacta “cerrada” en la que los lóbulos quedan próximos. Cuando están presentes la molécula similar al ATP y el ADN, los lóbulos se separan hacia una configuración más “abierta” que puede acunar el ADN en una ranura cargada positivamente. Un pequeño bucle aromático dentro de WRN se remodela en una hélice corta y se interpone entre las bases del ADN, actuando como un trinquete que ayuda a la proteína a avanzar sin deslizarse hacia atrás.
Cómo los fármacos actuales apagan WRN
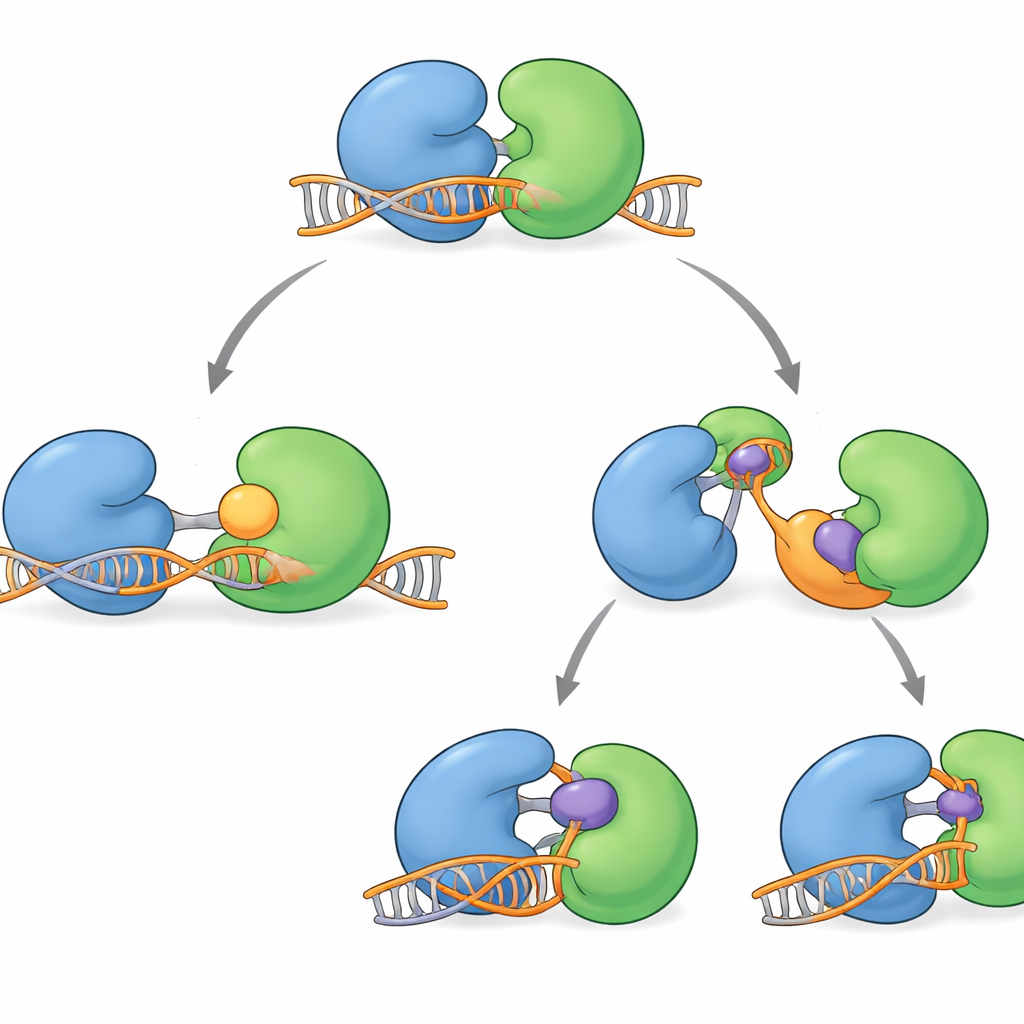
Varios compuestos bloqueadores de WRN han entrado recientemente en ensayos clínicos. No taponan directamente la ranura activa de la proteína. En cambio, actúan a distancia, agarrando la región de la bisagra y bloqueando a WRN en conformaciones que no pueden unirse correctamente al ADN. Algunas moléculas, como HRO761 y un candidato clínico relacionado de GSK, giran un lóbulo aproximadamente 180 grados respecto al otro, creando una forma “retorcida” dramática que queda fuera del ADN. Otras, incluyendo VVD‑133214 y un compuesto estrechamente relacionado estudiado aquí, inmovilizan a WRN en una disposición fuertemente “cerrada” que no expone las superficies clave para agarrar el ADN. Experimentos biofísicos confirmaron que, cuando estos fármacos están unidos, WRN ya no puede formar un complejo estable con ADN monocatenario, cortando de hecho el vínculo entre el uso de ATP y el desenrollado del ADN.
Cómo aprenden a escapar las células cancerosas
Para ver cómo los tumores podrían eludir estos fármacos, el equipo cultivó células de cáncer colorrectal MSI‑H en presencia de inhibidores de WRN durante semanas o meses. Aparecieron poblaciones resistentes con rapidez. El análisis genético mostró que, en cada caso, las células habían adquirido un único cambio preciso en el gen WRN cerca de la bisagra donde se unen los fármacos. Una mutación debilitó el efecto del inhibidor que favorece el “estado retorcido” HRO761, mientras que otra mutación redujo la sensibilidad a VVD‑133214, que favorece el estado cerrado. Además, muchas células resistentes aumentaron la producción de WRN, dándose más copias del blanco y diluyendo en parte el impacto del fármaco. Estos hallazgos repiten patrones de resistencia observados con otros fármacos dirigidos contra el cáncer, donde pequeños ajustes estructurales en la proteína diana o su sobreexpresión pueden atenuar el tratamiento.
Mirando hacia bloqueadores de WRN más inteligentes
En conjunto, las nuevas estructuras trazan un ciclo de trabajo completo de WRN mientras se aferra al ADN, avanza y luego se reinicia. También muestran que los compuestos clínicos actuales estabilizan principalmente formas de la proteína “fuera del ADN”. Para el lector general, el punto clave es que ahora entendemos dónde WRN es vulnerable y cómo los tumores pueden adaptarse. Esto sugiere una próxima generación de inhibidores que se unan a WRN cuando está bloqueada sobre el ADN, potencialmente atrapándola en un estado tóxico—de manera similar a fármacos exitosos que atrapan a otras enzimas de reparación del ADN. Tales bloqueadores de WRN “on‑DNA”, usados solos o junto con agentes existentes, podrían ofrecer maneras más duraderas de explotar la debilidad oculta de los cánceres MSI‑H.
Cita: Fletcher, C.T., Mornement, A.A., Barrett, C. et al. Structural insights into WRN helicase reveal conformational states and opportunities for MSI-H cancer drug discovery. Commun Biol 9, 334 (2026). https://doi.org/10.1038/s42003-026-09584-0
Palabras clave: helicasa WRN, inestabilidad de microsatélites, reparación del ADN, inhibidores alostéricos, resistencia a fármacos