Clear Sky Science · es
PiR48444 inhibe la diferenciación osteogénica de las CMM y la regeneración ósea mediante la diana METTL7A/eIF4E mediada de la metilación m6A de BMP2
Por qué las moléculas diminutas importan para los huesos rotos
Las fracturas y la pérdida ósea relacionada con la edad son problemas comunes, y los médicos buscan emplear células madre para ayudar al cuerpo a reconstruir el esqueleto dañado. Sin embargo, estas células madre no siempre generan nuevo hueso con la eficiencia deseada, sobre todo en personas mayores o en tejidos inflamados. Este estudio descubre una pequeña molécula de ARN, llamada piR48444, que actúa como un freno molecular sobre las células madre formadoras de hueso. Al liberar ese freno, los investigadores muestran que podría ser posible potenciar la reparación ósea y proteger frente a la pérdida de masa ósea.
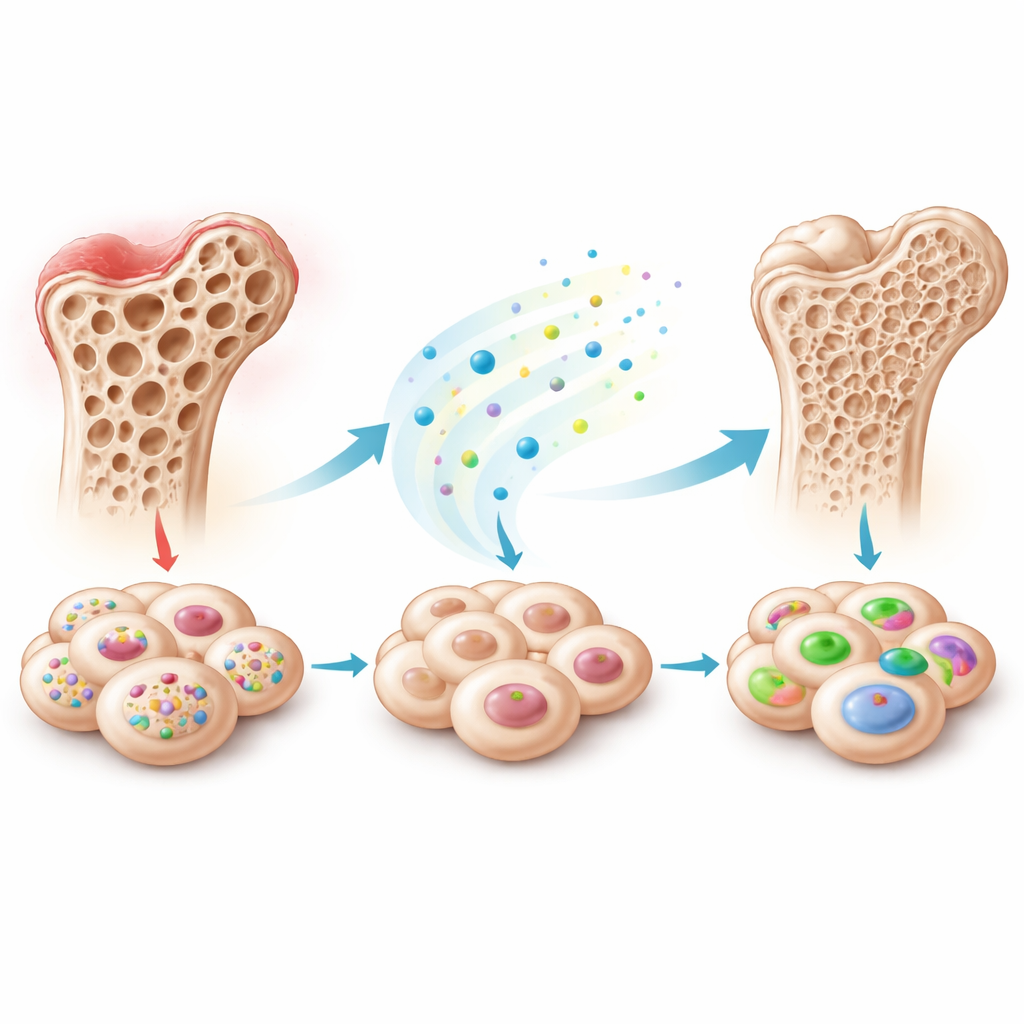
Un freno oculto dentro de muchos tipos de células madre
El equipo se centró en las células madre mesenquimales, células versátiles que pueden convertirse en hueso, cartílago, tejido graso y más, y que se aíslan de tejidos como la médula ósea, los dientes de leche y la grasa. Cuando estas células se inducen a formar hueso en el laboratorio, miles de genes y pequeños ARN modifican su actividad. Al secuenciar estas moléculas en células madre procedentes de dientes de leche exfoliados, los investigadores observaron que un ARN pequeño en particular, piR48444, disminuía de forma sostenida a medida que las células se orientaban hacia el hueso. Luego comprobaron otros tipos de células madre y vieron el mismo patrón: las células que formaban más hueso tenían menos piR48444, lo que sugiere que esta molécula podría normalmente frenar su capacidad osteogénica.
De las placas de cultivo a los huesos vivos
Para probar esta hipótesis, los científicos alteraron los niveles de piR48444 en varios tipos de células madre. Cuando redujeron piR48444, las células depositaron más calcio, activaron genes vinculados al hueso y mostraron un aspecto más parecido a tejido óseo inmaduro bajo el microscopio. Cuando forzaron a las células a producir piR48444 en exceso, ocurrió lo contrario: la actividad relacionada con el hueso disminuyó. El equipo pasó entonces a modelos animales. Células madre con piR48444 silenciado se usaron para rellenar pequeños defectos craneales en ratones. Estas células modificadas generaron mucho más hueso nuevo que las células de control, según lo mostrado por exploraciones 3D de rayos X y tinciones histológicas, lo que sugiere que bloquear piR48444 puede mejorar de forma tangible la reparación ósea en organismos vivos.
Protegiendo huesos frágiles en enfermedad y envejecimiento
La pérdida ósea no está impulsada solo por lesiones, sino también por la inflamación y el envejecimiento. En células madre de la médula ósea expuestas a toxinas bacterianas, y en células madre de animales envejecidos, los niveles de piR48444 eran inusualmente altos mientras que los marcadores de formación ósea estaban bajos. Los investigadores diseñaron un «antagomir»: una molécula corta concebida para neutralizar piR48444 en el torrente sanguíneo, y la inyectaron en ratones con pérdida ósea inducida por inflamación o en ratones naturalmente envejecidos. En ambos modelos, los animales tratados conservaron mucho más de su hueso esponjoso interno, con trabéculas más densas y numerosas, mientras que la corteza ósea externa permaneció sin cambios. Esto indica que bloquear piR48444 puede proteger selectivamente la parte frágil y metabólicamente activa del esqueleto, la más vulnerable durante el envejecimiento y la inflamación crónica.
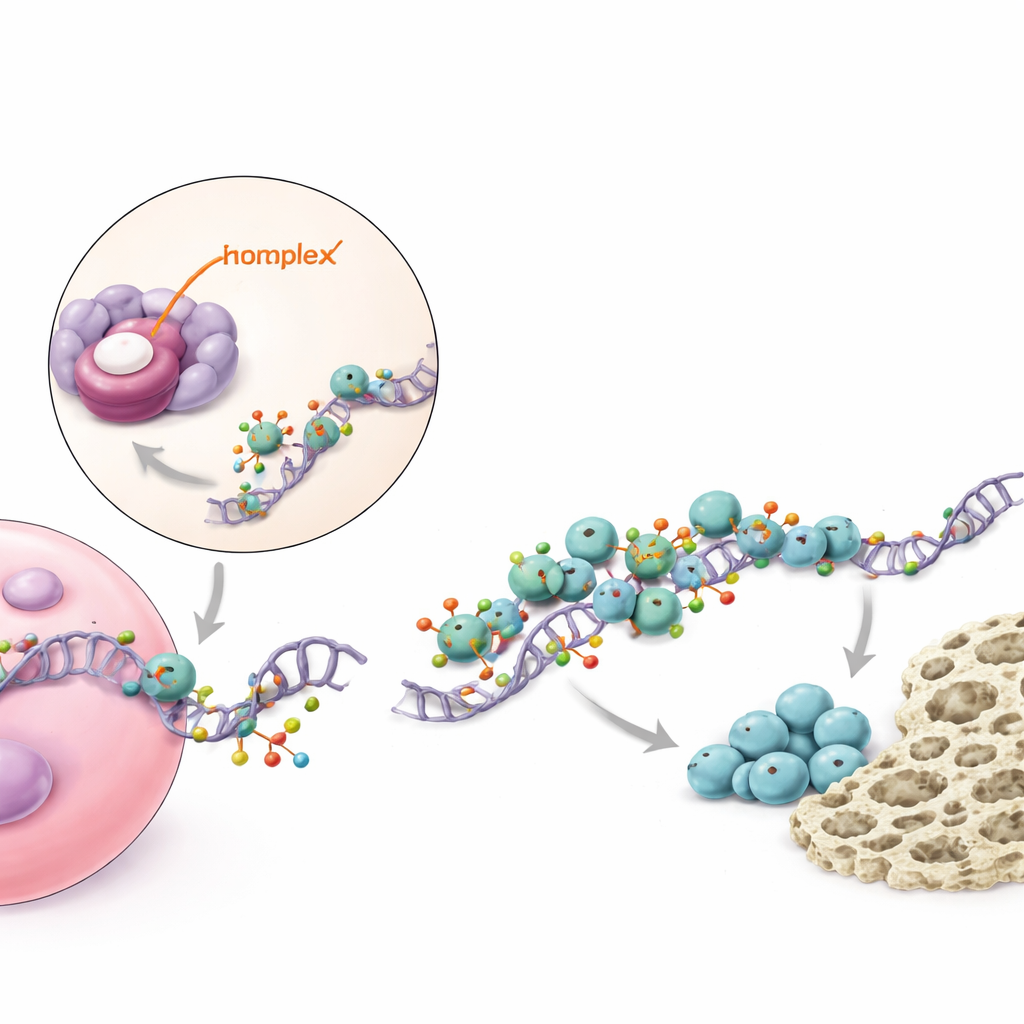
Un relevo molecular que potencia una señal clave para el hueso
Investigando en mayor profundidad, el estudio trazó cómo piR48444 ejerce sus efectos dentro de las células. El pequeño ARN se une y reprime una proteína llamada METTL7A, que actúa como una enzima que modifica los mensajeros que llevan el plano para BMP2, un factor de crecimiento conocido que estimula fuertemente la formación ósea. METTL7A añade pequeñas marcas químicas a los mensajeros de BMP2, haciendo que sean más estables y más fáciles de leer para la maquinaria celular de producción de proteínas. METTL7A también coopera con otra proteína, eIF4E, que ayuda a iniciar la síntesis proteica. Cuando piR48444 es abundante, METTL7A queda reprimida, menos mensajeros de BMP2 se marcan y traducen, y se produce menos proteína BMP2, por lo que las células madre tienen menos probabilidades de convertirse en hueso. Cuando se bloquea piR48444, aumentan METTL7A y BMP2, impulsando a las células hacia la formación ósea.
Lo que esto significa para la futura reparación ósea
En términos sencillos, los autores revelan una cadena de control en la que un pequeño ARN (piR48444) amortigua una enzima auxiliar (METTL7A), que a su vez limita una potente señal formadora de hueso (BMP2). Al cortar esta cadena a nivel de piR48444, pueden mejorar la capacidad osteogénica de diversas células madre y reducir la pérdida ósea en ratones. Si bien la seguridad, los efectos fuera de diana y las consecuencias a largo plazo requieren ensayos cuidadosos, el trabajo señala a piR48444 tanto como un posible marcador sanguíneo de riesgo de osteoporosis como una diana prometedora para fármacos destinados a potenciar la regeneración ósea basada en células madre en la clínica.
Cita: Zheng, Z., Li, X., Qin, W. et al. PiR48444 inhibits MSC osteogenic differentiation and bone regeneration via targeting METTL7A/eIF4E-mediated BMP2 m6A methylation. Commun Biol 9, 337 (2026). https://doi.org/10.1038/s42003-026-09583-1
Palabras clave: regeneración ósea, células madre mesenquimales, osteoporosis, ARN no codificante, señalización BMP2