Clear Sky Science · es
El apriete local de cationes deforma y ablanda el dímero de ARN
Por qué importa este pequeño giro en el ARN
Dentro de cada célula, el ADN y el ARN se doblan, estiran y torsionan constantemente mientras almacenan y usan la información genética. Estos movimientos no son solo detalles mecánicos: controlan cómo se leen los genes, cómo los virus se replican y cómo funcionarán los nuevos fármacos y nanodispositivos basados en ARN. Este estudio muestra que sales sencillas formadas por iones con carga positiva y negativa pueden cambiar de forma drástica cuán rígido o flexible es el ARN, y que el ARN responde de manera muy distinta al ADN. Comprender esta sutil danza de «ablandamiento y endurecimiento» podría ayudar a los científicos a diseñar mejor fármacos de ARN, vacunas y herramientas moleculares.
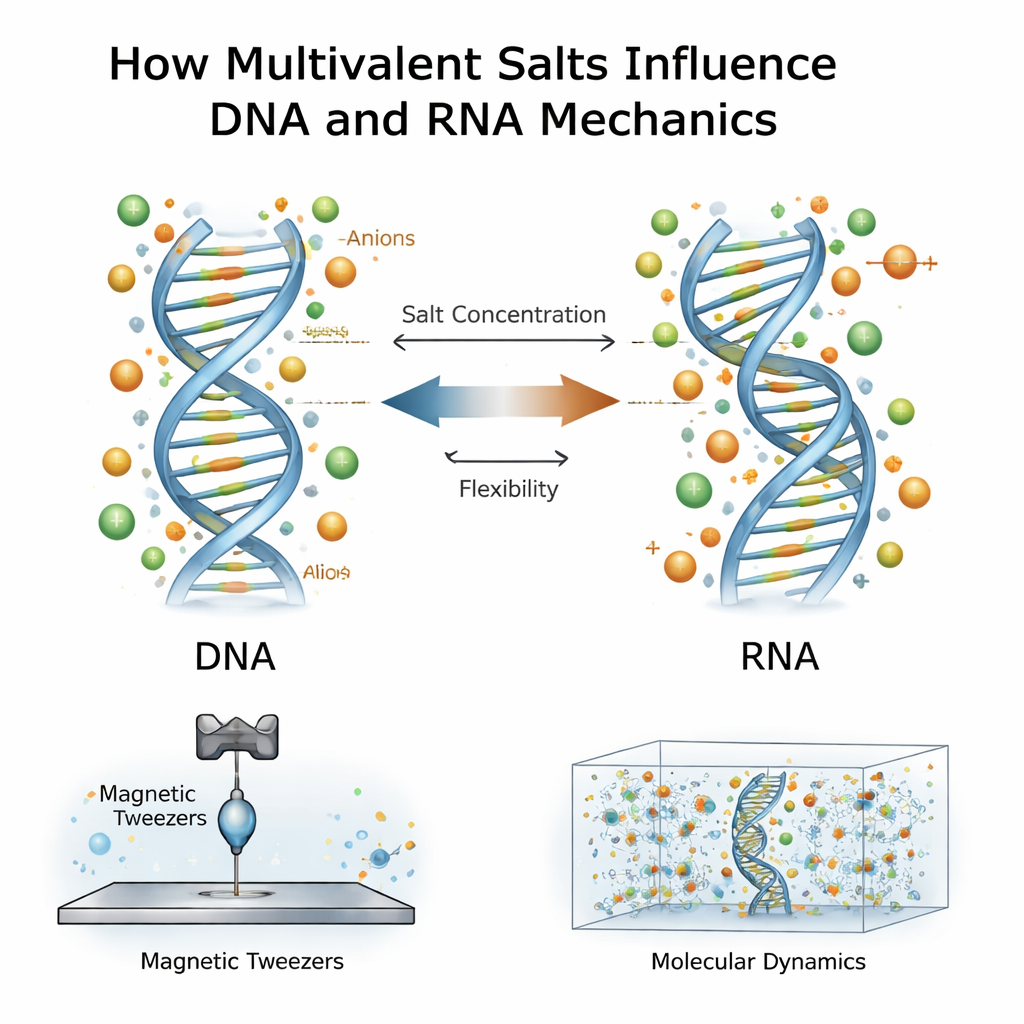
Entorno salino y moléculas genéticas
El ADN y el ARN tienen una fuerte carga eléctrica negativa, por lo que están rodeados por nubes de iones de carga opuesta en el agua. La mayor parte de trabajos anteriores se centró en iones con carga positiva, especialmente los multivalentes que llevan dos o tres cargas positivas, como el magnesio o la espermidina. Se sabe que estos iones mantienen las hebras de ADN juntas, las condensan o cambian la facilidad con que se doblan. El ARN, aunque químicamente similar al ADN, se comporta de forma distinta: suele ser más difícil de doblar pero más fácil de estirar. El trabajo nuevo plantea una pregunta más profunda: ¿qué ocurre cuando tanto los iones positivos como sus contrapartes negativas —los aniones— interactúan con el ADN y el ARN a niveles de sal muy altos, mucho mayores que los típicos en las células?
Tirando de moléculas individuales para medir la rigidez
Los investigadores usaron una técnica llamada pinzas magnéticas para estirar hélices dobles individuales de ADN o ARN una por una. Cada molécula estaba anclada a una superficie de vidrio en un extremo y a una pequeña perla magnética en el otro. Al mover imanes sobre la muestra, podían aplicar fuerzas controladas y registrar cuánto se extendía cada molécula y cómo giraba bajo tensión. A partir de estas curvas fuerza–extensión extrajeron cuatro rasgos mecánicos clave: lo difícil que es doblar la molécula, lo difícil que es estirarla, su longitud efectiva por par de bases y cómo el torsión cambia su longitud. Repetieron estas mediciones en un amplio rango de concentraciones de sales multivalentes para varias sales diferentes, incluida la espermidina y el cloruro de calcio.
El ADN se vuelve a endurecer, pero el ARN de repente se ablanda
En el caso del ADN, el comportamiento coincidió en gran medida con lo esperado. A medida que aumentaba la concentración de iones multivalentes positivos, el ADN primero se volvió más fácil de doblar: su rigidez disminuyó porque los iones neutralizaban su carga negativa. A niveles aún mayores, el exceso de iones positivos sobrecompensó, invirtiendo efectivamente la carga neta del ADN. Esta «inversión de carga» hizo que el ADN fuera de nuevo más difícil de doblar, por lo que su rigidez aumentó. Sorprendentemente, el ARN mostró el patrón opuesto y más dramático. A concentraciones bajas a moderadas de sal, su rigidez a la flexión aumentó: el dímero de ARN se volvió más recto y rígido. Pero a concentraciones muy altas, la rigidez a la flexión del ARN cayó a más de la mitad, y otras propiedades como su elasticidad y el comportamiento torsión–extensión se invirtieron de maneras inesperadas.
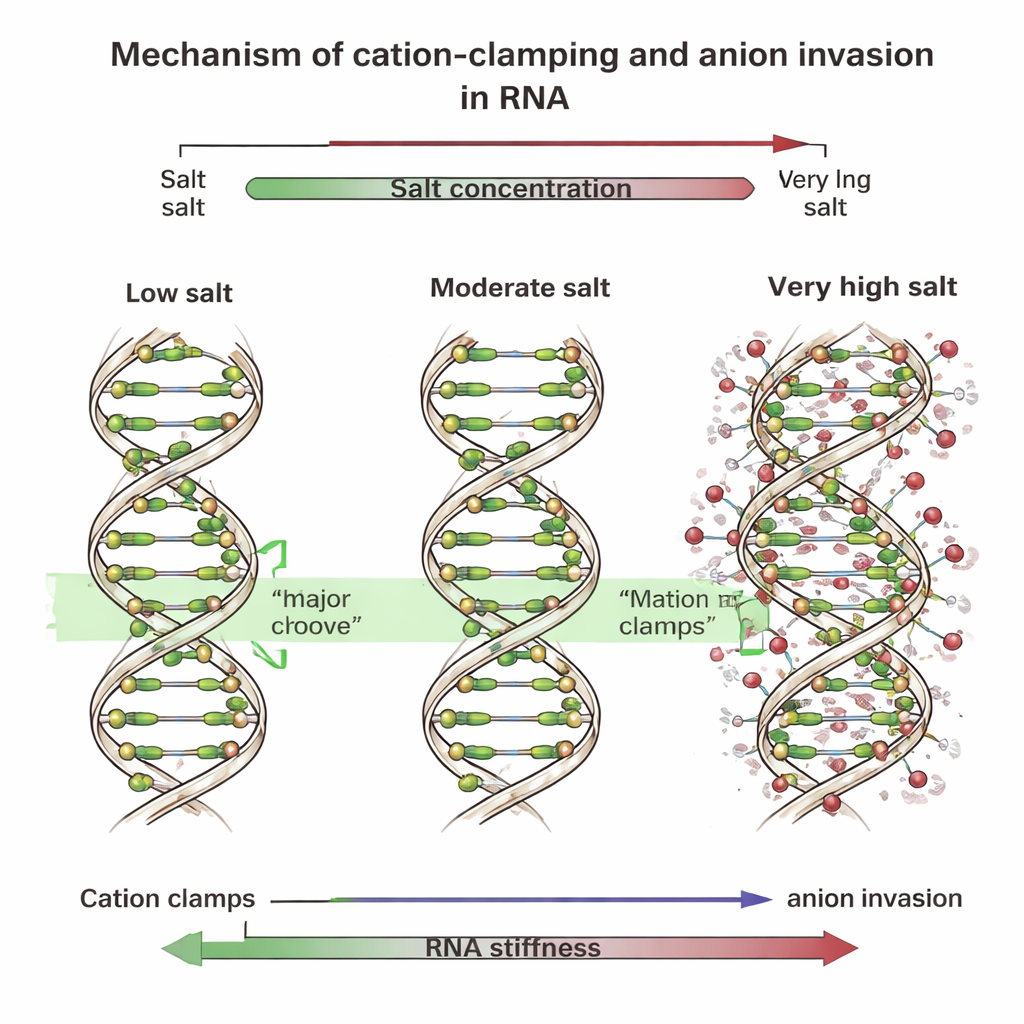
Abrojos, surcos e iones invasores
Para descubrir la causa, el equipo realizó simulaciones por ordenador detalladas que siguieron cada átomo de fragmentos cortos de ADN y ARN en agua salina. Estas simulaciones revelaron que a concentraciones bajas y moderadas, los iones multivalentes positivos se asientan en una amplia superficie del ARN llamada surco mayor. Allí forman «cierres de cationes» que puentean a través del surco, tirando de sus lados, enderezando la hélice y haciéndola más rígida. El ADN, cuyos surcos tienen otra forma, une principalmente estos iones a lo largo de su espina dorsal exterior. Sin embargo, a niveles de sal muy altos, muchos iones negativos —como el cloruro— se acercan a la columna vertebral del ARN e incluso penetran en el surco mayor. Su presencia trastorna los cierres ordenados, rompiéndolos en «cierres locales» irregulares y parcheados que deforman la hélice. Cuando los investigadores imitaron este efecto añadiendo resortes artificiales o fijando iones negativos adicionales cerca del ARN en las simulaciones, la columna del ARN se dobló más y su rigidez global se desplomó, tal como se observó en los experimentos.
Qué significa esto para futuras tecnologías basadas en ARN
En términos sencillos, el estudio muestra que el ARN puede volverse tanto más recto y rígido como más doblado y flexible simplemente cambiando el tipo y la concentración de las sales circundantes. A niveles modestos de iones multivalentes, las cargas positivas sujetan ordenadamente la superficie del ARN y lo refuerzan; en niveles extremos, iones negativos invasores rompen ese refuerzo uniforme y crean regiones deformadas y más blandas. El ADN no muestra este ablandamiento brusco porque une los iones de manera distinta y, en su lugar, experimenta una inversión neta de carga. Estos hallazgos subrayan que no solo los iones positivos, sino también sus socios negativos, son cruciales para controlar la forma del ARN. Ese conocimiento ayudará a los investigadores a sintonizar deliberadamente la mecánica del ARN en el laboratorio —por ejemplo, para estabilizar fármacos de ARN, controlar cómo se pliega el ARN en biosensores o diseñar nanoestructuras basadas en ARN más fiables.
Cita: Zhang, C., Dong, HL., Zhang, JH. et al. Local cation-clamping distorts and softens RNA duplex. Commun Biol 9, 308 (2026). https://doi.org/10.1038/s42003-026-09580-4
Palabras clave: Mecánica del ARN, iones multivalentes, apriete de cationes, ADN frente a ARN, efectos de la sal